Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
 resolution
resolution上村 拓也*; 喜田 昭子*; 渡邉 佳彦*; 安達 基泰; 黒木 良太; 森本 幸生*
Biochemical and Biophysical Research Communications, 469(2), p.158 - 163, 2016/01
被引用回数:16 パーセンタイル:52.57(Biochemistry & Molecular Biology)The X-ray crystal structure of a salicylate hydroxylase from 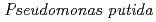 S-1 complexed with coenzyme FAD has been determined to a resolution of 2.5
S-1 complexed with coenzyme FAD has been determined to a resolution of 2.5 . Structural conservation with
. Structural conservation with 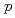 - or
- or 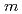 -hydroxybenzoate hydroxylase is very good throughout the topology, despite a low amino sequence identity of 20-40% between these three hydroxylases. Salicylate hydroxylase is composed of three distinct domains and includes FAD between domains I and II, which is accessible to solvent. In this study, which analyzes the tertiary structure of the enzyme, the unique reaction of salicylate, i.e. decarboxylative hydroxylation, and the structural roles of amino acids surrounding the substrate, are considered.
-hydroxybenzoate hydroxylase is very good throughout the topology, despite a low amino sequence identity of 20-40% between these three hydroxylases. Salicylate hydroxylase is composed of three distinct domains and includes FAD between domains I and II, which is accessible to solvent. In this study, which analyzes the tertiary structure of the enzyme, the unique reaction of salicylate, i.e. decarboxylative hydroxylation, and the structural roles of amino acids surrounding the substrate, are considered.
茶竹 俊行*; 佐崎 元*; 亀甲 龍彦*; 藤原 悟; 石川 卓哉*; 松本 治*; 森本 幸生*
Crystal Growth & Design, 10(3), p.1090 - 1095, 2010/03
被引用回数:4 パーセンタイル:48.29(Chemistry, Multidisciplinary)温度上昇により二本鎖DNAから一本鎖DNAへの転移が起こる熱的可逆過程を用いたDNA結晶化技術を提案した。DNA8量体(dCGCGCG)結晶の溶解度及びその融解点と二本鎖DNAから一本鎖DNAへの転移過程の関係を調べた結果、この転移過程が溶解度上昇を引き起こすことが明らかとなった。この温度による溶解度制御技術を用いることにより、少量のDNAから良質の単結晶が生成できることが示された。簡単に適用可能なこの方法は、高価な装置を用いることなく結晶の溶解度を制御できるという点で、従来の蒸気拡散法より優れている。
茶竹 俊行*; 柴山 修哉*; Park, S. Y.*; 栗原 和男; 玉田 太郎; 田中 伊知朗*; 新村 信雄*; 黒木 良太; 森本 幸生*
Journal of the American Chemical Society, 129(48), p.14840 - 14841, 2007/12
被引用回数:25 パーセンタイル:60.19(Chemistry, Multidisciplinary)A large crystal of human deoxy hemoglobin (Hb) was grown from D O solution (pD 6.3). The preliminary neutron diffraction experiment was carried out at the KUR reactor in RRI of Kyoto University, and the diffraction data set to 2.1
O solution (pD 6.3). The preliminary neutron diffraction experiment was carried out at the KUR reactor in RRI of Kyoto University, and the diffraction data set to 2.1  resolution was collected at JRR-3 reactor in JAEA using the BIX-3. The neutron crystal structure of Hb reveals that both the
resolution was collected at JRR-3 reactor in JAEA using the BIX-3. The neutron crystal structure of Hb reveals that both the  - and
- and  -distal histidines (His
-distal histidines (His 58 and His
58 and His 63) adopt fully (doubly) protonated form. This finding sharply contrasts with existing results on R (relaxed) state liganded Hbs where such full protonation can never occur. This results suggest an interesting possibility that the both histidines could contribute to the T (tense) state Bohr effect of Hb. Indeed, the protonation/deprotonation of each distal histidine may have a direct impact on the oxygen affinity of the nearby heme group through sterical hindrance and/or polarity change in the heme pocket without affecting the allosteric equilibrium of Hb.
63) adopt fully (doubly) protonated form. This finding sharply contrasts with existing results on R (relaxed) state liganded Hbs where such full protonation can never occur. This results suggest an interesting possibility that the both histidines could contribute to the T (tense) state Bohr effect of Hb. Indeed, the protonation/deprotonation of each distal histidine may have a direct impact on the oxygen affinity of the nearby heme group through sterical hindrance and/or polarity change in the heme pocket without affecting the allosteric equilibrium of Hb.
茶竹 俊行*; 栗原 和男; 黒木 良太; 森本 幸生*
no journal, ,
Proteinase K (PK) has highly activity in various environments. The aim of our study is to carry out neutron crystallographic analysis of PK for revealing detailed mechanisms of reaction and a resistance to severe environments. As for PK, it is hardly to get large crystals suitable for neutron diffraction study. Moreover, many NO ions locate on the surface of this protein, and some amino acids seemed to be distorted. At first, we found a new crystallization condition. PK crystals have so excellent quality that 1.05
ions locate on the surface of this protein, and some amino acids seemed to be distorted. At first, we found a new crystallization condition. PK crystals have so excellent quality that 1.05  X-ray diffraction data could be collected using a synchrotron radiation. Next, crystallizations were carried out in the deuterated solution. D
X-ray diffraction data could be collected using a synchrotron radiation. Next, crystallizations were carried out in the deuterated solution. D O solution had a small influence on the crystallization, and this crystallization condition was adequate for neutron experiment. Still photographs of deuterated crystals were collected with 12 hours exposure time using BIX-3 neutron diffractometer at JRR-3. Several diffraction spots could be identified.
O solution had a small influence on the crystallization, and this crystallization condition was adequate for neutron experiment. Still photographs of deuterated crystals were collected with 12 hours exposure time using BIX-3 neutron diffractometer at JRR-3. Several diffraction spots could be identified.
上村 拓也*; 喜田 昭子*; 安達 基泰; 黒木 良太; 森本 幸生*
no journal, ,
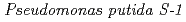 由来のサリチル酸水酸化酵素(SALH)は、分子量45kDa、分子内にFADを1つ持つフラビン酵素である。この酵素はNADHと分子状酵素の存在下でサリチル酸の脱炭酸・水酸化を同時に行いカテコールを生成する一原子酵素添加反応を触媒する。類似酵素であるパラ(PHBH)あるいはメタヒドロキシ安息香酸水酸化酵素(MHBH)は脱炭酸反応を触媒しない。これらの立体構造から、2種の反応機構の解析や活性部位周辺のアミノ酸残基の解析などが行われているが、その反応過程には不明点が多い。したがって、本酵素の反応機構を明らかにするために、基質であるサリチル酸との複合体の構造解析を行った。上記株由来の遺伝子情報からHisタグ融合酵素を大腸菌で発現させ、単離・精製・結晶化を行い、SPring-8において放射光回折実験を行い分解能2.5
由来のサリチル酸水酸化酵素(SALH)は、分子量45kDa、分子内にFADを1つ持つフラビン酵素である。この酵素はNADHと分子状酵素の存在下でサリチル酸の脱炭酸・水酸化を同時に行いカテコールを生成する一原子酵素添加反応を触媒する。類似酵素であるパラ(PHBH)あるいはメタヒドロキシ安息香酸水酸化酵素(MHBH)は脱炭酸反応を触媒しない。これらの立体構造から、2種の反応機構の解析や活性部位周辺のアミノ酸残基の解析などが行われているが、その反応過程には不明点が多い。したがって、本酵素の反応機構を明らかにするために、基質であるサリチル酸との複合体の構造解析を行った。上記株由来の遺伝子情報からHisタグ融合酵素を大腸菌で発現させ、単離・精製・結晶化を行い、SPring-8において放射光回折実験を行い分解能2.5 で構造を決定した。PHBHやMHBHでは基質であるパラあるいはメタ安息香酸のカルボキシル基を周辺のアミノ酸が保持しているが、本酵素ではこの部位はむしろFAD側に向き、保持するアミノ酸残基は存在しない。この配置から基質の脱炭酸と水酸基付与についての機構を考察した。
で構造を決定した。PHBHやMHBHでは基質であるパラあるいはメタ安息香酸のカルボキシル基を周辺のアミノ酸が保持しているが、本酵素ではこの部位はむしろFAD側に向き、保持するアミノ酸残基は存在しない。この配置から基質の脱炭酸と水酸基付与についての機構を考察した。