Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
佐藤 達彦
no journal, ,
近年研究が盛んに行われているマイクロビーム照射実験は、個々の細胞を狙って一定量の放射線を照射することが可能であり、バイスタンダー効果や適応応答など従来のビーム(ブロードビーム)を用いた実験では観測できなかったさまざまな知見が報告されている。しかし、これまでブロードビーム実験結果の指標として用いてきたマクロスケールの吸収線量"D"の概念では、各細胞内での付与エネルギー分布が不均一となるマイクロビーム実験結果を適切に表現できない。そこで、マイクロビームとブロードビーム実験に共通して使える線量概念の構築が求められていた。マイクロドジメトリの分野では、DNAや細胞スケールの微少空間内の吸収線量はspecific energy "z"として定義され、Dとは区別される。zとDの違いは、確率的な分散を持つか持たないかであり、zの平均値がDとなる。この分散の概念を導入すれば、マイクロビームとブロードビーム実験の違いは、各細胞や細胞内部における吸収線量分布(すなわちz分布)の違いで数学的に表現することができ、両実験結果は同一のモデルで解析できるようになる。発表では、マイクロビームとブロードビームを用いた細胞生存率の測定結果を、染色体と細胞核の2つのレベルでのz分布から再解析した結果を紹介するとともに、z分布の分散が生存率に与える影響について考察する。
冠城 雅晃*; 渡辺 立子; 佐藤 達彦; 横谷 明徳; Pinak, M.; 勝村 庸介*; 上坂 充*
no journal, ,
ホウ素中性子捕捉療法(BNCT)は、普及が進められている放射線治療法の一つである。BNCTでは、腫瘍にホウ素化合物が、照射した熱中性子と中性子捕捉反応を起こすことで2次粒子として低エネルギーの 粒子とリチウム粒子が生成する。これらの粒子が患部に効率的にエネルギーを付与できることから、X線治療で治療が困難な腫瘍に対しても効果が期待される。しかし、まだ臨床,研究ともに事例が少なく、生物効果の基礎的知見は十分とは言えない。そこで、われわれは、BNCTのマイクロドジメトリに着目し、生物効果をDNA損傷レベルで評価することを目的とした研究を行っている。方法は、モンテカルロ飛跡コードによる微視的線量分布に基づいて、DNA損傷の量や空間分布を評価するものである。発表では、粒子線による微小領域での線量分布,間接作用を担うOHラジカルの収率,DNAの水溶液におけるDNA鎖切断について実験データと比較検討した結果について示す。本研究は、実験等が厳しいBNCTの現状の中でシミュレーションにより有力な基礎データを提供できるものと考える。最終的には実際の治療現場に即したさまざまな条件下でのDNA損傷もシミュレーションを行っていく予定である。
粒子とリチウム粒子が生成する。これらの粒子が患部に効率的にエネルギーを付与できることから、X線治療で治療が困難な腫瘍に対しても効果が期待される。しかし、まだ臨床,研究ともに事例が少なく、生物効果の基礎的知見は十分とは言えない。そこで、われわれは、BNCTのマイクロドジメトリに着目し、生物効果をDNA損傷レベルで評価することを目的とした研究を行っている。方法は、モンテカルロ飛跡コードによる微視的線量分布に基づいて、DNA損傷の量や空間分布を評価するものである。発表では、粒子線による微小領域での線量分布,間接作用を担うOHラジカルの収率,DNAの水溶液におけるDNA鎖切断について実験データと比較検討した結果について示す。本研究は、実験等が厳しいBNCTの現状の中でシミュレーションにより有力な基礎データを提供できるものと考える。最終的には実際の治療現場に即したさまざまな条件下でのDNA損傷もシミュレーションを行っていく予定である。
渡辺 立子; 椎名 卓也*; 横谷 明徳
no journal, ,
これまでに放射線飛跡構造シミュレーションを手段としてDNAの初期損傷のスペクトルの推定を行ってきた。この結果を用いて致死等の細胞応答と初期DNA損傷の関係に対するモデルの提案を目指している。しかし、そのためには、細胞核内構造領域レベルでのクラスターDNA損傷間の位置関係に関する情報も必要であると考えられる。そこで、細胞核内でのDNA損傷推定の精度向上を図りDNA構造モデルやスペクトル解析法に改良を行ったシミュレーションシステムを用い、DNA損傷のタイプ別の収率(損傷スペクトル)、細胞核内染色体領域サイズレベルでの放射線の飛跡に沿った各タイプのDNA損傷の生成位置について解析した結果について示す。この中で、特に 線など低LET放射線においては、低線量域で生じる線量分布の不均一性に着目した解析結果についても示す。これらのシミュレーションにより得られるDNA損傷スペクトル・損傷間の相互関係に関するデータについては、おもにLETの関数として、実験で得られた細胞生存率曲線から見積もった致死損傷量と比較して議論する。
線など低LET放射線においては、低線量域で生じる線量分布の不均一性に着目した解析結果についても示す。これらのシミュレーションにより得られるDNA損傷スペクトル・損傷間の相互関係に関するデータについては、おもにLETの関数として、実験で得られた細胞生存率曲線から見積もった致死損傷量と比較して議論する。
 の運動に対する放射線影響
の運動に対する放射線影響鈴木 芳代; 坂下 哲哉; 服部 佑哉; 辻 敏夫*; 小林 泰彦
no journal, ,
有人宇宙飛行のリスクや放射線治療の副作用を考える際には、放射線被ばくの発がんリスクを評価することとともに、生命維持に必要な生体機能に対する放射線被ばくの影響を理解することが重要である。中でも、運動機能は、危険回避や捕食などを担う最も重要な機能の一つだが、運動に対する放射線影響は生体から切り離された組織や培養細胞を用いた実験系では評価できない。そこで、講演者らは、運動を指標とした行動(個体)レベルの実験系が確立されており、運動制御を担う神経が既知であるモデル生物線虫(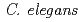 )に着目し、放射線(
)に着目し、放射線( 線,重イオンビーム)の運動への影響を調べてきた。そして、線虫の全身に
線,重イオンビーム)の運動への影響を調べてきた。そして、線虫の全身に 線を照射すると、体壁筋を駆使した全身運動(移動)や咽頭筋を駆使したポンピング運動(エサの咀しゃく・嚥下)が線量依存的に低下すること、及びこれらの運動低下が数時間後には回復することなどを明らかにした。また、一般に重イオンなどの高LET放射線は、
線を照射すると、体壁筋を駆使した全身運動(移動)や咽頭筋を駆使したポンピング運動(エサの咀しゃく・嚥下)が線量依存的に低下すること、及びこれらの運動低下が数時間後には回復することなどを明らかにした。また、一般に重イオンなどの高LET放射線は、 線のような低LET放射線に比べて高い生物効果を示すことが知られているが、線虫の運動に対する照射影響は、炭素線と
線のような低LET放射線に比べて高い生物効果を示すことが知られているが、線虫の運動に対する照射影響は、炭素線と 線との間で差がないことも明らかにした。本発表では、線虫の運動に対する放射線影響について概説するとともに、今後の研究の展開について議論する。
線との間で差がないことも明らかにした。本発表では、線虫の運動に対する放射線影響について概説するとともに、今後の研究の展開について議論する。
藤井 健太郎; 藤井 紳一郎*; 秋光 信佳*; 月本 光俊*; 小島 周二*
no journal, ,
本研究では、SPring-8原子力機構専用軟X線ビームラインBL23SUの持つ高分解能単色X線の照射により、ATPに対する軟X線照射障害を多様な生物学的特性の観点(生体エネルギー供与,遺伝情報伝達,細胞間情報伝達)から解析した。さらに、照射による分子構造変異をエレクトロスプレー質量分析装置(ESIMS)や軟X線吸収分光法により解析した。その結果、真空中で軟X線を照射したATPでは、ATP受容体活性化によるextracellular signal-regulated kinase 1/2(ERK1/2)のリン酸化活性化能、及びルシフェラーゼ活性が両者とも低下することが明らかになった。ESIMSや軟X線吸収分光法により、プリン環の分解や窒素原子の脱離が照射試料から観測されており、これらのATPの分子構造変異に起因した効果であると推測される。
漆原 あゆみ; 児玉 靖司*; 横谷 明徳
no journal, ,
Io電離放射線による生物影響の中で、遅延性影響に関与する遺伝的不安定性の誘発にはDNA2重鎖切断(DSBs)の生成が関与すると考えられている。しかし、遺伝的不安定性は数回 数十回の細胞分裂を経た後の子孫細胞で見られる現象であることから、その間DSBsがそのままの形で保持され続け、不安定性を誘発するとは考えにくく、DSBsの修復後に残存する何らかの損傷が誘発原因であると考えられる。そこで、非DSBs型の損傷である酸化型塩基損傷に着目し、DSBs以外のDNA損傷が遺伝的不安定性を誘発するのかを明らかにすることを目的として研究を行った。非DSBs型損傷である酸化型塩基損傷の生成には、DSBsを生じにくく、かつ酸化損傷を生じやすいUVAを用い、微小核細胞融合法によってUVAを照射したヒト21番染色体を非照射のマウス線維芽細胞由来株であるm5S細胞に移入することにより損傷導入細胞を作製した。作製した細胞は、ヒト21番染色体特異的なWCP-FISH法を用いてUVA照射染色体を染め分け、照射染色体と非照射染色体のそれぞれの染色体異常誘発頻度を調べた。その結果、UVA照射により生じた損傷を移入した非照射環境下のレシピエント細胞では、照射されたヒト染色体そのものに生じる染色体異常頻度の増加だけでなく、非照射であるはずのマウス染色体についても染色体数の増加や染色体異常頻度の増加を引き起こすことが明らかになった。このような直接の照射の有無にかかわらない染色体の不安定化は、移入したUVA照射染色体によって細胞全体に不安定性が誘発される可能性を示唆している。
数十回の細胞分裂を経た後の子孫細胞で見られる現象であることから、その間DSBsがそのままの形で保持され続け、不安定性を誘発するとは考えにくく、DSBsの修復後に残存する何らかの損傷が誘発原因であると考えられる。そこで、非DSBs型の損傷である酸化型塩基損傷に着目し、DSBs以外のDNA損傷が遺伝的不安定性を誘発するのかを明らかにすることを目的として研究を行った。非DSBs型損傷である酸化型塩基損傷の生成には、DSBsを生じにくく、かつ酸化損傷を生じやすいUVAを用い、微小核細胞融合法によってUVAを照射したヒト21番染色体を非照射のマウス線維芽細胞由来株であるm5S細胞に移入することにより損傷導入細胞を作製した。作製した細胞は、ヒト21番染色体特異的なWCP-FISH法を用いてUVA照射染色体を染め分け、照射染色体と非照射染色体のそれぞれの染色体異常誘発頻度を調べた。その結果、UVA照射により生じた損傷を移入した非照射環境下のレシピエント細胞では、照射されたヒト染色体そのものに生じる染色体異常頻度の増加だけでなく、非照射であるはずのマウス染色体についても染色体数の増加や染色体異常頻度の増加を引き起こすことが明らかになった。このような直接の照射の有無にかかわらない染色体の不安定化は、移入したUVA照射染色体によって細胞全体に不安定性が誘発される可能性を示唆している。
横田 裕一郎; 舟山 知夫; 武藤 泰子; 池田 裕子; 小林 泰彦
no journal, ,
本研究では放射線誘発バイスタンダー応答の時間依存性を調べた。実験では、ヒト正常繊維芽細胞WI-38株に炭素線マイクロビーム局部照射(LET=103keV/ m,10イオン/箇所),炭素線ブロードビーム全体照射(0.13Gy)又はCo-60
m,10イオン/箇所),炭素線ブロードビーム全体照射(0.13Gy)又はCo-60 線全体照射(0.2keV/
線全体照射(0.2keV/ m, 0.5Gy)した。全体照射実験では、細胞は通過できないが、培地や細胞から放出されるシグナル分子は通過できる多孔性メンブレンを挟んで、照射細胞と非照射細胞を共培養した。照射細胞とバイスタンダー細胞の比率は、マイクロビーム局所照射試料で1:20,000、全体照射試料で1:2とした。いずれの実験でも、照射から一定時間の培養後に、バイスタンダー細胞を回収して、コロニー形成率から生存率を調べた。その結果、局所照射試料では、バイスタンダー細胞の生存率は照射後6時間では変化せず、24時間で約20%低下した。一方、全体照射試料では、バイスタンダー細胞の生存率は照射後6時間以降で10から20%低下した。以上の結果から、バイスタンダー応答は照射細胞数に応じた時間依存性を示すことを明らかにした。
m, 0.5Gy)した。全体照射実験では、細胞は通過できないが、培地や細胞から放出されるシグナル分子は通過できる多孔性メンブレンを挟んで、照射細胞と非照射細胞を共培養した。照射細胞とバイスタンダー細胞の比率は、マイクロビーム局所照射試料で1:20,000、全体照射試料で1:2とした。いずれの実験でも、照射から一定時間の培養後に、バイスタンダー細胞を回収して、コロニー形成率から生存率を調べた。その結果、局所照射試料では、バイスタンダー細胞の生存率は照射後6時間では変化せず、24時間で約20%低下した。一方、全体照射試料では、バイスタンダー細胞の生存率は照射後6時間以降で10から20%低下した。以上の結果から、バイスタンダー応答は照射細胞数に応じた時間依存性を示すことを明らかにした。
坂下 哲哉; 鈴木 芳代; 武藤 泰子; 横田 裕一郎; 舟山 知夫; 浜田 信行*; 深本 花菜*; 小林 泰彦
no journal, ,
放射線被ばくにより、学習障害など神経系に影響をもたらされることが示唆されている。われわれは、これまでの研究から、全身被ばくした線虫の化学走性学習行動が、特定の条件下においてのみ影響を受けることを明らかにした。しかし、線虫のどの部位における放射線被ばくが、線虫の化学走性学習行動の変化を誘導するかは未だ明らかでない。一方、マイクロビーム照射技術は、細胞あるいは組織レベルでの直接的な放射線の影響を調べるための有効なツールとして知られている。そこで、われわれは、炭素イオンマイクロビームを用いて、線虫の化学走性学習に対する直接的な放射線の影響部位を明らかにすることを目的として研究を開始した。線虫でのマイクロビーム照射実験を実施するために、シリコン製小動物用マイクロデバイスを用いることで、線虫の動きをマイクロビーム照射時においてのみ抑制する方法を導入した。また、神経機能を麻痺させる麻酔下でのマイクロビーム照射実験を実施し、神経活動の状態の違いによる結果の比較を行った。本発表では、炭素イオンマイクロビーム照射実験の成果について最新の知見を報告する。
坂下 哲哉
no journal, ,
低線量・低フルエンス照射実験では、細胞集団の個々の細胞がポアソン分布に従い不均一に被ばくする(マクロスケール)。一方、近年研究が盛んに行われているマイクロビーム照射実験では、1個の細胞の核を狙って一定量の放射線を照射することが可能であり、1細胞ごとの正確な被ばくを評価し解析を行うことができる(マイクロスケール)。しかし、このマイクロスケールとマクロスケールの放射線影響には、バイスタンダー効果の有無や吸収線量Gyの適用限界のため、両者をつないで議論することには、未だ多くの課題が存在する。各論であるバイスタンダー効果,放射線エネルギー分布の不均一性、さらにはマイクロドジメトリに触れる前に、これらの課題をわかりやすく概説する。
赤松 憲; 鹿園 直哉
no journal, ,
電離放射線によって生じたDNA損傷は、完全に修復されなければ突然変異や発癌の原因になると言われている。特に、高LET放射線の飛跡周辺や二次電子の飛跡末端で生じやすいとされている、いわゆるクラスター損傷(複数の損傷がDNA上の狭い領域に集中的に生じている)は修復が困難とされているが、その実体はほとんど明らかになっていない。そこでわれわれは、このような仮説的な損傷を実験的に解明するために、フェルスター共鳴エネルギー移動(FRET)現象に着目した損傷位置ばらつき評価法の開発を行っている。APに蛍光プローブ(AlexaFluor350、及びAlexaFluor488型)標識したDNAオリゴマーを用いたモデル実験において、AP損傷間距離に応じたFRET効率が得られることを既に確認している(前年会PA-7)。次に、APがランダムに生じると予想される熱処理(70 C, pH5)DNA(pUC19, 2686bp)を用いて、FRET実験データ点とランダムな場合(指数分布)の理論曲線を比較した。その結果、両者は一致することがわかった。熱処理DNAにはAPがランダムに存在することを実験的に初めて確認できたといえる。本FRET法の放射線照射DNAへの適用についても報告する。
C, pH5)DNA(pUC19, 2686bp)を用いて、FRET実験データ点とランダムな場合(指数分布)の理論曲線を比較した。その結果、両者は一致することがわかった。熱処理DNAにはAPがランダムに存在することを実験的に初めて確認できたといえる。本FRET法の放射線照射DNAへの適用についても報告する。
横谷 明徳; 鵜飼 正敏; 岡 壽崇; 藤井 健太郎
no journal, ,
内殻電子励起とこれに続くAuger緩和を経た後のイオン化したDNAは、化学的に安定化した分子変化(損傷)に至る前駆体と考えられる。軟X線のエネルギーがDNAを構成する炭素,窒素,酸素のイオン化閾値より十分に高い場合は、これらの元素は2価陽イオンになる。しかしイオン化閾値に十分近い場合は、イオン化する光電子のエネルギーの速度が遅く後続のAuger電子が光電子を追い越すことで原子のポテンシャルが変化して光電子の著しい減速が起こり再び原子に捕獲される可能性がある(Post Collision Interaction (PCI)過程)。PCIが起こると原子のイオン価数も1価となり、その後の安定損傷への緩和過程も影響を受けることが予想される。本研究では、半古典的なモデルにより光電子再捕獲確率を推定した。その結果、イオン化閾値ではほぼ100%の効率で光電子は再捕獲されるが、閾値を超えると再捕獲率は急激に下がり、2eV程度超えた場合には10%程度にまでなった。これらの結果は、閾値付近で5eV程度の幅を持つEPR装置で測定された不対電子種収率の増感スペクトルを説明するには不十分であり、PCI以外の過程も不対電子収率増減に寄与していることが示唆された。
椎名 卓也; 菅谷 雄基; 白石 伊世; 渡辺 立子; 横谷 明徳; 鶴岡 千鶴*; 鈴木 雅雄*
no journal, ,
APサイトが他の損傷とクラスターを構成することでその後の修復過程に大きく影響することが多くの合成クラスター損傷を含むオリゴヌクレオチドを用いた実験により明らかにされつつある。われわれは、スキャベンジャー濃度をさまざまに変えたプラスミドDNAを試料として用い、これに異なる線質及び異なるLETの放射線を照射した際に生じるAPサイトとこれを含むクラスターDNA損傷の収率の違いを調べている。APサイトは、AP lyaseの一つである大腸菌由来のEndoculeaseIV (Nfo)で処理することで、鎖切断として検出した。試料中のスキャベンジャー濃度を変えることで、APサイト生成に果たす直接効果と間接効果の違いについても調べた。その結果、線質及びLETの違いによってNfo認識サイトの収率に差が見られた。本研究では、X線及びHIMACから得られる炭素イオンビーム(290MeV/nucleon, LET 13, 60keV/ m)の照射により生じるAPサイト及びこれを含むクラスターDNA損傷の収率を定量し、鎖切断や塩基損傷の収率に関する従来のデータと比較することで、APサイトの生成プロセスが他の損傷、特に塩基損傷の場合と異なる可能性を見いだした。
m)の照射により生じるAPサイト及びこれを含むクラスターDNA損傷の収率を定量し、鎖切断や塩基損傷の収率に関する従来のデータと比較することで、APサイトの生成プロセスが他の損傷、特に塩基損傷の場合と異なる可能性を見いだした。
白石 伊世; 椎名 卓也; 菅谷 雄基; 鹿園 直哉; 横谷 明徳
no journal, ,
クラスターDNA損傷は、SSBや塩基損傷,APサイトなどから構成されるため、これらに対する細胞応答において異なる修復系が同時にあるいは逐次的に関与することが予測される。最初に作用する修復タンパク質によりクラスター損傷の性質が変化するため、作用する修復系の順序がその後の生物応答に大きな違いをもたらす可能性がある。本研究では、クラスターDNA損傷に対する塩基除去修復酵素の作用機序の違いがクラスターDNA損傷の難修復特性にどのようにかかわるかを明らかにすることを目的とした。高LETのイオンビームを照射したプラスミドDNA(pUC18)をNthとFpgの2種類のグリコシレースで処理し、酵素活性を生じたニック(SSB)量としてpUC18の立体構造変化としてゲル電気泳動法により定量した。この際、2種類の酵素の処理の順番をさまざまに変えた時に、ニッキング活性にどのような差が見られるのかについて調べた。C6+イオンビームを照射した場合はFpgを先に処理したものの方が、同時処理やNthを先に処理したものより損傷を持たない閉環型分子の線量あたりの残存量が約5%小さい傾向にあった。講演では収量の差をもたらす原因としてのクラスター損傷の構造について議論する。
菅谷 雄基; 椎名 卓也; 白石 伊世; 藤井 健太郎; 横谷 明徳
no journal, ,
本研究では、軟X線を照射したDNAに生成される鎖切断や塩基損傷,APサイトを定量し、内殻励起やイオン化が選択的損傷生成に果たす役割を明らかにすることを目的とする。試料にはプラスミドDNA(pUC18)を用い、SPring-8のBL23SUを使用して照射を行った。ピリミジン塩基損傷及びプリン塩基損傷,APサイトの検出は、それぞれNth, Fpg, Nfoの3種類のDNAグリコシレースで処理しSSB(single strand break)に変え、アガロース電気泳動法によって定量した。その結果、酸素のK殻電子の6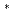 励起では各損傷の収率は他のエネルギーにおける照射と比較して、小さいことが明らかになった。この理由として、試料に含まれる塩類の酸素の内殻吸収は損傷生成に寄与していない可能性が示唆された。
励起では各損傷の収率は他のエネルギーにおける照射と比較して、小さいことが明らかになった。この理由として、試料に含まれる塩類の酸素の内殻吸収は損傷生成に寄与していない可能性が示唆された。
端 邦樹; 漆原 あゆみ; 山下 真一; 鹿園 直哉; 横谷 明徳; 室屋 裕佐*; 勝村 庸介*
no journal, ,
本研究は、抗酸化剤エダラボンの放射線防護効果の起源としてOHラジカル捕捉に加え、DNAラジカルに対する化学回復もあるのではないかと考え、エダラボンの化学回復作用の有無を調べた。まず電子線照射により生じたヌクレオチド(dGMP)ラジカルをエダラボンが還元することを、パルスラジオリシス法により示した。さらに実際のDNA分子に化学回復が機能するか否かを調べるため、プラスミドDNA溶液試料に対する 線照射を行った。照射により生じた鎖切断に加えAPサイト及び塩基損傷収率を、塩基除去修復酵素をプローブとして用いることで定量した。その結果、鎖切断に比べてAPサイトや塩基損傷がエダラボン添加により大きく抑制された。この結果は、これらのDNA損傷の前駆体であるDNAラジカルをエダラボンが化学回復することを示唆している。
線照射を行った。照射により生じた鎖切断に加えAPサイト及び塩基損傷収率を、塩基除去修復酵素をプローブとして用いることで定量した。その結果、鎖切断に比べてAPサイトや塩基損傷がエダラボン添加により大きく抑制された。この結果は、これらのDNA損傷の前駆体であるDNAラジカルをエダラボンが化学回復することを示唆している。
岡 壽崇; 横谷 明徳; 藤井 健太郎
no journal, ,
DNA核酸塩基及びDNA変異の物理化学過程の解明のため、ピリミジン核酸塩基(チミン,シトシン)と仔牛胸腺DNA薄膜のESR測定を行った。すべての薄膜において軟X線照射中のみ薄膜中に誘起される不対電子の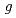 値2.000は 自由電子の
値2.000は 自由電子の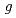 値2.0023よりも低いことから、観測されたESRシグナルはイオン化により生じた自由電子のものではことがわかった。核酸塩基のESR強度の窒素及び酸素のK殻吸収端近傍の軟X線エネルギー依存性を調べたところ、X線吸収微細構造(XANES)を反映したピークが現れた。シトシンは、イオン化閾値以上のエネルギーにおいてESR強度がXANES強度よりも2倍以上大きかったのに対し、チミンではほとんど強度が変わらなかったことから、シトシンはチミンと比べて内殻励起・イオン化による不対電子収率が高いことが示された。一方、仔牛胸腺DNA薄膜のESR強度もシトシン同様XANES強度よりも大きいことが明らかになった。これらのことから、シトシンは内殻イオン化によって生成した正孔に加えて、光電子はオージェ電子の付着の結果生じるアニオンラジカルを一緒に検出しているために不対電子収率が高かったと考えられ、DNA変異過程において電子の一時的な貯蔵庫の役割を果たしており、DNAの不対電子の起源の1つになっていることが推察される。
値2.0023よりも低いことから、観測されたESRシグナルはイオン化により生じた自由電子のものではことがわかった。核酸塩基のESR強度の窒素及び酸素のK殻吸収端近傍の軟X線エネルギー依存性を調べたところ、X線吸収微細構造(XANES)を反映したピークが現れた。シトシンは、イオン化閾値以上のエネルギーにおいてESR強度がXANES強度よりも2倍以上大きかったのに対し、チミンではほとんど強度が変わらなかったことから、シトシンはチミンと比べて内殻励起・イオン化による不対電子収率が高いことが示された。一方、仔牛胸腺DNA薄膜のESR強度もシトシン同様XANES強度よりも大きいことが明らかになった。これらのことから、シトシンは内殻イオン化によって生成した正孔に加えて、光電子はオージェ電子の付着の結果生じるアニオンラジカルを一緒に検出しているために不対電子収率が高かったと考えられ、DNA変異過程において電子の一時的な貯蔵庫の役割を果たしており、DNAの不対電子の起源の1つになっていることが推察される。
山下 真一; 廣木 章博; 長澤 尚胤; 田口 光正
no journal, ,
電子線照射により橋かけしたヒドロキシプロピルセルロース(HPC)をゲル母材とすることで、毒性が低く環境にも優しい高分子ゲル線量計を開発した。がん治療での実用的な線量範囲(1-4Gy)の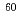 Co
Co 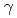 線照射に伴う白濁化が確認され、これを定量的に評価するために濁度と吸光度(透過度)の測定も実施した。濁度は4Gy以下の低線量域で直線的に10-25%増加し、増加率はゲルに浸透させる検出剤モノマーと架橋剤の比率によって変化し、この線量域では架橋剤の割合が高い方が濁度の増加率が高かった。一方、10Gy以上の高線量域では検出剤モノマーの割合が高い方が濁度の増加率が高かった。吸光度の線量に対する変化は観測波長で異なり、300-500nmの短波長領域では長波長領域(500-800nm)と異なる挙動が観測された。4Gy程度でミクロゲルによる散乱と思われるピークが300-400nm付近に出現し、このピークは照射とともに長波長側に100nm程度シフトすることもわかった。以上の結果、毒性が低く環境にも優しい高分子ゲル線量計の白濁化しやすい線量を浸透させる薬剤の組成により制御できる可能性が示された。
線照射に伴う白濁化が確認され、これを定量的に評価するために濁度と吸光度(透過度)の測定も実施した。濁度は4Gy以下の低線量域で直線的に10-25%増加し、増加率はゲルに浸透させる検出剤モノマーと架橋剤の比率によって変化し、この線量域では架橋剤の割合が高い方が濁度の増加率が高かった。一方、10Gy以上の高線量域では検出剤モノマーの割合が高い方が濁度の増加率が高かった。吸光度の線量に対する変化は観測波長で異なり、300-500nmの短波長領域では長波長領域(500-800nm)と異なる挙動が観測された。4Gy程度でミクロゲルによる散乱と思われるピークが300-400nm付近に出現し、このピークは照射とともに長波長側に100nm程度シフトすることもわかった。以上の結果、毒性が低く環境にも優しい高分子ゲル線量計の白濁化しやすい線量を浸透させる薬剤の組成により制御できる可能性が示された。
池田 裕子; 横田 裕一郎; 舟山 知夫; 武藤 泰子; 金井 達明*; 小林 泰彦
no journal, ,
近年、放射線の効果は、照射細胞だけでなく、周辺の照射されていない細胞にも現れる、いわゆるバイスタンダー効果が報告されてきた。本研究では、重粒子線がん治療における腫瘍と正常組織間の応答を明らかにするため、異細胞種間共培養実験下におけるバイスタンダー効果を解析した。実験では、ヒト胎児肺由来正常線維芽細胞株WI-38と、ヒト肺がん細胞株H1299の遺伝子改変株であるH1299/wtp53(正常p53タンパク質を発現)を使用した。炭素線照射(LET=108keV/ m, Dose=0.5Gy)又はCo-60
m, Dose=0.5Gy)又はCo-60  線照射(LET=0.2keV/
線照射(LET=0.2keV/ m, Dose=0.5Gy)した細胞と、非照射細胞を非接触で6時間又は24時間共培養した後、非照射細胞を回収して、コロニー形成率から生存率を算出した。これまでに、炭素線あるいは
m, Dose=0.5Gy)した細胞と、非照射細胞を非接触で6時間又は24時間共培養した後、非照射細胞を回収して、コロニー形成率から生存率を算出した。これまでに、炭素線あるいは 線照射したH1299/wtp53細胞と非照射のWI-38細胞を共培養したとき、WI-38細胞の生存率が増加することを見いだした。この結果から、照射したH1299/wtp53細胞はバイスタンダー細胞の接着や増殖を促進する何らかのシグナル物質を放出している可能性が考えられた。
線照射したH1299/wtp53細胞と非照射のWI-38細胞を共培養したとき、WI-38細胞の生存率が増加することを見いだした。この結果から、照射したH1299/wtp53細胞はバイスタンダー細胞の接着や増殖を促進する何らかのシグナル物質を放出している可能性が考えられた。
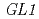 遺伝子座に生じる大規模欠失変異頻度のLET依存性
遺伝子座に生じる大規模欠失変異頻度のLET依存性長谷 純宏; 吉原 亮平; 野澤 樹; 鳴海 一成
no journal, ,
イオンビームは飛程末端近くで多くのエネルギーを付与する。飛程末端に近いイオンビームの変異誘発効果については、特に植物ではほとんど知見がない。植物におけるイオンビーム変異誘発効果に関する知見を深めるため、飛程末端に近い炭素イオン(平均LET: 425keV/ m)と平均LET 113keV/
m)と平均LET 113keV/ mの炭素イオンの変異誘発効果を比較した。シロイヌナズナの
mの炭素イオンの変異誘発効果を比較した。シロイヌナズナの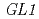 遺伝子座に生じた突然変異の特徴を大規模欠失変異に注目して解析した。野生型Col株と
遺伝子座に生じた突然変異の特徴を大規模欠失変異に注目して解析した。野生型Col株と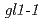 変異株を交配して得た種子を材料として用い、Colと
変異株を交配して得た種子を材料として用い、Colと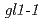 の塩基配列を区別できる多形マーカーを用いて欠失変異を検出した。無毛変異セクターの発生頻度は2種類の炭素イオン間で有意な差はなかったが、大規模欠失(
の塩基配列を区別できる多形マーカーを用いて欠失変異を検出した。無毛変異セクターの発生頻度は2種類の炭素イオン間で有意な差はなかったが、大規模欠失(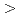
 30kb)の頻度は飛程末端に近い炭素イオンで6倍上昇した。ネオンイオン(352keV/
30kb)の頻度は飛程末端に近い炭素イオンで6倍上昇した。ネオンイオン(352keV/ m)においても、113keV/
m)においても、113keV/ mの炭素イオンに比べて大規模欠失の頻度が6.4倍上昇した。これらの結果は、植物においてLETの増大に伴って大規模欠失の割合が増加することを示唆する。
mの炭素イオンに比べて大規模欠失の頻度が6.4倍上昇した。これらの結果は、植物においてLETの増大に伴って大規模欠失の割合が増加することを示唆する。
舟山 知夫; 横田 裕一郎; 坂下 哲哉; 小林 泰彦
no journal, ,
これまでの集束式マイクロビーム装置を用いた細胞照射実験では、試料を設置した電動ステージを駆動し、細胞をビームスポットに重ねることで照射を行っていた。一方、集束式マイクロビームの特性を活かし、ビームスポットをビームスキャナで指定の位置に高速に移動することが実現できれば、細胞を高速照射できるようになる。このビームスキャナを用いた高速細胞照射の実現には、顕微鏡下で検出した細胞位置を、スキャナへの印加電圧に変換し、スポット位置を正確に制御するシステムの開発が必要となる。そこで、手はじめに細胞の画像上の位置を、ビームスキャナに印加する電圧に変換するコードを開発した。開発したコードを用い、既取得の細胞画像から変換した電圧をビームスキャナに順次印加してイオン飛跡検出プラスチックCR-39を照射、照射後にCR-39をアルカリ処理することで飛跡を可視化し、飛跡の空間分布を顕微鏡下で観察し、照射パターンを元となった細胞分布と比較した結果、描画された飛跡パターンは、元となった細胞分布と正確に合致した。この結果から、本コードを用いることで、細胞へのビームスキャナを用いた高速な照準照射が実現できることが示唆された。