Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
嘉悦 勲; 吉田 勝; 浅野 雅春; 久保 長生*; 嘉多村 孝一*; 大川 智彦*; 牧田 登之*; 今井 強一*; 真下 透*; 湯浅 久子*; et al.
人工臓器, 15(1), p.210 - 213, 1986/00
制癌剤含有ポリマー複合体を癌組織に投与した場合、薬物の組織浸透により壊死が起るが、その範囲が限定されているため、これを拡大するために、新しい担体ポリマーと薬物及びadditiveなどの組合せの検討を行なった。その結果、ラットの正常肝組織に対しては、シスプラティンを含有したDL-アラニン/ -エチル-L-アスパラテートコポリマーの複合体が薬物滲透、組織壊死の両面で最も良好であることがわかった。次いで、この系を担癌動物にも使用して有効性をしらべたところ、顕著な壊死効果が認められた。コポリペプチド以外の生体消化性ポリマーについても、担体としての効果を検討し、消化性の速いものほど有効であることを認めた。
-エチル-L-アスパラテートコポリマーの複合体が薬物滲透、組織壊死の両面で最も良好であることがわかった。次いで、この系を担癌動物にも使用して有効性をしらべたところ、顕著な壊死効果が認められた。コポリペプチド以外の生体消化性ポリマーについても、担体としての効果を検討し、消化性の速いものほど有効であることを認めた。
嘉悦 勲; 吉田 勝; 浅野 雅春; 久保 長生*; 喜多村 孝一*; 今井 強一*; 真下 透*; 湯浅 久子*; 山中 英寿*; 鈴木 慶二*
人工臓器, 15(1), p.214 - 217, 1986/00
低温放射線重合法によってnonbiodegrable vinyl copolymer中に制癌剤を包含し、徐放性針状複合体(1.6mm径、5mm長)を調製した。cisplatinを含む複合体針をウィスター系ラットの腎臓に7日間にわたって埋入留置した時、制癌剤のin vivo累積放出量は仕込みの12%であった。この値は複合体針の埋入箇所の違いによって著明に異なった。例えば、cisplatinのin vivo累積放出量は皮下埋入に対し38%、肝臓埋入に対し21%そして脳埋入に対し7%を示した。一方、徐放性制癌剤による組織壊死範囲は制癌剤の種類によって著しく異なり、例えば腎臓に対する壊死の場合、その作用はcisplain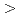 MMC
MMC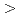 ADM
ADM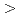 ACNU
ACNU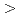 5-FUの順に減少した。しかし、脳の場合、組織の壊死作用はACNUの方がcisplatinより顕著に有効であった。従って、組織の違いによっても、徐放性制癌剤の壊死作用が異なることが結論できた。これらの結果に基づいて、ACNU含有複合体針を中心に脳腫瘍領域に適用を試みた。
5-FUの順に減少した。しかし、脳の場合、組織の壊死作用はACNUの方がcisplatinより顕著に有効であった。従って、組織の違いによっても、徐放性制癌剤の壊死作用が異なることが結論できた。これらの結果に基づいて、ACNU含有複合体針を中心に脳腫瘍領域に適用を試みた。
吉田 勝; 浅野 雅春; 嘉悦 勲; 今井 強一*; 真下 透*; 湯浅 久子*; 山中 英寿*; 久保 長生*
人工臓器, 14(2), p.830 - 833, 1985/00
放射線重合法・加圧加熱溶融法によってポリマー担体(7mg)中に制癌剤(5mg)を包含し、除放性機能と局所療法を目的とする種々の針状複合体を調製した。この複合体をラットの正常肝臓に挿入し薬物拡散と組織壊死の範囲をコントロールすることを目標として、その壊死状態を検討した。cisplatinを含む生体分解copoly(DL-alanine/ -ethyl-L-aspartate,75/25)を用いた時に最大壊死範囲(14mm径)が観察された。この場合、組織壊死は複合体挿入から3日目で最大に達した。複合体からの制癌剤の放出パターンが微量長期放出および多量短期放出タイプの場合、組織壊死は上記の範囲より著しく狭くなった。従って、肝臓組織を広範囲に壊死化するには、複合体からの制癌剤のin vivo放出は試験開始から3日程度の期間に集中させ、この期間に仕込み制癌剤量の90%以上を放出させるような複合体系が望ましいと結論した。
-ethyl-L-aspartate,75/25)を用いた時に最大壊死範囲(14mm径)が観察された。この場合、組織壊死は複合体挿入から3日目で最大に達した。複合体からの制癌剤の放出パターンが微量長期放出および多量短期放出タイプの場合、組織壊死は上記の範囲より著しく狭くなった。従って、肝臓組織を広範囲に壊死化するには、複合体からの制癌剤のin vivo放出は試験開始から3日程度の期間に集中させ、この期間に仕込み制癌剤量の90%以上を放出させるような複合体系が望ましいと結論した。