Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
 -glucanase from
-glucanase from 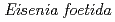
有森 貴夫*; 伊藤 彰紘*; 中澤 昌美*; 上田 光宏*; 玉田 太郎
Journal of Synchrotron Radiation, 20(6), p.884 - 889, 2013/11
被引用回数:17 パーセンタイル:65.54(Instruments & Instrumentation)セルロースを含む木質バイオマスからのバイオエタノール生産における糖化プロセスにおいて、(293K以下でも十分な活性を示す)低温寛容性セルラーゼを用いることができれば、加熱するためのエネルギーを節約できるだけではなく、並行複発酵による高濃度アルコール生産が可能となる。GHファミリー9に属するシマミミズ由来1,4- -エンドグルカナーゼ(EF-EG2)は313Kにおいて最大活性を示すが、283Kにおいても比較的高い活性を保持する。酵母を用いた組換え型EF-EG2の発現系を構築し、引き続き試料精製および結晶化を実施したところ、回折実験可能な針状結晶を得ることに成功した。この結晶を用いて放射光施設において1.5
-エンドグルカナーゼ(EF-EG2)は313Kにおいて最大活性を示すが、283Kにおいても比較的高い活性を保持する。酵母を用いた組換え型EF-EG2の発現系を構築し、引き続き試料精製および結晶化を実施したところ、回折実験可能な針状結晶を得ることに成功した。この結晶を用いて放射光施設において1.5 分解能の回折データを収集し、結晶学的
分解能の回折データを収集し、結晶学的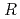 値が14.7%(free-
値が14.7%(free-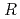 値が16.8%)まで精密化を完了した。EF-EG2の全体構造は(
値が16.8%)まで精密化を完了した。EF-EG2の全体構造は( /
/ )
)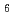 バレルから成り、その中心に活性部位と想定されるクレフトが確認された。また、分子表面は負電荷に富んでいたが、この特徴は構造既知の低温寛容性酵素においても広く観察されており、EF-EG2の低温寛容性との関連が示唆された。
バレルから成り、その中心に活性部位と想定されるクレフトが確認された。また、分子表面は負電荷に富んでいたが、この特徴は構造既知の低温寛容性酵素においても広く観察されており、EF-EG2の低温寛容性との関連が示唆された。
 -glucanase from Eisenia foetida
-glucanase from Eisenia foetida有森 貴夫*; 伊藤 彰紘*; 中澤 昌美*; 上田 光宏*; 玉田 太郎
no journal, ,
We cloned the gene for endo-1,4- -glucanase from Eisenia foetida (EF-EG2) consisting of 1368 bp encoding 456 amino acid residues. The amino acid sequence of the gene shares sequence homology (
-glucanase from Eisenia foetida (EF-EG2) consisting of 1368 bp encoding 456 amino acid residues. The amino acid sequence of the gene shares sequence homology (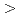 50%) with endo-1,4-
50%) with endo-1,4- -glucanases belonging to glycoside hydrolase family 9. The recombinant EF-EG2 showed highest activity at 40
-glucanases belonging to glycoside hydrolase family 9. The recombinant EF-EG2 showed highest activity at 40 C, and also retained a comparatively high activity at 10
C, and also retained a comparatively high activity at 10 C. We purified the recombinant EF-EG2 expressed in Pichia pastoris, and then grew needle shaped EF-EG2 crystals with dimensions of 0.02
C. We purified the recombinant EF-EG2 expressed in Pichia pastoris, and then grew needle shaped EF-EG2 crystals with dimensions of 0.02  0.02
0.02  1 mm. Diffraction data of EF-EG2 was collected at beamline 1A, Photon Factory, KEK, and integrated and scaled to 2.1
1 mm. Diffraction data of EF-EG2 was collected at beamline 1A, Photon Factory, KEK, and integrated and scaled to 2.1  resolution. The crystals belonged to space group
resolution. The crystals belonged to space group 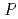 3
3 21 with unit-cell parameters of
21 with unit-cell parameters of 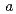 =
= 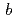 = 135
= 135  ,
, 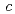 =54.9
=54.9  . The location of one EF-EG2 molecule in the asymmetric unit was identified by molecular replacement analysis using the coordinates of endoglucanase from Nasutitermes takasagoensis (NtEgl). The final model of EF-EG2 was refined to a crystallographic
. The location of one EF-EG2 molecule in the asymmetric unit was identified by molecular replacement analysis using the coordinates of endoglucanase from Nasutitermes takasagoensis (NtEgl). The final model of EF-EG2 was refined to a crystallographic 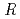 -factor of 17.9% (free R-factor of 21.4%) to 2.1
-factor of 17.9% (free R-factor of 21.4%) to 2.1  resolution. Overall structure of EF-EG2 is similar to that of NtEgl with an RMSD value of 0.9
resolution. Overall structure of EF-EG2 is similar to that of NtEgl with an RMSD value of 0.9  for 423 C
for 423 C atoms, however, a slight difference between both structures was confirmed around substrate binding site.
atoms, however, a slight difference between both structures was confirmed around substrate binding site.
 -エンドグルカナーゼの結晶構造解析
-エンドグルカナーゼの結晶構造解析有森 貴夫*; 伊藤 彰紘*; 中澤 昌美*; 上田 光宏*; 玉田 太郎
no journal, ,
植物バイオマスを糖化する際、従来の高温条件下ではなく、低温条件下で効率よく糖化できれば、加温するためのエネルギーを節約することができる。最近われわれは、シマミミズ由来1,4- -エンドグルカナーゼ(EF-EG2)のクローニングに成功した。本酵素は、40
-エンドグルカナーゼ(EF-EG2)のクローニングに成功した。本酵素は、40 において最大活性を示すが、低温(20
において最大活性を示すが、低温(20 C)条件においても比較的高い活性を保持する。EF-EG2は、456アミノ酸残基から構成される約50kDaの酵素であり、GHファミリー9に属するタカサゴアリ由来の1,4-
C)条件においても比較的高い活性を保持する。EF-EG2は、456アミノ酸残基から構成される約50kDaの酵素であり、GHファミリー9に属するタカサゴアリ由来の1,4- -エンドグルカナーゼ(NTEgl)と高いアミノ酸配列相同性(55%)を有している。われわれは、EF-EG2が低温においても高い活性を保持する機構を立体構造情報から理解することを目的に、EF-EG2の結晶構造解析に取り組んだ。酵母を用いた組換え型酵素の発現系を構築し、引き続き試料精製、結晶化スクリーニング、結晶化条件の最適化を実施した結果、回折実験可能な針状のEF-EG2結晶を得ることに成功した。この結晶を用いて放射光施設において、2.1
-エンドグルカナーゼ(NTEgl)と高いアミノ酸配列相同性(55%)を有している。われわれは、EF-EG2が低温においても高い活性を保持する機構を立体構造情報から理解することを目的に、EF-EG2の結晶構造解析に取り組んだ。酵母を用いた組換え型酵素の発現系を構築し、引き続き試料精製、結晶化スクリーニング、結晶化条件の最適化を実施した結果、回折実験可能な針状のEF-EG2結晶を得ることに成功した。この結晶を用いて放射光施設において、2.1 分解能の回折データを収集し、引き続き既知のNTEglの構造情報を用いた分子置換法による位相決定、及び構造精密化を完了した。EF-EG2の全体構造は、一般的なGH9酵素と同様、(
分解能の回折データを収集し、引き続き既知のNTEglの構造情報を用いた分子置換法による位相決定、及び構造精密化を完了した。EF-EG2の全体構造は、一般的なGH9酵素と同様、( /
/ )
)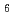 バレル構造をしていたが、糖結合部位付近の構造には他のGH9酵素との構造とわずかな相違がみられた。本発表では、得られたEF-EG2の立体構造と他のGH9酵素の立体構造との詳細比較から、EF-EG2の活性発現及び低温耐性機構について議論したい。
バレル構造をしていたが、糖結合部位付近の構造には他のGH9酵素との構造とわずかな相違がみられた。本発表では、得られたEF-EG2の立体構造と他のGH9酵素の立体構造との詳細比較から、EF-EG2の活性発現及び低温耐性機構について議論したい。
玉田 太郎; 有森 貴夫*; 福原 宏章*; 伊藤 彰紘*; 上田 光宏*
no journal, ,
セルロースを含む木質バイオマスからのバイオエタノール生産における糖化プロセスにおいて、低温適応性セルラーゼを用いることができれば、加熱するためのエネルギーを節約できるだけではなく、並行複発酵による高濃度アルコール生産が可能となる。GHファミリー9に属するシマミミズ由来1,4- -エンドグルカナーゼ(EF-EG2)は313Kにおいて最大活性を示すが、283Kにおいても比較的高い活性を保持する。酵母を用いた組換え型EF-EG2の発現系を構築し、引き続き試料精製および結晶化を実施したところ、太さ0.02mm程度の針状結晶を得ることに成功した。この結晶を用いて1.50
-エンドグルカナーゼ(EF-EG2)は313Kにおいて最大活性を示すが、283Kにおいても比較的高い活性を保持する。酵母を用いた組換え型EF-EG2の発現系を構築し、引き続き試料精製および結晶化を実施したところ、太さ0.02mm程度の針状結晶を得ることに成功した。この結晶を用いて1.50 分解能の回折データを収集し、結晶学的
分解能の回折データを収集し、結晶学的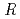 値が14.7%(free-
値が14.7%(free-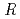 値が16.8%)まで精密化を完了した。さらに、触媒残基と想定されるGlu431をGlnに置換した変異体(E431Q)と基質(セロトリオース)複合体結晶を作製し、1.55
値が16.8%)まで精密化を完了した。さらに、触媒残基と想定されるGlu431をGlnに置換した変異体(E431Q)と基質(セロトリオース)複合体結晶を作製し、1.55 分解能の回折データを収集した。現在、精密化中であるが、サブサイト-2
分解能の回折データを収集した。現在、精密化中であるが、サブサイト-2 -4にセロトリオース由来の明瞭な電子密度を観測することができた。また、分子表面は負電荷に富んでいたが、この特徴は構造既知の低温適応性酵素においても広く観察されており、EF-EG2の低温適応性との関連が示唆された。
-4にセロトリオース由来の明瞭な電子密度を観測することができた。また、分子表面は負電荷に富んでいたが、この特徴は構造既知の低温適応性酵素においても広く観察されており、EF-EG2の低温適応性との関連が示唆された。