Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
 -sheet-rich prion protein in scrapie-infected neuroblastoma cells with human IgG1 antibody specific for
-sheet-rich prion protein in scrapie-infected neuroblastoma cells with human IgG1 antibody specific for  -form prion protein
-form prion protein久保田 俊也*; 濱添 勇太*; 橋口 周平*; 石橋 大輔*; 赤坂 一之*; 西田 教行*; 片峰 茂*; 坂口 末廣*; 黒木 良太; 中島 敏博*; et al.
Journal of Biological Chemistry, 287(17), p.14023 - 14039, 2012/04
被引用回数:5 パーセンタイル:11.64(Biochemistry & Molecular Biology)遺伝子組み換え型の -sheet-rich recombinant full-length prion protein (
-sheet-rich recombinant full-length prion protein ( -form PrP)を準備し、この
-form PrP)を準備し、この -form PrPとヒト一本鎖抗体を提示したファージライブラリを用いて、
-form PrPとヒト一本鎖抗体を提示したファージライブラリを用いて、 -formではなく
-formではなく -form PrPに特異的なヒトIgG1抗体(PRB7 IgG)を確立した。プリオンに感染したScN2a細胞をPRB7 IgGと共培養させると、細胞質中でPRB7結合粒子が生成蓄積され、その結果、非常に大きなPRB7結合凝集体を生成するアポトーシスを起こした細胞となる。全長PrPのN末端のオクタリピート領域を認識するSAF32抗体は、共焦点顕微鏡法で決定されるようにこれらの細胞内の明瞭な粒子を染色した。PRB7 IgG又はSAF32の存在下で培養されたプリオン感染ScN2a細胞内でPK抵抗性PrPの蓄積を観察すると、SAF32によって強く阻害されたが、PRB7 IgGによっては全く阻害されなかった。このようにして、ScN2a細胞内の
-form PrPに特異的なヒトIgG1抗体(PRB7 IgG)を確立した。プリオンに感染したScN2a細胞をPRB7 IgGと共培養させると、細胞質中でPRB7結合粒子が生成蓄積され、その結果、非常に大きなPRB7結合凝集体を生成するアポトーシスを起こした細胞となる。全長PrPのN末端のオクタリピート領域を認識するSAF32抗体は、共焦点顕微鏡法で決定されるようにこれらの細胞内の明瞭な粒子を染色した。PRB7 IgG又はSAF32の存在下で培養されたプリオン感染ScN2a細胞内でPK抵抗性PrPの蓄積を観察すると、SAF32によって強く阻害されたが、PRB7 IgGによっては全く阻害されなかった。このようにして、ScN2a細胞内の -sheet-rich PrPの産生・蓄積の直接的証拠を新たに掴んだ。これらの結果は、(1)PRB7結合PrPが、
-sheet-rich PrPの産生・蓄積の直接的証拠を新たに掴んだ。これらの結果は、(1)PRB7結合PrPが、 -form PrP凝集体の蓄積に寄与していず、むしろ結果としてアポトーシス細胞死を引き起こす最終産物である、(2)PRB7が認識する
-form PrP凝集体の蓄積に寄与していず、むしろ結果としてアポトーシス細胞死を引き起こす最終産物である、(2)PRB7が認識する -formが欠乏したSAF32結合PrPは伝播性を伴ういわゆるPrP
-formが欠乏したSAF32結合PrPは伝播性を伴ういわゆるPrP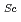 かもしれない、ということを示唆している。PRB7は、
かもしれない、ということを示唆している。PRB7は、 -form PrPに特異的な最初のヒト抗体であり、生化学的,病理学的なプリオンを特徴付けるための強力なツールになると考えられる。
-form PrPに特異的な最初のヒト抗体であり、生化学的,病理学的なプリオンを特徴付けるための強力なツールになると考えられる。
杉山 晃一*; 郷 慎太郎*; 富松 太郎*; 甲斐 民人*; 長江 大輔*; 石橋 優一*; 松永 壮太郎*; 永田 優斗*; 西畑 洸希*; 鷲山 広平*; et al.
no journal, ,
中性子過剰重アクチノイド核の励起準位構造を明らかにするため、アイソマースコープ法を用いたアクチノイド核のインビーム 線分光実験を実施した。中性子過剰重アクチノイド核は、原子力機構タンデム加速器で加速したO-18(
線分光実験を実施した。中性子過剰重アクチノイド核は、原子力機構タンデム加速器で加速したO-18(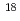 O)ビームをCm-248(
O)ビームをCm-248(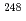 Cm)標的に照射して多核子移行反応で合成した。後方に散乱したビーム様粒子をSi E-
Cm)標的に照射して多核子移行反応で合成した。後方に散乱したビーム様粒子をSi E-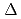 E検出器で検出して生成核を識別し、前方方向に散乱された標的様粒子の核異性体を60mm程度下流に設置したアルミ板で捕集した。アルミ板の周囲に4台のGe検出器及び4台のLaBr検出器を設置して、捕集された核異性体からの
E検出器で検出して生成核を識別し、前方方向に散乱された標的様粒子の核異性体を60mm程度下流に設置したアルミ板で捕集した。アルミ板の周囲に4台のGe検出器及び4台のLaBr検出器を設置して、捕集された核異性体からの 線を測定した。標的と検出器の間にタングステン遮蔽を設置して標的から放出される多量の
線を測定した。標的と検出器の間にタングステン遮蔽を設置して標的から放出される多量の 線を遮蔽し、アクチノイド核異性体からの
線を遮蔽し、アクチノイド核異性体からの 線を感度良く検出することに成功した。
線を感度良く検出することに成功した。