Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
 ladder
ladder上田 宏*; 小野田 繁樹*; 山口 泰弘*; 木村 剛*; 吉澤 大智*; 森岡 俊晶*; 萩原 政幸*; 萩原 雅人*; 左右田 稔*; 益田 隆嗣*; et al.
Physical Review B, 101(14), p.140408_1 - 140408_6, 2020/04
被引用回数:4 パーセンタイル:26.53(Materials Science, Multidisciplinary)We report experimental and theoretical evidence that Rb Cu
Cu Mo
Mo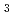 O
O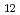 has a nonmagnetic tetramer ground state of a two-leg ladder comprising antiferromagnetically coupled frustrated spin-
has a nonmagnetic tetramer ground state of a two-leg ladder comprising antiferromagnetically coupled frustrated spin-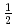 chains and exhibits a Haldane spin gap of emergent spin-1 pairs. Three spin excitations split from the spin-1 triplet by a Dzyaloshinskii-Moriya interaction are identified in inelastic neutron-scattering and electron spin resonance spectra. A tiny magnetic field generates ferroelectricity without closing the spin gap, indicating a unique class of ferroelectricity induced by a vector spin chirality order.
chains and exhibits a Haldane spin gap of emergent spin-1 pairs. Three spin excitations split from the spin-1 triplet by a Dzyaloshinskii-Moriya interaction are identified in inelastic neutron-scattering and electron spin resonance spectra. A tiny magnetic field generates ferroelectricity without closing the spin gap, indicating a unique class of ferroelectricity induced by a vector spin chirality order.
松尾 龍人; 荒田 敏昭*; 小田 俊郎*; 中島 健次; 河村 聖子; 菊地 龍弥; 藤原 悟
Biochemistry and Biophysics Reports (Internet), 6, p.220 - 225, 2016/07
Hydration water is essential for a protein to perform its biological function properly. In this study, the dynamics of hydration water around F-actin and myosin subfragment-1 (S1), which are the partner proteins playing a major role in various cellular functions related to cell motility, was characterized by incoherent quasielastic neutron scattering (QENS). The QENS spectra of hydration water around F-actin and S1 provided the translational diffusion coefficient, the residence time, and the rotational correlation time. The differences in these parameters indicate a significant difference in mobility of the hydration water between S1 and F-actin: S1 has the typical hydration water, the mobility of which is reduced compared with that of bulk water, while F-actin has the unique hydration water, the mobility of which is close to that of bulk water rather than the typical hydration water around proteins.
松尾 龍人; 武田 壮一*; 小田 俊郎*; 藤原 悟
Biophysics and Physicobiology (Internet), 12, p.145 - 158, 2015/12
Troponin (Tn), consisting of three subunits, TnC, TnI, and TnT, is a protein that plays a major role in regulation of muscle contraction. Various mutations of Tn cause familial hypertrophic cardiomyopathy. Here we focus on the mutations E244D and K247R of TnT, which induce an increase in the maximum tension of cardiac muscle without changes in Ca -sensitivity, and carried out small-angle X-ray scattering experiments on the Tn core domain containing the wild type subunits and those containing the mutant TnT in the absence and presence of Ca
-sensitivity, and carried out small-angle X-ray scattering experiments on the Tn core domain containing the wild type subunits and those containing the mutant TnT in the absence and presence of Ca . Changes in the overall shape induced by the mutations were detected for the first time by the changes in the radius of gyration and the maximum dimension between the wild type and the mutants. Analysis by model calculations shows that TnC adopts a dumbbell structure regardless of the mutations, and that the mutations change the distributions of the conformational ensembles so that the flexible N- and C-terminal regions of TnT become close to the center of the whole molecule.
. Changes in the overall shape induced by the mutations were detected for the first time by the changes in the radius of gyration and the maximum dimension between the wild type and the mutants. Analysis by model calculations shows that TnC adopts a dumbbell structure regardless of the mutations, and that the mutations change the distributions of the conformational ensembles so that the flexible N- and C-terminal regions of TnT become close to the center of the whole molecule.
山鹿 親信; 富川 裕文; 小林 直樹; 直井 洋介; 小田 哲三; 持地 敏郎
JAEA-Review 2015-023, 108 Pages, 2015/10
日本原子力研究開発機構は、2014年12月3日に、「原子力平和利用と核不拡散・核セキュリティに係る国際フォーラム-エネルギー基本計画を受け今後の核不拡散向上のための方向性及び人材育成COEのあり方について-」を開催した。フォーラムでは、日米の政府関係者が原子力平和利用と核不拡散・核セキュリティに係る取組みや日本への期待等について講演した。パネル討論では、「国内外の情勢を踏まえた効果的・効率的な核不拡散確保のための方策と技術開発の役割及びその方向性」、「核不拡散・核セキュリティ人材育成の中核拠点(COE)の役割と今後にむけた期待」という2つのテーマで議論が行われた。前者では、核不拡散を確保しつつ効果的・効率的な保障措置の実施及びプルトニウム利用の透明性確保のための制度的、技術的方策、技術開発の役割と方向性について議論を行った。後者では核不拡散・核セキュリティの強化に向けて、各国のCOEが今後、どのような貢献をし、実現していくかについて議論した。本報告書は、同フォーラムの基調講演の要旨、パネル討論の概要及びパネル討論で使用された発表資料を収録したものである。
松尾 龍人; 荒田 敏昭*; 小田 俊郎*; 中島 健次; 河村 聖子; 菊地 龍弥; 藤原 悟
Biochemical and Biophysical Research Communications, 459(3), p.493 - 497, 2015/04
被引用回数:4 パーセンタイル:12.91(Biochemistry & Molecular Biology)Various biological functions related to cell motility are driven by the interaction between the partner proteins, actin and myosin. To obtain insights into how this interaction occurs, the internal dynamics of F-actin and myosin subfragment-1 (S1) were characterized by quasielastic neutron scattering measurements on the solution samples of F-actin and S1. Contributions of the internal motions of the proteins to the scattering spectra were separated from those of the global macromolecular diffusion. Analysis of the spectra arising from the internal dynamics showed that the correlation times of the atomic motions were about two times shorter for F-actin than for S1, suggesting that F-actin fluctuates more rapidly than S1. It was also shown that the fraction of the immobile atoms is larger for S1 than for F-actin. These results suggest that F-actin actively facilitates the binding of myosin by utilizing the more frequent conformational fluctuations than those of S1.
松尾 龍人; 荒田 敏昭*; 小田 俊郎*; 藤原 悟
Biophysics, 9, p.99 - 106, 2013/07
Hydration structures around F-actin and myosin subfragment-1 (S1), which play central roles as counterparts in muscle contraction, were investigated by small-angle X-ray scattering (SAXS) and small-angle neutron scattering (SANS). The radius of gyration of S1 was evaluated to be 41.3  1.1
1.1  for SAXS, 40.1
for SAXS, 40.1  3.0
3.0  for SANS in H
for SANS in H O, and 37.8
O, and 37.8  0.8
0.8  for SANS in D
for SANS in D O, respectively. The values of the cross-sectional radius of gyration of F-actin were 25.4
O, respectively. The values of the cross-sectional radius of gyration of F-actin were 25.4  0.03
0.03  for SAXS, 23.4
for SAXS, 23.4  2.4
2.4  for SANS in H
for SANS in H O, and 22.6
O, and 22.6  0.6
0.6  for SANS in D
for SANS in D O, respectively. Analysis showed that the hydration shell of S1 has the average density 10-15% higher than bulk water, being the typical hydration shell, while the hydration shell of F-actin has the average density more than 19% higher than bulk water, indicating that F-actin has a denser, unusual hydration structure. The results indicate a difference in the hydration structures around F-actin and S1.
O, respectively. Analysis showed that the hydration shell of S1 has the average density 10-15% higher than bulk water, being the typical hydration shell, while the hydration shell of F-actin has the average density more than 19% higher than bulk water, indicating that F-actin has a denser, unusual hydration structure. The results indicate a difference in the hydration structures around F-actin and S1.
藤原 悟; Plazanet, M.*; 小田 俊郎*
Biochemical and Biophysical Research Communications, 431(3), p.542 - 546, 2013/02
被引用回数:4 パーセンタイル:11.19(Biochemistry & Molecular Biology)Quasi-elastic neutron scattering experiments of powder samples of F-actin and G-actin, hydrated either with D O or H
O or H O, at hydration ratios of 0.4 and 1.0, were performed. Combined analysis of the quasi-elastic neutron scattering spectra provided the parameters characterizing the water dynamics in the first hydration layer and those outside of the first layer. The translational diffusion coefficients (D
O, at hydration ratios of 0.4 and 1.0, were performed. Combined analysis of the quasi-elastic neutron scattering spectra provided the parameters characterizing the water dynamics in the first hydration layer and those outside of the first layer. The translational diffusion coefficients (D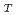 ) of the hydration water in the first layer were found to be 1.2
) of the hydration water in the first layer were found to be 1.2  10
10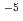 cm
cm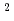 /s and 1.7
/s and 1.7  10
10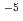 cm
cm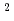 /s for F-actin and G-actin, respectively, while that for bulk water was 2.8
/s for F-actin and G-actin, respectively, while that for bulk water was 2.8  10
10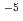 cm
cm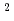 /s. The residence times were 6.6 ps and 5.0 ps for F-actin and G-actin, respectively, while that for bulk water was 0.63 ps. These differences between F-actin and G-actin, indicating that the hydration water around G-actin is more mobile than that around F-actin, are in concert with the results of the internal dynamics of F-actin and G-actin, showing that G-actin fluctuates more rapidly than F-actin. This implies that the dynamics of the hydration water is coupled to the internal dynamics of the actin molecules. The D
/s. The residence times were 6.6 ps and 5.0 ps for F-actin and G-actin, respectively, while that for bulk water was 0.63 ps. These differences between F-actin and G-actin, indicating that the hydration water around G-actin is more mobile than that around F-actin, are in concert with the results of the internal dynamics of F-actin and G-actin, showing that G-actin fluctuates more rapidly than F-actin. This implies that the dynamics of the hydration water is coupled to the internal dynamics of the actin molecules. The D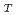 values of the water molecules outside of the first hydration layer were found to be similar to that of bulk water though the residence times are strongly affected by the first hydration layer. This supports the recent observation on intracellular water that shows bulk-like behavior.
values of the water molecules outside of the first hydration layer were found to be similar to that of bulk water though the residence times are strongly affected by the first hydration layer. This supports the recent observation on intracellular water that shows bulk-like behavior.
伊藤 拓人*; 出来 真斗; 富田 卓朗*; 松尾 繁樹*; 橋本 修一*; 北田 貴弘*; 井須 俊郎*; 小野田 忍; 大島 武
Proceedings of 12th International Symposium on Laser Precision Microfabrication (LPM 2011) (Internet), 5 Pages, 2011/06
The polarization dependence of local electric conductivity in Silicon carbide (SiC) modified by femtosecond laser (fs-laser) was studied. The surface of SiC was irradiated by fs-laser with the different polarization configurations. In the case that the scanning direction is parallel to the electric field, the local electric conductivity drastically increases with increasing fs-laser fluence. On the other hand, in the case that the scanning direction is perpendicular to electric field, the local electric conductivity slightly increase with increasing fluence. According to Raman spectroscopy and secondary electron microscope observation, we found that the amorphous-Si, -C, -SiC are created for parallel irradiation, but the amorphous-SiC is created for perpendicular irradiation. Therefore, we suggests that the polarization dependence of local electric conductivity is due to the chemical composition of laser modified region.
藤原 悟; Plazanet, M.*; 松本 富美子; 小田 俊郎*
European Biophysics Journal, 40(5), p.661 - 671, 2011/05
被引用回数:10 パーセンタイル:30.04(Biophysics)The quasielastic neutron scattering (QENS) experiments were carried out to characterize the internal dynamics of the protein, actin in the polymerized form (F-actin) and the monomeric form (G-actin). To investigate the effects of hydration, the measurements were done on the powder samples containing only the first layer of hydration water, and those containing more layers of water. The QENS spectra obtained indicated that the internal motions of both F-actin and G-actin have distributions of motions with distinct correlation times and amplitudes. Increasing hydration changes relative populations of these distinct motions. The effects of hydration were shown to be different between F-actin and G-actin. The elastic incoherent neutron scattering measurements provided the concerted results. The observed effects were interpreted in terms of the differences in the dynamical heterogeneity of G-actin and F-actin.
出来 真斗; 伊藤 拓人*; 山本 稔*; 富田 卓朗*; 松尾 繁樹*; 橋本 修一*; 北田 貴弘*; 井須 俊郎*; 小野田 忍; 大島 武
Applied Physics Letters, 98(13), p.133104_1 - 133104_3, 2011/03
被引用回数:13 パーセンタイル:49.19(Physics, Applied)Enhancement of local electric conductivity in Silicon Carbide (SiC) induced by irradiation of femtosecond laser was studied. Current-voltage characteristics of the laser-modified regions were measured. As a result, it was found that the conductivity increases with increase in the fluence, and the conductivity sharply increases in the fluence range from 5.0 to 6.7 J/cm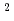 . The conductivity of modified region at the irradiation fluence of 53 J/cm
. The conductivity of modified region at the irradiation fluence of 53 J/cm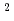 is six orders of magnitude higher than the non irradiated one. From the current-voltage characteristics and the scanning electron microscope observations, we conclude that the drastic change in electrical conductivity is assumed to be associated with the phase transition induced by femtosecond laser.
is six orders of magnitude higher than the non irradiated one. From the current-voltage characteristics and the scanning electron microscope observations, we conclude that the drastic change in electrical conductivity is assumed to be associated with the phase transition induced by femtosecond laser.
出来 真斗; 伊藤 拓人*; 富田 卓朗*; 松尾 繁樹*; 橋本 修一*; 北田 貴弘*; 井須 俊郎*; 小野田 忍; 大島 武
Proceedings of 9th International Workshop on Radiation Effects on Semiconductor Devices for Space Applications (RASEDA-9), p.218 - 221, 2010/10
Femtosecond laser exhibits extremely high peak intensity and short pulse duration, and can process inside transparent materials without damaging the surface of sample. In this study, the local electrical conductivity in Silicon Carbide (SiC) is evaluated. As a result of femtosecond laser irradiation with various irradiation fluences, the drastic change of electrical conductivity is observed in resistivity ranges from 10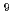 to 10
to 10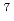
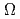 . It is found that the local conductivity strongly depends on the fluence. We suggest that the local conductivity is attributed to the phase transition. From the surface observations by Secondary Electron Microscopy (SEM), we conclude that the formation of the classical laser-induced periodic structures causes the sudden increase in the electrical conductivities.
. It is found that the local conductivity strongly depends on the fluence. We suggest that the local conductivity is attributed to the phase transition. From the surface observations by Secondary Electron Microscopy (SEM), we conclude that the formation of the classical laser-induced periodic structures causes the sudden increase in the electrical conductivities.
松本 富美子; 弟子丸 俊吾*; 小田 俊郎*; 藤原 悟
Analytical Biochemistry, 399(2), p.299 - 301, 2010/04
被引用回数:2 パーセンタイル:58.78(Biochemical Research Methods)天然の筋肉の細いフィラメント及び大腸菌に発現させた組換えトロポニン構成成分から筋肉の細いフィラメントを再構成する技術を開発した。この技術により、pH6.2において20%グルセロール及び0.3M KCl存在下で、再構成されたトロポニン複合体が天然の細いフィラメント中に交換導入される。90%以上の内在トロポニン複合体が組換えトロポニン複合体に交換される。この技術により調製された再構成細いフィラメントの構造及びCa 感受性が保持されることが、X線繊維回折測定、並びに、細いフィラメントにより活性化されるミオシンサブフラグメント1のATP分解活性の測定により確認された。
感受性が保持されることが、X線繊維回折測定、並びに、細いフィラメントにより活性化されるミオシンサブフラグメント1のATP分解活性の測定により確認された。
富田 卓朗*; 岩見 勝弘*; 山本 稔*; 出来 真斗*; 松尾 繁樹*; 橋本 修一*; 中川 圭*; 北田 貴弘*; 井須 俊郎*; 齋藤 伸吾*; et al.
Materials Science Forum, 645-648, p.239 - 242, 2010/04
フェムト秒レーザーを用いて炭化ケイ素(SiC)の改質を試みた。フーリエ変換赤外分光法(FTIR)法を用いて改質領域を調べた結果、残留線バンドの強度が減少し、この現象が結晶性の劣化によるものと説明できた。また、残留線バンドが偏波依存性を有することがわかり、この特性を活かすことで赤外領域で動作する光学素子への応用が期待できる。電流電圧特性測定とホール係数測定の結果、改質後の電気伝導度が改質前に比べて4桁以上も大きい5.9 10
10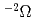 mになることがわかり、フェムト秒レーザーによりSiCの電気特性を改質できることを明らかにした。
mになることがわかり、フェムト秒レーザーによりSiCの電気特性を改質できることを明らかにした。
藤原 悟; Plazanet, M.*; 松本 富美子; 小田 俊郎*
Biophysical Journal, 94(12), p.4880 - 4889, 2008/06
被引用回数:9 パーセンタイル:21.55(Biophysics)アクチンは、ほぼすべての真核細胞内に存在し、細胞運動や輸送等にかかわる実に多様な機能を持つ。アクチン単量体(G-アクチン)は重合して繊維状重合体(F-アクチン)を形成するが、多様なアクチンの機能は、種々の蛋白質との相互作用を可能とするF-アクチンの柔らかさのゆえである。F-アクチンの柔らかさの起源を明らかにするための第一段階として、われわれはピコ領域におけるアクチンの運動特性の測定を、中性子非干渉性弾性散乱(EINS)法を用いて行った。G-アクチン及びF-アクチンの水和粉末試料についてEINS測定を行い、アクチン分子内の原子の平均自乗変位の温度依存性を調べた。その結果、平均自乗変位には150K付近及び245K付近に2つの転移が観測されること、その振舞がG-アクチンとF-アクチンで異なること、そしてG-アクチンの方がF-アクチンより"柔らかい"ことが示された。さらに、アクチンは、G-アクチンとF-アクチンで同様の柔らかさを持つ領域と、G-アクチンにおいてより柔らかくなる領域という動的不均一性を持っていることが示唆された。
松本 富美子; 前田 佳代*; 似内 靖*; 小田 俊郎*; 前田 雄一郎*; 藤原 悟
no journal, ,
遺伝性心筋症(HMC)は心臓の収縮機能やカルシウム調節に異常をきたす疾患で、筋収縮調節を担う蛋白質であるトロポニン(Tn;TnT, TnI, TnCからなる複合体)の変異により生じることが報告されている。われわれはTnの変異により生じるHMCの発症原因を探るため、Tn結晶構造中でIT-armと呼ばれるコイルドコイル中に存在する2つの変異(TnT(E244D), TnT(K247R))に注目して研究を行った。これまで、TnT(E244D)変異は心筋のカルシウム感受性を変えることなく最大張力を増大させるという報告があるが、TnT(K247R)についての報告はまだない。われわれは、これらの部位に種々の変異を導入し(E244; D, M, A, K and K247; R, E, A)、それにより生じる筋原繊維の機能異常を系統的に調べた。その結果、われわれは、IT-arm中に存在する2つの心筋症型変異が、同様の機能異常を引き起こすことを明らかにした。さらにこれらの部位が、IT-armの柔軟性を決定付けさせるような非常に特徴的なアミノ酸ネットワークを形成していることを見いだした。発表では変異により生じると考えられるIT-armの柔軟性変化と機能異常との関連について述べ、HMCの原因について考察する。
藤原 悟; 小田 俊郎*; Plazanet, M.*; 松本 富美子
no journal, ,
アクチンは、ほぼすべての真核細胞内に存在し、細胞運動や輸送等にかかわる実に多様な機能を持つ。アクチン単量体(G-アクチン)は重合して繊維状重合体(F-アクチン)を形成するが、多様なアクチンの機能は、種々の蛋白質との相互作用を可能とするF-アクチンの柔らかさのゆえである。F-アクチンの柔らかさの起源を明らかにするための第一段階として、われわれはピコ領域におけるアクチンの運動特性の測定を、中性子非干渉性弾性散乱(EINS)及び準弾性散乱(QENS)法を用いて行った。EINS測定により見積もられたアクチン分子内の原子の平均自乗変位の温度に依存した振舞がG-アクチンとF-アクチンで異なることが示された。また、QENSスペクトルから、アクチン分子内の原子の運動は、制限された空間内における拡散的運動として記述できること、並びにスペクトルがG-アクチンとF-アクチンで異なることが明らかとなった。これらのスペクトルの解析の結果、アクチンは、G-アクチンとF-アクチンで同様の柔らかさを持つ領域と、G-アクチンにおいてより柔らかくなる領域という動的不均一性を持っていることが示唆された。
藤原 悟; Plazanet, M.*; 松本 富美子; 小田 俊郎*
no journal, ,
アクチンは、真核細胞に最も豊富に存在する蛋白質で、細胞運動や輸送等にかかわる実に多様な機能を持つ。アクチン単量体(G-アクチン)は重合して繊維状重合体(F-アクチン)を形成するが、多様なアクチンの機能は、種々の蛋白質との相互作用を可能とするF-アクチンの柔らかさに由来する。F-アクチンの柔らかさはアクチンの運動特性による。われわれはF-アクチンの柔らかさを理解するための第一段階として、アクチンの運動特性を、中性子非干渉性弾性散乱(EINS)及び準弾性散乱(QENS)法により測定した。EINS測定により見積もられたアクチン分子内の原子の平均自乗変位の温度に依存した振舞がG-アクチンとF-アクチンで異なることが示された。また、QENSスペクトルから、アクチン分子内の原子の運動は、制限された空間内における拡散運動と局所的なジャンプ運動の組合せとして記述できること、及びG-アクチンとF-アクチンの振舞が異なることが示された。これらの違いがアクチン分子内の動的不均一性によることが示唆された。
藤原 悟; 小田 俊郎*; Plazanet, M.*; 松本 富美子
no journal, ,
F-アクチンは、真核細胞に最も豊富に存在し、細胞運動に関係する実に多様な機能を持つ。どのようにして、このような多様な機能が可能となるかを理解するためには、アクチン分子の内部運動から分子間の相対的運動、そしてF-アクチン全体の運動までのさまざまなレベルでの運動特性を明らかにすることが重要である。われわれは、そのためにF-アクチン及びアクチン単量体(G-アクチン)の中性子非干渉性弾性散乱実験を行い、F-アクチン及びG-アクチンの運動特性の違いを明らかにした。さらにアクチン分子内部の運動特性を詳しく特徴付けるため、中性子準弾性散乱実験を行った。第1水和層まで含む水和粉末試料及び「バルク」水まで含む試料についての測定を行った結果、F-アクチン及びG-アクチンのいずれも、少なくとも2種類の異なった振幅と速度を持つ運動が存在すること、そして含水量の増大は、これらの動きを速くさせること、そしてG-アクチンはF-アクチンよりも、より大きな振幅及び速い速度の運動を示す傾向があることを明らかにした。
藤原 悟; Plazanet, M.*; 松本 富美子; 小田 俊郎*
no journal, ,
F-アクチンは、アクチン単量体(G-アクチン)の繊維状重合体であり、細胞運動に関係する実に多様な機能を持つ。どのようにして、このような多様な機能が可能となるかを理解するためには、アクチン分子の内部運動から分子間の相対的運動、そしてF-アクチン全体の運動までのさまざまなレベルでの運動特性を明らかにすることが重要である。われわれは、そのためにF-アクチン及びG-アクチンの中性子非干渉性弾性散乱実験を行い、F-アクチン及びG-アクチンの運動特性の違いを明らかにした。さらにアクチン分子内部の運動特性を詳しく特徴付けるため、中性子準弾性散乱実験を行った。第1水和層まで含む水和粉末試料及び「バルク」水まで含む試料についての測定を行った結果、F-アクチン及びG-アクチンのいずれも、少なくとも2種類の異なった振幅と速度を持つ運動が存在すること、そして含水量の増大は、これらの動きを速くさせること、そしてG-アクチンはF-アクチンよりも、より大きな振幅及び速い速度の運動を示す傾向があることを明らかにした。
藤原 悟; 松本 富美子; 中川 洋; 遠藤 仁*; 小田 俊郎*
no journal, ,
F-アクチンの細胞運動や輸送等にかかわる実に多様な機能を可能とするF-アクチンの柔らかさの起源を解明し、機能多様性の分子機構を明らかにするための第一段階として、さまざまな時空間階層における運動モードのうち、ピコ ナノ秒領域におけるアクチンのダイナミクスの測定を行った。東京大学物性研究所所有の中性子スピンエコー分光器(iNSE)を用いて、時間領域30ナノ秒までのQ-領域0.03
ナノ秒領域におけるアクチンのダイナミクスの測定を行った。東京大学物性研究所所有の中性子スピンエコー分光器(iNSE)を用いて、時間領域30ナノ秒までのQ-領域0.03 0.2
0.2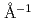 の中性子スピンエコー測定を、F-アクチン溶液及びその対照としての単量体G-アクチン溶液のそれぞれについて行った。この時空間領域は、蛋白質の並進拡散や蛋白質内ドメインの運動などの起こる領域に対応し、中性子スピンエコー法によってのみ測定可能な時空領域である。得られた中間関数から、F-アクチン及びG-アクチンのいずれも単一の緩和過程で記述できることが示された。そして、緩和の早さ、すなわち(みかけの)拡散係数がF-アクチンの方が小さくなることが明らかとなった。G-アクチン及びF-アクチンのいずれも、単純な溶液中の自由併進拡散のみでなく、内部運動が影響していることが示唆された。
の中性子スピンエコー測定を、F-アクチン溶液及びその対照としての単量体G-アクチン溶液のそれぞれについて行った。この時空間領域は、蛋白質の並進拡散や蛋白質内ドメインの運動などの起こる領域に対応し、中性子スピンエコー法によってのみ測定可能な時空領域である。得られた中間関数から、F-アクチン及びG-アクチンのいずれも単一の緩和過程で記述できることが示された。そして、緩和の早さ、すなわち(みかけの)拡散係数がF-アクチンの方が小さくなることが明らかとなった。G-アクチン及びF-アクチンのいずれも、単純な溶液中の自由併進拡散のみでなく、内部運動が影響していることが示唆された。