Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
冨田 雅典*; 松本 英樹*; 舟山 知夫; 横田 裕一郎; 大塚 健介*; 前田 宗利*; 小林 泰彦
Life Sciences in Space Research, 6, p.36 - 43, 2015/07
放射線誘発バイスタンダー効果は、放射線で直接照射された細胞から放出された細胞間シグナルが、周辺の非照射細胞に放射線応答を誘導する現象である。とりわけ、低フルエンス重イオンが誘導するバイスタンダー効果は、宇宙環境における宇宙飛行士の放射線リスクに直結する重要な問題である。そこで、原子力機構・高崎量子応用研究所のマイクロビーム細胞照射装置を用いた重イオン照射でバイスタンダー効果を誘導し、そのシグナル経路の解析を行った。研究の結果、COX-2遺伝子が含まれる、AktおよびNF-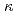 B依存シグナル伝達経路が、一酸化窒素ラジカルが関与する重イオン誘発バイスタンダー応答の誘導に重要であることが示された。加えて、COX-2タンパク質が重イオン誘発バイスタンダー応答におけるバイスタンダー細胞の分子マーカーとして利用できる可能性も示した。
B依存シグナル伝達経路が、一酸化窒素ラジカルが関与する重イオン誘発バイスタンダー応答の誘導に重要であることが示された。加えて、COX-2タンパク質が重イオン誘発バイスタンダー応答におけるバイスタンダー細胞の分子マーカーとして利用できる可能性も示した。
松本 英樹*; 冨田 雅典*; 大塚 健介*; 畑下 昌範*; 前田 宗利*; 舟山 知夫; 横田 裕一郎; 鈴木 芳代; 坂下 哲哉; 池田 裕子; et al.
JAEA-Review 2014-050, JAEA Takasaki Annual Report 2013, P. 76, 2015/03
低線量/低線量率放射線に対して生物が示す特異的な応答様式には、放射線適応応答、放射線誘発バイスタンダー応答、放射線超高感受性、遺伝的不安定性等がある。我々は、原子力機構において開発された細胞局部照射装置(HZ1)および深度制御種子照射装置(HY1)を用いて、放射線誘発バイスタンダー応答による放射線適応応答の誘導機構の解析を実施した。中央にスポットしたコロニーの細胞に520MeV 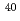 Ar
Ar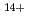 をマイクロビーム照射し、4-6時間培養後に同
をマイクロビーム照射し、4-6時間培養後に同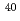 Ar
Ar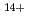 をブロードビーム照射した結果、放射線適応応答の誘導が認められ、この誘導はNO特異的な捕捉剤であるcarboxy-PTIOの添加でほぼ完全に抑制された。このマイクロビーム照射による放射線適応応答の誘導が起きた細胞で、
をブロードビーム照射した結果、放射線適応応答の誘導が認められ、この誘導はNO特異的な捕捉剤であるcarboxy-PTIOの添加でほぼ完全に抑制された。このマイクロビーム照射による放射線適応応答の誘導が起きた細胞で、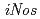 遺伝子の発現が特異的に発現誘導されていることが見いだされ、放射線適応応答の誘導にNOを介したバイスタンダー効果の誘導が関与していることが強く示唆された。
遺伝子の発現が特異的に発現誘導されていることが見いだされ、放射線適応応答の誘導にNOを介したバイスタンダー効果の誘導が関与していることが強く示唆された。
冨田 雅典*; 松本 英樹*; 大塚 健介*; 舟山 知夫; 横田 裕一郎; 鈴木 芳代; 坂下 哲哉; 小林 泰彦
JAEA-Review 2014-050, JAEA Takasaki Annual Report 2013, P. 77, 2015/03
低粒子数の重イオン線による生物影響を解明する上で、DNA初期損傷量に依存しない「非標的効果」が注目されている。特に、放射線に直接曝露された細胞の近傍に存在する全く放射線に曝露されていない細胞において観察される「放射線誘発バイスタンダー応答」は、最も特徴的な非標的効果であり、その解明は放射線生物学のみならず、粒子線がん治療、宇宙放射線の生体影響評価においても重要である。本研究は、これまでの2次元での培養細胞を用いた研究から、組織レベルでの生体応答研究への展開を図るため、分化誘導させたヒト3次元培養皮膚モデルを用い、原子力機構の細胞局部照射装置を利用し、放射線誘発バイスタンダー応答によって生じるシグナル伝達経路の変化を明らかにすることを目的とした。2015年度は、ヒト3次元培養皮膚モデルへの重イオンマイクロビーム照射条件の検討を行い、照射した試料のMTT法による生細胞率測定を実施し、試料全体を重イオンビームで照射したものと比較した。その結果、全体照射した試料では生存率の低下が認められた一方、本条件でマイクロビーム照射した試料では生存率の低下が認められなかった。
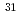 Ne
Ne中村 隆司*; 小林 信之*; 近藤 洋介*; 佐藤 義輝*; 青井 考*; 馬場 秀忠*; 出口 茂樹*; 福田 直樹*; Gibelin, J.*; 稲辺 尚人*; et al.
Physical Review Letters, 103(26), p.262501_1 - 262501_4, 2009/12
被引用回数:198 パーセンタイル:97.53(Physics, Multidisciplinary)理化学研究所のRIBFにて中性子過剰核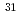 Neの1中性子分離反応の断面積を測定した。鉛ターゲットと炭素ターゲットの断面積を比較することにより、
Neの1中性子分離反応の断面積を測定した。鉛ターゲットと炭素ターゲットの断面積を比較することにより、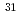 Neのクーロン分解反応断面積が540(70)mbと導出された。その断面積は通常の原子核の断面積と比べ非常に大きく、中性子が非常に弱く束縛されているハロー構造を示唆している。この原子核のクーロン分解断面積を直接ブレークアップ模型と殻模型で求めた波動関数の重なり(分光学的因子)を組合せることにより定量的に計算した結果、
Neのクーロン分解反応断面積が540(70)mbと導出された。その断面積は通常の原子核の断面積と比べ非常に大きく、中性子が非常に弱く束縛されているハロー構造を示唆している。この原子核のクーロン分解断面積を直接ブレークアップ模型と殻模型で求めた波動関数の重なり(分光学的因子)を組合せることにより定量的に計算した結果、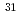 Ne核の最後の1個の中性子は、普通の軌道の順序である
Ne核の最後の1個の中性子は、普通の軌道の順序である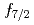 ではなく
ではなく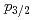 軌道を主に占め、
軌道を主に占め、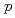 軌道の小さな軌道角運動量により一粒子ハローを形成していることが明らかとなった。
軌道の小さな軌道角運動量により一粒子ハローを形成していることが明らかとなった。
松本 英樹*; 冨田 雅典*; 大塚 健介*; 舟山 知夫; 小林 泰彦
no journal, ,
The radioadaptive response, radiation-induced bystander responses, low-dose radio-hypersensitivity, and genomic instability are specifically observed in response to low dose/low dose-rate radiation, and the mechanisms underlying these responses often involve biochemical/molecular signals that respond to targeted and non-targeted events. However, mechanisms of these phenomena are not fully known. To elucidate the mechanisms of radiation-induced bystander responses, we analyzed the formation of  H2AX and pNBS1 foci after irradiation of a targeted cell with 460 MeV
H2AX and pNBS1 foci after irradiation of a targeted cell with 460 MeV 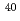 Ar microbeams. We found that the foci of
Ar microbeams. We found that the foci of  H2AX and pNBS1 were formed in the unirradiated cells in the colony including the targeted cell 6 h after the irradiation and that this formation of these foci was almost completely suppressed by the addition of DMSO or Lindane. Also we found that the foci of
H2AX and pNBS1 were formed in the unirradiated cells in the colony including the targeted cell 6 h after the irradiation and that this formation of these foci was almost completely suppressed by the addition of DMSO or Lindane. Also we found that the foci of  H2AX and pNBS1 were formed in the unirradiated cells in the colonies not including the targeted cell 6 h after irradiation and that this formation of the foci was almost completely suppressed by the addition of aminoguanidine or c-PTIO. Our findings strongly suggested that ROS and NO may be actually initiators/mediators for evoking radiation-induced bystander responses.
H2AX and pNBS1 were formed in the unirradiated cells in the colonies not including the targeted cell 6 h after irradiation and that this formation of the foci was almost completely suppressed by the addition of aminoguanidine or c-PTIO. Our findings strongly suggested that ROS and NO may be actually initiators/mediators for evoking radiation-induced bystander responses.