Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
石田 毅; 中島 伸一; 近藤 伸次; 林原 健一; 山田 茂樹*; 岡本 諒*; 中村 仁宣
第44回日本核物質管理学会年次大会会議論文集(インターネット), 4 Pages, 2023/11
日本原子力研究開発機構人形峠環境技術センター(以下、「人形峠センター」という。)では、国内初の遠心分離法によるウラン濃縮技術の実用化のため、1979年よりウラン濃縮パイロットプラントの試験運転を開始後2001年の運転終了に至るまでの間、ウラン濃縮技術に係る研究開発活動が実施されてきた。現在は濃縮施設の廃止措置に係る技術開発を実施している。ウラン濃縮技術は、核不拡散の観点において、その情報を厳格に管理する必要がある。人形峠センターは研究開発活動を実施するにあたって、核不拡散対応を含む保障措置上の様々な課題解決に取り組んできた。本論文では主な課題に対する取り組みについて紹介する。
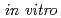 evaluation of F(
evaluation of F( -
- I)KCCYSL for targeting HER2
I)KCCYSL for targeting HER2佐々木 一郎; 渡辺 茂樹; 大島 康宏; 須郷 由美; 山田 圭一*; 花岡 宏史*; 石岡 典子
Peptide Science 2015, p.243 - 246, 2016/03
Radioisotope labeled peptides with high affinity to receptors overexpressing on the surface of tumor cells are promising for applications in nuclear medicine such as diagnostic radiography and radiotherapy. Radiohalogens such as  I and
I and 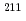 At are useful for clinical imaging and therapeutic applications, and it can be introduced at the
At are useful for clinical imaging and therapeutic applications, and it can be introduced at the 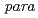 position of phenylalanine residue via electrophilic destannylation. KCCYSL (Lys
position of phenylalanine residue via electrophilic destannylation. KCCYSL (Lys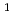 -Cys
-Cys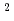 -Cys
-Cys -Tyr
-Tyr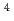 -Ser
-Ser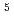 -Leu
-Leu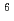 ) is a hexapeptide containing disulfide bond. Previous study revealed that KCCYSL has potential as tumor imaging and therapeutic agent targeting tumor cells overexpressing the human epidermal growth factor receptor type 2 (HER2). In this study, we report synthesis and
) is a hexapeptide containing disulfide bond. Previous study revealed that KCCYSL has potential as tumor imaging and therapeutic agent targeting tumor cells overexpressing the human epidermal growth factor receptor type 2 (HER2). In this study, we report synthesis and 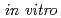 evaluation of radiohalogenated KCCYSL derivatives. Precursor peptides, Boc-F(
evaluation of radiohalogenated KCCYSL derivatives. Precursor peptides, Boc-F( -SnBu
-SnBu )K(Boc)C(Trt)C(Trt)Y(
)K(Boc)C(Trt)C(Trt)Y(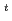 Bu)S(
Bu)S(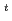 Bu)L-OH and Boc-F(
Bu)L-OH and Boc-F( -SnBu
-SnBu )GS(
)GS(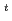 Bu)GK(Boc)C(Trt)C(Trt)Y(
Bu)GK(Boc)C(Trt)C(Trt)Y(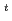 Bu)S(
Bu)S(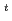 Bu)L-OH, were synthesized by the Fmoc solid phase peptide synthesis. Then, precursor peptides were radioiodinated via electrophilic destannylation, and they were deprotected to obtain F(
Bu)L-OH, were synthesized by the Fmoc solid phase peptide synthesis. Then, precursor peptides were radioiodinated via electrophilic destannylation, and they were deprotected to obtain F( -
- I)KCCYSL and F(
I)KCCYSL and F( -
- I)GSGKCCYSL in radiochemical yield 15% and 17%, respectively.
I)GSGKCCYSL in radiochemical yield 15% and 17%, respectively. 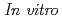 assays of the radioiodinated peptides for HER2 and stability in serum are being undertaken.
assays of the radioiodinated peptides for HER2 and stability in serum are being undertaken.
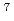 Li +
Li + 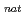 Pb reaction
Pb reaction西中 一朗; 横山 明彦*; 鷲山 幸信*; 前田 英太*; 渡辺 茂樹; 橋本 和幸; 石岡 典子; 牧井 宏之; 豊嶋 厚史; 山田 記大*; et al.
Journal of Radioanalytical and Nuclear Chemistry, 304(3), p.1077 - 1083, 2015/06
被引用回数:9 パーセンタイル:60.64(Chemistry, Analytical)29-57MeVの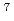 Liビームと
Liビームと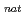 Pb標的核の反応においてアスタチン同位体
Pb標的核の反応においてアスタチン同位体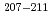 Atの生成断面積を
Atの生成断面積を 線,
線,  線スペクトルメトリーで測定した。生成断面積の励起関数を統計模型モデル計算と比較することで、
線スペクトルメトリーで測定した。生成断面積の励起関数を統計模型モデル計算と比較することで、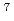 Li +
Li + 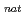 Pbの反応機構を調べた。44MeVより大きい入射エネルギーでの
Pbの反応機構を調べた。44MeVより大きい入射エネルギーでの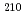 Atと
Atと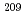 Atの生成断面積が理論値よりも小さいことから、分解反応が存在することを明らかにした。照射した鉛標的からのアスタチンの化学分離を乾式蒸留法に基づいて調べ、アスタチン製造の相補的な手法を開発した。
Atの生成断面積が理論値よりも小さいことから、分解反応が存在することを明らかにした。照射した鉛標的からのアスタチンの化学分離を乾式蒸留法に基づいて調べ、アスタチン製造の相補的な手法を開発した。
 -lactamase from the moderate halophile
-lactamase from the moderate halophile 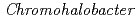 sp.560 and the discovery of a Cs
sp.560 and the discovery of a Cs -selective binding site
-selective binding site新井 栄揮; 米澤 悌*; 岡崎 伸生*; 松本 富美子*; 柴崎 千枝; 清水 瑠美; 山田 貢*; 安達 基泰; 玉田 太郎; 河本 正秀*; et al.
Acta Crystallographica Section D, 71(3), p.541 - 554, 2015/03
被引用回数:7 パーセンタイル:50.76(Biochemical Research Methods)蛋白質を利用した希少・有害金属捕集材料の研究開発の一環として、中度好塩菌Chromohalobacter sp.560由来・高酸性 -Lactamase(HaBLA)のX線結晶構造を解明するとともに、X線異常分散測定により、HaBLA分子上のCs
-Lactamase(HaBLA)のX線結晶構造を解明するとともに、X線異常分散測定により、HaBLA分子上のCs , Sr
, Sr 結合部位の抽出を試みた。PFのNW3AにてHaBLAのX線結晶構造を解明した後、Cs吸収端(
結合部位の抽出を試みた。PFのNW3AにてHaBLAのX線結晶構造を解明した後、Cs吸収端(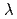 =2.175
=2.175 )近傍のX線を利用できるSAGA-LSのBL7やPFのBL17A、及び、Sr吸収端(
)近傍のX線を利用できるSAGA-LSのBL7やPFのBL17A、及び、Sr吸収端(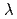 =0.770
=0.770 )近傍のX線を利用できるSPring-8のBL38B1やPFのBL5Aなどを使用して、HaBLA分子に結合したCs
)近傍のX線を利用できるSPring-8のBL38B1やPFのBL5Aなどを使用して、HaBLA分子に結合したCs 及びSr
及びSr を同定した。その結果、HaBLA分子上に少なくとも1ヶ所のCs
を同定した。その結果、HaBLA分子上に少なくとも1ヶ所のCs 結合部位、3ヶ所のSr
結合部位、3ヶ所のSr 結合部位を発見した。特に、今回発見したCs
結合部位を発見した。特に、今回発見したCs 結合部位は、Na
結合部位は、Na がCs
がCs の9倍量存在する条件下(Na
の9倍量存在する条件下(Na /Cs
/Cs = 90mM/10mM)でもCs
= 90mM/10mM)でもCs を選択的に結合できることが明らかになった。このCs
を選択的に結合できることが明らかになった。このCs 選択的結合部位は、Trp側鎖のベンゼン環によるカチオン-
選択的結合部位は、Trp側鎖のベンゼン環によるカチオン-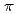 相互作用、および、主鎖の2つの酸素原子によってCs
相互作用、および、主鎖の2つの酸素原子によってCs を結合していた。本研究で得たCs
を結合していた。本研究で得たCs 結合部位の立体構造情報は、原発事故によって放出された放射性Cs
結合部位の立体構造情報は、原発事故によって放出された放射性Cs を捕集する蛋白質材料の設計(人工的Cs
を捕集する蛋白質材料の設計(人工的Cs 結合部位の設計)の土台として利用できる。
結合部位の設計)の土台として利用できる。
佐々木 一郎; 花岡 宏史*; 山田 圭一*; 渡辺 茂樹; 須郷 由美; 大島 康宏; 鈴木 博元; 石岡 典子
Peptide Science 2014, p.257 - 260, 2015/03
We have sought to establish drug discovery system using radioisotope (RI) labeled peptides which have high affinity to target proteins overexpressed in cancers. Of the target proteins, we chose the human epidermal growth factor receptor type 2 (HER2), a membrane protein overexpressed in various cancers to evaluate the drug discovery system. Three series of random hexapeptide libraries introduced a radioiodinated D-tyrosine (y(3- I)) to
I)) to 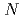 -terminal were designed and binding assay with HER2-expressed cell lines were conducted in this study. First, we synthesized a series of random hexapeptide libraries with fixed amino acid sequence at 1 and 2 positions, y(3-
-terminal were designed and binding assay with HER2-expressed cell lines were conducted in this study. First, we synthesized a series of random hexapeptide libraries with fixed amino acid sequence at 1 and 2 positions, y(3- I)X
I)X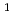 X
X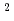 X
X X
X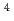 X
X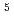 X
X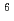 . Non-radioactive random peptide libraries, yXXXXXX, were prepared by Fmoc-SPPS with an automatic peptide synthesizer. Radioiodinated y(3-
. Non-radioactive random peptide libraries, yXXXXXX, were prepared by Fmoc-SPPS with an automatic peptide synthesizer. Radioiodinated y(3- I)XXXXXX were subsequently synthesized in 30-50% radiochemical yield. Binding assay using HER2-overexpressed cell line showed that high affinity (38-50% dose, n=6) was obtained with yIIXXXX, while other random peptide libraries were yielded low affinity (approximately 1% dose), which indicated that the system using RI labeled random peptide libraries have potential to discover peptide drug for cancer therapy. Preparation of other random hexapeptide libraries are being undertaken.
I)XXXXXX were subsequently synthesized in 30-50% radiochemical yield. Binding assay using HER2-overexpressed cell line showed that high affinity (38-50% dose, n=6) was obtained with yIIXXXX, while other random peptide libraries were yielded low affinity (approximately 1% dose), which indicated that the system using RI labeled random peptide libraries have potential to discover peptide drug for cancer therapy. Preparation of other random hexapeptide libraries are being undertaken.
佐々木 一郎; 山田 圭一*; 渡辺 茂樹; 花岡 宏史*; 須郷 由美; 奥 浩之*; 石岡 典子
JAEA-Review 2013-059, JAEA Takasaki Annual Report 2012, P. 96, 2014/03
Radioisotope (RI)-labeled peptide with high affinity to receptors overexpressing on the surface of tumor cells are promising for applications in nuclear medicine such as diagnostic radiography and radiotherapy. MARSGL (H-Met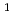 -Ala
-Ala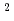 -Arg
-Arg -Ser
-Ser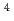 -Gly
-Gly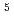 -Leu
-Leu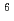 -OH), a linear peptide consisting of six amino acids, has high affinity to HER2/neu receptor overexpressing in various cancer cells. Radiohalogens (radionuclides) such as radioiodine and radiobromine are versatile for clinical imaging and therapeutic applications. Thus, radiohalogenated MARSGL may have potential for clinical applications to HER2 overexpressing tumors. In this study, in order to achieve the labeling of radiohalogen for MARSGL, we design a radioiodinated peptide, F(
-OH), a linear peptide consisting of six amino acids, has high affinity to HER2/neu receptor overexpressing in various cancer cells. Radiohalogens (radionuclides) such as radioiodine and radiobromine are versatile for clinical imaging and therapeutic applications. Thus, radiohalogenated MARSGL may have potential for clinical applications to HER2 overexpressing tumors. In this study, in order to achieve the labeling of radiohalogen for MARSGL, we design a radioiodinated peptide, F( -
- I)MARSGL, in which phenylalanine labeled with
I)MARSGL, in which phenylalanine labeled with  I (t
I (t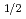 = 8.0 d) at the
= 8.0 d) at the 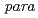 position of the aromatic ring is introduced into the N-terminal of MARSGL and report a new technique to prepare radiohalogen of peptide via electrophilic destanylation.
position of the aromatic ring is introduced into the N-terminal of MARSGL and report a new technique to prepare radiohalogen of peptide via electrophilic destanylation.
佐々木 一郎; 山田 圭一*; 渡邉 茂樹; 花岡 宏史*; 須郷 由美; 奥 浩之*; 石岡 典子
Peptide Science 2013, p.157 - 160, 2013/03
Radioisotope (RI)-labeled peptides which have the high affinity to receptors on surface of the tumor cell are promising for diagnostic radiography (PET and SPECT) and radiotherapy. MARSGL (H-Met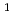 -Ala
-Ala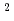 -Arg
-Arg -Ser
-Ser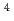 -Gly
-Gly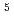 -Leu
-Leu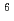 -OH), a linear hexapeptide consisting of six amino acids, has the high affinity to HER2/neu receptor overexpressing in various cancer cells. Thus, radiolabeled MARSGL has potential for the above mentioned purposes. Radiohalogens have various useful radionuclides, which could be introduced to aromatic compounds via tin-halogen exchange reaction. In this study, stannylated peptide Boc-F(
-OH), a linear hexapeptide consisting of six amino acids, has the high affinity to HER2/neu receptor overexpressing in various cancer cells. Thus, radiolabeled MARSGL has potential for the above mentioned purposes. Radiohalogens have various useful radionuclides, which could be introduced to aromatic compounds via tin-halogen exchange reaction. In this study, stannylated peptide Boc-F( -SnBu
-SnBu )MAR(Pbf)S(
)MAR(Pbf)S(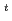 Bu)GL-OH was synthesized to prepare radiohalogen (
Bu)GL-OH was synthesized to prepare radiohalogen ( Br or
Br or  I)-labeled FMARSGL derivatives. First, Boc-Phe(
I)-labeled FMARSGL derivatives. First, Boc-Phe( -SnBu
-SnBu )-OH was prepared from Boc-Phe(
)-OH was prepared from Boc-Phe( -I)-OMe via Pd(0)-catalyzed coupling reaction with (Bu
-I)-OMe via Pd(0)-catalyzed coupling reaction with (Bu Sn)
Sn) and was successfully introduced into
and was successfully introduced into 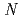 -terminal of H-MARSGL-Trt(2-Cl) resin synthesized from H-Leu-Trt(2-Cl) resin by Fmoc-SPPS. After cleavage reaction of Boc-F(
-terminal of H-MARSGL-Trt(2-Cl) resin synthesized from H-Leu-Trt(2-Cl) resin by Fmoc-SPPS. After cleavage reaction of Boc-F( -SnBu
-SnBu )MAR(Pbf)S(
)MAR(Pbf)S(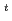 Bu)GL-Trt(2-Cl) resin with 25% 1,1,1,3,3,3-hexafluoro-2-propanol in CH
Bu)GL-Trt(2-Cl) resin with 25% 1,1,1,3,3,3-hexafluoro-2-propanol in CH Cl
Cl , Boc-F(
, Boc-F( -SnBu
-SnBu )MAR(Pbf)S(
)MAR(Pbf)S(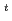 Bu)GL-OH was obtained and identified by using ESI-MS and NMR. Synthesis of
Bu)GL-OH was obtained and identified by using ESI-MS and NMR. Synthesis of  I-labeled FMARSGL is due to report in this presentation.
I-labeled FMARSGL is due to report in this presentation.
 I]-sansalvamide A derivative
I]-sansalvamide A derivative渡邉 茂樹; 山田 圭一*; 津久井 匠隆*; 花岡 宏史*; 大島 康宏; 山口 藍子*; 奥 浩之*; 石岡 典子
JAEA-Review 2012-046, JAEA Takasaki Annual Report 2011, P. 88, 2013/01
Sansalvamide A (SA), a penta cyclic peptide isolated marine fungus, is a lead compound of anti-cancer reagent because the peptide has cytotoxicity against various cancer cell lines. Halogenated SA derivatives (SA-X, X = Cl, Br, I) was prepared and remarkable cytotocity against malignant human breast cancer. In this study, a radiohalogenated SA derivative [ I]SA-I was prepared to conduct in vivo evaluation of SA derivatives. Synthetic scheme of [
I]SA-I was prepared to conduct in vivo evaluation of SA derivatives. Synthetic scheme of [ I]SA-I are as follows: an iodinated linear peptide, Boc-F(p-I)LLVL-OMe, was prepared by the conventional solid phase peptide synthesis. After preparation of stannylated peptide, Boc-F(p-SnBu
I]SA-I are as follows: an iodinated linear peptide, Boc-F(p-I)LLVL-OMe, was prepared by the conventional solid phase peptide synthesis. After preparation of stannylated peptide, Boc-F(p-SnBu )LLVL-OMe,
)LLVL-OMe,  I was labeled with electrophilic destannylation in the presence of oxidizing reagent. After deprotection of N- and C-termius, [
I was labeled with electrophilic destannylation in the presence of oxidizing reagent. After deprotection of N- and C-termius, [ I]SA-I was obtained successfully by macrocyclization in liquid phase. Overall labeled yield was 7%. To our best knowledge, this report is the first on the synthesis of radiolabeled SA derivative. In vivo evaluation of the SA derivative using [
I]SA-I was obtained successfully by macrocyclization in liquid phase. Overall labeled yield was 7%. To our best knowledge, this report is the first on the synthesis of radiolabeled SA derivative. In vivo evaluation of the SA derivative using [ I]SA-I is being undertaken.
I]SA-I is being undertaken.
 Br-labeled amino acid derivative for PET imaging of tumor
Br-labeled amino acid derivative for PET imaging of tumor花岡 宏史*; 渡邉 茂樹; 富永 英之*; 大島 康宏; 渡辺 智; 山田 圭一*; 飯田 靖彦*; 石岡 典子; 遠藤 啓吾*
JAEA-Review 2012-046, JAEA Takasaki Annual Report 2011, P. 89, 2013/01
近年、がんに対する特異性が高いPET薬剤として、 Cや
Cや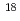 Fで標識したアミノ酸誘導体が開発され、臨床応用されるようになってきた。しかしながら
Fで標識したアミノ酸誘導体が開発され、臨床応用されるようになってきた。しかしながら Cや
Cや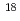 Fは半減期が非常に短いため、それぞれの病院で製造・合成する必要があり、限られた施設でしか使えないのが現状である。一方、
Fは半減期が非常に短いため、それぞれの病院で製造・合成する必要があり、限られた施設でしか使えないのが現状である。一方、 Brは、半減期が16.1時間とポジトロン放出核種としては比較的長く、またハロゲン核種であるため母体化合物との結合にキレート剤等が必要ないことから、アミノ酸のような低分子化合物に対しても応用可能である。そこで本研究では、広く臨床使用することが可能な、新規がん診断用PETイメージング薬剤として
Brは、半減期が16.1時間とポジトロン放出核種としては比較的長く、またハロゲン核種であるため母体化合物との結合にキレート剤等が必要ないことから、アミノ酸のような低分子化合物に対しても応用可能である。そこで本研究では、広く臨床使用することが可能な、新規がん診断用PETイメージング薬剤として Br標識アミノ酸誘導体の開発を計画した。基礎検討には半減期が長い放射性臭素である
Br標識アミノ酸誘導体の開発を計画した。基礎検討には半減期が長い放射性臭素である Br(半減期57時間)を用いて行うこととした。Br標識アミノ酸としては、
Br(半減期57時間)を用いて行うこととした。Br標識アミノ酸としては、 メチルフェニルアラニン(
メチルフェニルアラニン( -Me-Phe)のパラ位にBrを導入したBr-
-Me-Phe)のパラ位にBrを導入したBr- -Me-Pheを設計した。
-Me-Pheを設計した。 Br-
Br- -Me-Pheは標識率25-40%で合成することができた。
-Me-Pheは標識率25-40%で合成することができた。 Br-
Br- -Me-Pheを担癌マウスに投与したところ、腫瘍への高い集積性を示し、投与3時間後の腫瘍対血液比は3.94、腫瘍対筋肉比は3.95であった。
-Me-Pheを担癌マウスに投与したところ、腫瘍への高い集積性を示し、投与3時間後の腫瘍対血液比は3.94、腫瘍対筋肉比は3.95であった。 Br-
Br- -Me-Pheを担癌マウスに投与してPET撮像を行ったところ、腫瘍を明瞭に描出することができた。以上の結果から、
-Me-Pheを担癌マウスに投与してPET撮像を行ったところ、腫瘍を明瞭に描出することができた。以上の結果から、 Br-
Br- -Me-Pheの新規がんイメージング薬剤としての有用性が示唆された。
-Me-Pheの新規がんイメージング薬剤としての有用性が示唆された。
 Cu-labeled DOTA-
Cu-labeled DOTA-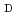 -Phe
-Phe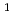 -Tyr
-Tyr -octreotide (
-octreotide ( Cu-DOTA-TOC) for imaging somatostatin receptor-expressing tumors
Cu-DOTA-TOC) for imaging somatostatin receptor-expressing tumors花岡 宏史*; 富永 英之*; 山田 圭一*; Paudyal, P.*; 飯田 靖彦*; 渡邉 茂樹; Paudyal, B.*; 樋口 徹也*; 織内 昇*; 遠藤 啓吾*
Annals of Nuclear Medicine, 23(6), p.559 - 567, 2009/08
被引用回数:17 パーセンタイル:46.65(Radiology, Nuclear Medicine & Medical Imaging)In-111 (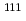 In)-labeled octreotide has been clinically used for imaging somatostatin receptor-positive tumors, and radiolabeled octreotide analogs for positron emission tomography (PET) have been developed. The aim of this study is to produce and fundamentally examine a
In)-labeled octreotide has been clinically used for imaging somatostatin receptor-positive tumors, and radiolabeled octreotide analogs for positron emission tomography (PET) have been developed. The aim of this study is to produce and fundamentally examine a  Cu-labeled octreotide analog,
Cu-labeled octreotide analog,  Cu-1,4,7,10-tetraazacyclododecane-1,4,7,10-tetraacetic acid-
Cu-1,4,7,10-tetraazacyclododecane-1,4,7,10-tetraacetic acid-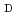 -Phe
-Phe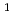 -Tyr
-Tyr -octreotide (
-octreotide ( Cu-DOTA-TOC).
Cu-DOTA-TOC).  Cu-DOTA-TOC can be produced in amounts efficient for clinical study with high radiochemical yield.
Cu-DOTA-TOC can be produced in amounts efficient for clinical study with high radiochemical yield.  Cu-DOTA-TOC was stable in vitro, but time-dependent transchelation to protein was observed after injection into mice. In biodistribution studies, the radioactivity of
Cu-DOTA-TOC was stable in vitro, but time-dependent transchelation to protein was observed after injection into mice. In biodistribution studies, the radioactivity of  Cu was higher than that of
Cu was higher than that of 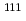 In in all organs except kidney. In tumor-bearing mice,
In in all organs except kidney. In tumor-bearing mice,  Cu-DOTA-TOC showed a high accumulation in the tumors, and the tumor-to-blood ratio reached as high as 8.81
Cu-DOTA-TOC showed a high accumulation in the tumors, and the tumor-to-blood ratio reached as high as 8.81  1.17 at 6 h after administration.
1.17 at 6 h after administration.  Cu-DOTA-TOC showed significantly higher accumulation in the tumor than
Cu-DOTA-TOC showed significantly higher accumulation in the tumor than  Cu-TETA-OC and
Cu-TETA-OC and  Cu-DOTA-OC. PET showed a very clear image of the tumor, which was comparable to that of
Cu-DOTA-OC. PET showed a very clear image of the tumor, which was comparable to that of 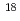 F-FDG PET and very similar to that of
F-FDG PET and very similar to that of  Cu-TETA-OC.
Cu-TETA-OC.  Cu-DOTA-TOC clearly imaged a somatostatin receptor-positive tumor and seemed to be a potential PET tracer in the clinical phase.
Cu-DOTA-TOC clearly imaged a somatostatin receptor-positive tumor and seemed to be a potential PET tracer in the clinical phase.
津久井 匠隆; 渡邉 茂樹; 山田 圭一*; 花岡 宏史*; 奥 浩之*; 松尾 一郎*; 遠藤 啓吾*; 石岡 典子
no journal, ,
生理活性ペプチドの中には、抗がん作用,抗菌作用を示すものやホルモン様作用を示して受容体と結合するものがあり、創薬のリード化合物となり得る。われわれが開発したパラ位に臭素原子が置換された芳香族アミノ酸を構造中に有する環状ペプチドは、インビトロ実験において乳がん細胞の増殖抑制能を有することが明らかになっている。そこで、インビボ実験における体内分布の取得を目指し、開発した環状ペプチドへの放射性臭素の標識に関する基礎検討を実施した。構成アミノ酸である芳香族アミノ酸誘導体の標識条件では、前駆体に対しCATを1等量、NCSでは4等量加え、室温15分間反応させることで、それぞれ標識率70%で反応が進行し、効率よくBr-77を導入できることを確認した。標識前駆体の合成では、Boc-SPPS法により生成した化合物についてESI-MS分析を行った結果、目的物に相当するイオンピークは得られず、トリブチルスズアミノ酸を用いるBoc-SPPS法は環状ペプチド合成に適していないことが明らかとなった。そこで、現在新たな合成法として脱保護に塩基を用いるFmoc-SPPSによる合成について検討を行っている。
津久井 匠隆; 渡邉 茂樹; 花岡 宏史*; 山田 圭一*; 奥 浩之*; 石岡 典子; 遠藤 啓吾*; 松尾 一郎*
no journal, ,
生理活性ペプチドには顕著な抗腫瘍活性を示すものがあり、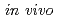 での治療効果に興味が持たれている。これらの生理活性ペプチドにおける構造活性相関等の創薬研究は、さまざまな所で行われている。創薬研究では、薬剤の体内分布や腫瘍への集積能が重要な因子となり得る。演者らは、放射性核種を標識した生理活性ペプチドを用いて体内での薬剤挙動と治療効果を同時に計測できれば薬剤開発の効率化が可能になると考え、その標識化法を検討している。本発表では、Boc-Phe(
での治療効果に興味が持たれている。これらの生理活性ペプチドにおける構造活性相関等の創薬研究は、さまざまな所で行われている。創薬研究では、薬剤の体内分布や腫瘍への集積能が重要な因子となり得る。演者らは、放射性核種を標識した生理活性ペプチドを用いて体内での薬剤挙動と治療効果を同時に計測できれば薬剤開発の効率化が可能になると考え、その標識化法を検討している。本発表では、Boc-Phe(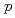 -SnBu
-SnBu )-OMeを前駆体としたBr-77標識アミノ酸の合成に関する基礎的検討について報告する。酸化剤にChloramine T、N-Chlorosuccinimideを用いて室温30分間標識化したところ、その標識率は60
)-OMeを前駆体としたBr-77標識アミノ酸の合成に関する基礎的検討について報告する。酸化剤にChloramine T、N-Chlorosuccinimideを用いて室温30分間標識化したところ、その標識率は60 85%であった。現在、Phe(
85%であった。現在、Phe(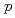 -SnBu
-SnBu )含有ペプチドへの適用も検討しており、併せて報告する予定である。
)含有ペプチドへの適用も検討しており、併せて報告する予定である。
 Br標識アミノ酸誘導体の開発
Br標識アミノ酸誘導体の開発花岡 宏史*; 渡邉 茂樹; 富永 英之*; 大島 康宏; 津久井 匠隆; 渡辺 智; 山田 圭一*; 飯田 靖彦*; 織内 昇*; 樋口 徹也*; et al.
no journal, ,
 Cや
Cや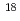 Fで標識したアミノ酸誘導体は、がん診断用のPET薬剤として、臨床使用されているものも少なくない。しかしながら
Fで標識したアミノ酸誘導体は、がん診断用のPET薬剤として、臨床使用されているものも少なくない。しかしながら Cや
Cや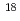 Fは短半減期であるため、それぞれの病院で製造する必要があり、限られた施設でしか使えないのが現状である。一方で
Fは短半減期であるため、それぞれの病院で製造する必要があり、限られた施設でしか使えないのが現状である。一方で Brは半減期が16.1時間とポジトロン放出核種としては比較的長く、また
Brは半減期が16.1時間とポジトロン放出核種としては比較的長く、また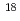 Fと同じハロゲン核種であるため、
Fと同じハロゲン核種であるため、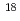 F標識アミノ酸製剤と同様の分子設計を行うことができるという利点を有する。そこで本研究では、広く臨床使用することが可能な、新規がん診断用PETイメージング薬剤として
F標識アミノ酸製剤と同様の分子設計を行うことができるという利点を有する。そこで本研究では、広く臨床使用することが可能な、新規がん診断用PETイメージング薬剤として Br標識アミノ酸誘導体を開発することを計画した。基礎的検討には半減期が長い放射性臭素である
Br標識アミノ酸誘導体を開発することを計画した。基礎的検討には半減期が長い放射性臭素である Br(半減期57時間)を用いて行うこととした。Br標識アミノ酸としては、
Br(半減期57時間)を用いて行うこととした。Br標識アミノ酸としては、 -メチルフェニルアラニンのパラ位にBrを導入したp-Bromo-
-メチルフェニルアラニンのパラ位にBrを導入したp-Bromo- -methyl-Pheを設計した。
-methyl-Pheを設計した。 Br標識Phe誘導体は標識率25
Br標識Phe誘導体は標識率25 40%で合成することができた。ノーマルマウスにおける体内動態を検討した結果、膵臓に高い集積が認められたことから、本化合物はアミノ酸トランスポーターに認識されていることが示唆された。一方で腎臓に対しても高い集積がみられた。担癌マウスに投与したところ、腫瘍への高い集積性を示し、投与3時間後の腫瘍血液比は3.94、腫瘍筋肉比は3.51となった。以上の結果から、Br標識Phe誘導体は、新規がんイメージング剤として有用である可能性が示された。
40%で合成することができた。ノーマルマウスにおける体内動態を検討した結果、膵臓に高い集積が認められたことから、本化合物はアミノ酸トランスポーターに認識されていることが示唆された。一方で腎臓に対しても高い集積がみられた。担癌マウスに投与したところ、腫瘍への高い集積性を示し、投与3時間後の腫瘍血液比は3.94、腫瘍筋肉比は3.51となった。以上の結果から、Br標識Phe誘導体は、新規がんイメージング剤として有用である可能性が示された。
津久井 匠隆; 山田 圭一*; 渡邉 茂樹; 花岡 宏史*; 奥 浩之*; 遠藤 啓吾*; 石岡 典子; 松尾 一郎*
no journal, ,
p-(tri-n-butyl-stannyl)-phenylalanine (Phe(p-Bu Sn)) is an useful building blocks for synthesizing radiolabeled pharmaceutics. To best of our knowledge, there are few studies of the synthesis of Phe(p-Bu
Sn)) is an useful building blocks for synthesizing radiolabeled pharmaceutics. To best of our knowledge, there are few studies of the synthesis of Phe(p-Bu Sn)-containing peptides. In this study, we report solid-phase synthesis of cyclic peptides containing Phe(p-Bu
Sn)-containing peptides. In this study, we report solid-phase synthesis of cyclic peptides containing Phe(p-Bu Sn) residue, cyclo(Phe(p-Bu
Sn) residue, cyclo(Phe(p-Bu Sn)-Leu-MeLeu-Val-Leu) (I). Boc-Phe(p-Bu
Sn)-Leu-MeLeu-Val-Leu) (I). Boc-Phe(p-Bu Sn)-OH was synthesized from Boc-Phe(p-I)-OMe by treatment with bis(tri-n-butyl)tin and Pd(0) catalyst followed by saponification. The linear peptide containing Phe(p-Bu
Sn)-OH was synthesized from Boc-Phe(p-I)-OMe by treatment with bis(tri-n-butyl)tin and Pd(0) catalyst followed by saponification. The linear peptide containing Phe(p-Bu Sn) residue was assembled on Kaiser-oxime resin. On-resin macrocyclization of the linear peptide, however, did not afford the cyclic peptide I. Cross coupling of cyclic peptide containing Phe(p-I) residue, cyclo(Phe(p-I)-Leu-MeLeu-Val-Leu) with bis(tri-n-butyl)tin and Pd(0) catalyst gave the desired peptide, which was confirmed by ESI-MS. In this presentation, we will report the Fmoc-SPPS of the peptide I.
Sn) residue was assembled on Kaiser-oxime resin. On-resin macrocyclization of the linear peptide, however, did not afford the cyclic peptide I. Cross coupling of cyclic peptide containing Phe(p-I) residue, cyclo(Phe(p-I)-Leu-MeLeu-Val-Leu) with bis(tri-n-butyl)tin and Pd(0) catalyst gave the desired peptide, which was confirmed by ESI-MS. In this presentation, we will report the Fmoc-SPPS of the peptide I.
 I-Sansalvamide Aの合成と評価
I-Sansalvamide Aの合成と評価渡邉 茂樹; 津久井 匠隆; 花岡 宏史*; 山田 圭一*; 大島 康宏; 飯田 靖彦*; 遠藤 啓吾*; 石岡 典子
no journal, ,
抗がん作用や抗菌作用を示す生理活性物質は、創薬におけるリード化合物となる。Sansalvamide A(SA)は、構造中にエステル結合を有する海洋真菌類由来の環状デプシペプチドで、大腸がん細胞に対して高い細胞毒性を示すことから、抗がん剤開発のリード化合物として注目されている。これまでわれわれは、フェニルアラニン側鎖にヨウ素を導入したSA誘導体を開発し、この化合物が悪性度の高い乳がん細胞MD-MBA-231に対して高い細胞障害活性を示すことを明らかにしてきた。そこで、本研究ではI-SAの生体内における動態を解明するために、 Iを導入した
Iを導入した I-SAを合成し、ノーマルマウスにおける体内分布を明らかにすることとした。
I-SAを合成し、ノーマルマウスにおける体内分布を明らかにすることとした。
 -Lactamase derived from
-Lactamase derived from 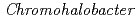 sp.560
sp.560新井 栄揮; 徳永 廣子*; 玉田 太郎; 米澤 悌; 安達 基泰; 山田 貢; 石橋 松二郎*; 徳永 正雄*; 黒木 良太
no journal, ,
好塩性蛋白質は、表面に存在する多くの酸性アミノ酸残基によってさまざまな無機イオンを結合することができる。好塩性蛋白質はレアメタルや放射性金属イオンの捕集材料として用いることができる可能性があるため、分子構造・機能研究グループでは好塩性蛋白質の分子構造を研究している。最近、分子構造・機能研究グループでは、中度好塩菌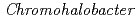 sp.560由来
sp.560由来 -Lactamase(HaBLA)のX線結晶解析に成功した。Photon FactoryのNE3Aビームラインにより、3.0
-Lactamase(HaBLA)のX線結晶解析に成功した。Photon FactoryのNE3Aビームラインにより、3.0 分解能の回折データを収集し、構造解析を行った結果、HaBLAの主鎖構造は非好塩性
分解能の回折データを収集し、構造解析を行った結果、HaBLAの主鎖構造は非好塩性 -Lactamaseと類似した構造をとるが、HaBLAの分子表面は大部分が負電荷で占められることが判明した。このような構造学的情報は、CsやSrのような金属の特異性を向上させるために有効となる。
-Lactamaseと類似した構造をとるが、HaBLAの分子表面は大部分が負電荷で占められることが判明した。このような構造学的情報は、CsやSrのような金属の特異性を向上させるために有効となる。
山田 圭一*; 渡邉 茂樹; 大島 康宏; 花岡 宏史*; 津久井 匠隆*; 高野 智香子*; 山口 藍子*; 奥 浩之*; 石岡 典子
no journal, ,
Sansalvamide A (SA) is a marin-derived cyclic depsipeptide that exhibits cytotoxicity against colon cancer cell line. Recently, a series of cyclic pentapeptide analogs of SA in which Hmp ((2S)-2-hydroxy-4-methylpentanoic acid) residue was replaced by amino acids or N-methyl-amino acids were synthesized. We previously reported that the haogenated analog of [MeLeu ]SA, namely SA-Br, SA-I, SA-Cl, exhibited potent cytotoxicity against MDA-MB-231. In the present study, we considered to evaluate in vivo biodistribution, stability and antitumor activity of these halogenated SA peptides in tumor-bearing mice. For this purpose, radiohalogen atoms are most suitable for labeling without changing their primary structure and biological activity. Here, we report the synthesis and in vivo biodistribution of
]SA, namely SA-Br, SA-I, SA-Cl, exhibited potent cytotoxicity against MDA-MB-231. In the present study, we considered to evaluate in vivo biodistribution, stability and antitumor activity of these halogenated SA peptides in tumor-bearing mice. For this purpose, radiohalogen atoms are most suitable for labeling without changing their primary structure and biological activity. Here, we report the synthesis and in vivo biodistribution of  I-labeled SA analog (SA-[
I-labeled SA analog (SA-[ I]).
I]).
 I標識環状ペプチドSansalvamide A誘導体の合成と評価
I標識環状ペプチドSansalvamide A誘導体の合成と評価渡邉 茂樹; 山田 圭一*; 花岡 宏史*; 大島 康宏; 津久井 匠隆*; 高野 智香子*; 山口 藍子*; 奥 浩之*; 飯田 靖彦*; 遠藤 啓吾*; et al.
no journal, ,
Sansalvamide A(SA)は、抗腫瘍活性を持つ海洋真菌類由来の天然環状ペプチドである。われわれはSAのPhe側鎖芳香環にハロゲンを導入した誘導体SA-X(cyclo(Phe(p-X)-Leu-MeLeu-Val-Leu), X=Cl, Br, I)を合成し、これらが乳がん細胞MDA-MB-231に対してin vitroで細胞毒性を持つことを見いだした。本研究ではin vivo評価を目的として I標識Sansalvamide A誘導体[
I標識Sansalvamide A誘導体[ I]SA-Iの合成について検討した。その結果、Boc固相合成法により直鎖ペプチドBoc-Phe(p-SnBu
I]SA-Iの合成について検討した。その結果、Boc固相合成法により直鎖ペプチドBoc-Phe(p-SnBu )-Leu-MeLeu-Val-Leu-OMeを得た後、スズ-ヨウ素交換反応による
)-Leu-MeLeu-Val-Leu-OMeを得た後、スズ-ヨウ素交換反応による I標識,脱保護、及び、液相での環化を行うことで[
I標識,脱保護、及び、液相での環化を行うことで[ I]SA-Iを合成できることを見いだした。
I]SA-Iを合成できることを見いだした。
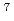 Li+
Li+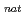 Pb反応でのAtの製造とAtの簡易化学分離
Pb反応でのAtの製造とAtの簡易化学分離西中 一朗; 横山 明彦*; 鷲山 幸信*; 天野 良平*; 李 恵子*; 山田 記大*; 石黒 梨花*; 前田 英太*; 牧井 宏之; 橋本 和幸; et al.
no journal, ,
標的アルファ放射線療法で期待されるアルファ放射性核種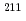 Atの製造と利用の研究を開始した。タンデム加速器施設で29-48MeV
Atの製造と利用の研究を開始した。タンデム加速器施設で29-48MeV 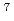 Li+
Li+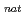 Pb反応で生成する放射性同位体アスタチンの生成断面積をアルファ線,
Pb反応で生成する放射性同位体アスタチンの生成断面積をアルファ線, 線スペクトロメトリーによって求めた。加えてアスタチンの簡易化学分離法を開発した。
線スペクトロメトリーによって求めた。加えてアスタチンの簡易化学分離法を開発した。
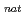 Pb reaction
Pb reaction西中 一朗; 横山 明彦*; 鷲山 幸信*; 天野 良平*; 前田 英太*; 山田 記大*; 牧井 宏之; 渡邉 茂樹; 石岡 典子; 橋本 和幸
no journal, ,
An  radioactive nuclide
radioactive nuclide 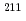 At with a half-life of 7.2 h is a prospective candidate for utilization in targeted alpha radiotherapy. In a general way,
At with a half-life of 7.2 h is a prospective candidate for utilization in targeted alpha radiotherapy. In a general way, 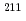 At is produced through the
At is produced through the 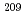 Bi(
Bi( ,2n)
,2n)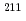 At reaction. However, the nuclear reactions using lithium ion beams provide the possible production routes of
At reaction. However, the nuclear reactions using lithium ion beams provide the possible production routes of 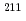 At. Therefore, we have measured excitation functions of At isotopes in the reaction of 29-57 MeV
At. Therefore, we have measured excitation functions of At isotopes in the reaction of 29-57 MeV 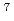 Li +
Li + 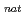 Pb at the tandem accelerator of JAEA-Tokai. The cross sections of radioactive products were determined by
Pb at the tandem accelerator of JAEA-Tokai. The cross sections of radioactive products were determined by  - and
- and  -ray spectrometry. The experimental excitation functions of astatine isotopes have been compared with a statistical calculation to study the reaction mechanism. Besides, a chemical separation of carrier-free radioactive astatine isotopes from an irradiated target has been studied with a dry-chemistry method. Details will be shown in the presentation.
-ray spectrometry. The experimental excitation functions of astatine isotopes have been compared with a statistical calculation to study the reaction mechanism. Besides, a chemical separation of carrier-free radioactive astatine isotopes from an irradiated target has been studied with a dry-chemistry method. Details will be shown in the presentation.