Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
大野 英雄; 綱脇 恵章*; 梅咲 則正*; 古川 和男; 岩本 信也*
J.Chem.Res., p.158 - 159, 1978/00
溶融LiBeF およびFlinak(LiF-NaF-KF共晶混合物)中のフッ素の自己拡散係数を、
およびFlinak(LiF-NaF-KF共晶混合物)中のフッ素の自己拡散係数を、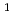
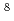 Fトレーサーとして毛管浸漬法により測定した。溶融LiBeF
Fトレーサーとして毛管浸漬法により測定した。溶融LiBeF 中およびFlinak中のフッ素の自己拡散係数D
中およびFlinak中のフッ素の自己拡散係数D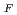 (cm
(cm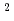 /sec)は、D
/sec)は、D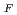 =1.23
=1.23 10
10 exp〔-(29.4
exp〔-(29.4 3.9)
3.9) 10
10 /RT〕(LiBeF
/RT〕(LiBeF ),D
),D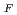 =2.77
=2.77 10
10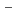
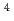 exp〔-(5.01
exp〔-(5.01 1.00)
1.00) 10
10 ・RT〕(Flinak)で表わされる。溶融Flinak(LiF-BeF
・RT〕(Flinak)で表わされる。溶融Flinak(LiF-BeF 系)中のフッ素の自己拡散現象と溶融珪酸塩中の酸素の自己拡散現象との類似性について考察した。また実験上の誤差となる原因についても考察した。
系)中のフッ素の自己拡散現象と溶融珪酸塩中の酸素の自己拡散現象との類似性について考察した。また実験上の誤差となる原因についても考察した。
勝田 博司; 古川 和男
J.Chem.Res.,Part S, (12), p.322 - 323, 1977/12
一定の水素濃度を有する液体Naの平衡水素圧力は、温度が高くなると減少する。一方液体Liの場合はこれと逆である。また液体Na中の水素、酸素溶解度は180 C以下の温度ではArrhenis形の直線からずれて、高い値をとるようになるが、Li中の水素溶解度はArrhenisの直線が表すことができる。液体Li-H素では、10at,%,以上の高い水素濃度になると、H-H相互作用のためにSievertsの法則が成立しなくなる。これらの現象について、液体NaやLiを擬結晶とみなして、統計熱力学的解析を試みた。計算結果と実験結果を比較することにより、いくつかの熱力学的数値の確定をすることができた。例としては、NaとHの相互作用エネルギー(N
C以下の温度ではArrhenis形の直線からずれて、高い値をとるようになるが、Li中の水素溶解度はArrhenisの直線が表すことができる。液体Li-H素では、10at,%,以上の高い水素濃度になると、H-H相互作用のためにSievertsの法則が成立しなくなる。これらの現象について、液体NaやLiを擬結晶とみなして、統計熱力学的解析を試みた。計算結果と実験結果を比較することにより、いくつかの熱力学的数値の確定をすることができた。例としては、NaとHの相互作用エネルギー(N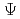
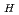
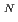 a)=-48kcal/mol,LiとHの相互作用エネルギー(N
a)=-48kcal/mol,LiとHの相互作用エネルギー(N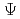
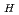
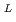 i)=-58kcal/mol,NaとO,NaとOH相互作用エネルギーの差(N
i)=-58kcal/mol,NaとO,NaとOH相互作用エネルギーの差(N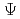
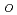
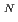 a-N
a-N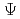
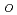 H
H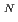 a)=76kcal/mol,Li中のH-H相互作用エネルギー(N
a)=76kcal/mol,Li中のH-H相互作用エネルギー(N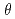
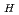 -H
-H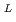 i)=-0.3~-0.9kcal/mol
i)=-0.3~-0.9kcal/mol