The Contribution of the Japanese team; Neutron diffraction experiment of fully deuterated proteins, such as RNase A, insulin, myoglobin and so on
完全重水素化試料(RNase A,インスリン,ミオグロビン)の中性子回折実験; 日本チーム分担
新村 信雄*; 田中 伊知朗*; 大西 裕季*; Ostermann, A.*; 栗原 和男; 本庄 栄二郎; 黒木 良太; 二見 淳一郎*; 山田 秀徳*
Niimura, Nobuo*; Tanaka, Ichiro*; Onishi, Yuki*; Ostermann, A.*; Kurihara, Kazuo; Honjo, Eijiro; Kuroki, Ryota; Futami, Junichiro*; Yamada, Hidenori*
本研究の目的は、中性子回折データを用いて厳密な数学的手法だけでタンパク質分子構造を決定する新しい方法を開発し、幾つかのタンパク質に適用してこれを実証することにある。この手法では、水素原子を特異的に重水素原子に置き換えた結晶を利用する。本研究は、各々特徴のある中性子関連研究を行ってきている日・仏・米3か国の研究グループによる共同研究(筆頭提案者: H. A. Hauptman/Hauptman研(米))である。日本グループ(共同提案者:新村信雄/茨城大学)では主としてタンパク質の結晶化と中性子回折実験を担当し、高分解能で精度の高い中性子回折データの取得を目指す。当初は研究対象を基本的なタンパク質(ミオグロビン,インスリン,RNase Aなど)に限定する。後に、仏グループ(共同提案者: A. Podjarny/IGBMC)から提供される重水素置換タンパク質(ルブレドキシン,アルドース還元酵素など)も対象に加える。これらの中性子回折実験データを用い米グループが解析を行う。当会議では、上記の方針に則った日本グループ側の研究計画を説明,議論する。
Our goal is to develop new methods for determining macromolecular crystal structures 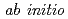 from neutron diffraction data and to validate these methods by making applications to several proteins. The proposed methods, which have the potential to be more powerful than X-ray ones, exploit perfectly isomorphous pairs of crystals that differ by replacement of D atoms with H atoms in selected amino-acid residues. This research involves collaboration among teams on three continents that have expertise in different aspects of neutron crystallography. The Japanese team measures high-resolution neutron diffraction data from protein crystals to answer questions about H bonding, protonation, hydration, and enzyme mechanisms. The team will focus on fundamental and simple proteins such as myoglobin, insulin, and RNase A at the first stage and then on rubredoxin, aldose reductase and other samples from the French team. In the meeting the research plan of the Japanese team will be reported.
from neutron diffraction data and to validate these methods by making applications to several proteins. The proposed methods, which have the potential to be more powerful than X-ray ones, exploit perfectly isomorphous pairs of crystals that differ by replacement of D atoms with H atoms in selected amino-acid residues. This research involves collaboration among teams on three continents that have expertise in different aspects of neutron crystallography. The Japanese team measures high-resolution neutron diffraction data from protein crystals to answer questions about H bonding, protonation, hydration, and enzyme mechanisms. The team will focus on fundamental and simple proteins such as myoglobin, insulin, and RNase A at the first stage and then on rubredoxin, aldose reductase and other samples from the French team. In the meeting the research plan of the Japanese team will be reported.