Conformational ensemble of a multidomain protein explored by Gd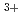 electron paramagnetic resonance
electron paramagnetic resonance
ガドリニウム(III)EPRによるマルチドメイン蛋白質酵素の構造アンサンブルの研究
齋尾 智英*; 平松 蒼野*; 浅田 瑞枝*; 中川 洋 

 ; 清水 和美*; 久米田 博之*; 中村 敏和*; 石森 浩一郎*
; 清水 和美*; 久米田 博之*; 中村 敏和*; 石森 浩一郎*
Saio, Tomohide*; Hiramatsu, Soya*; Asada, Mizue*; Nakagawa, Hiroshi; Shimizu, Kazumi*; Kumeta, Hiroyuki*; Nakamura, Toshikazu*; Ishimori, Koichiro*
電子常磁性共鳴分光法を用いてタンパク質上の2点間の距離を測定し、マルチドメインタンパク質酵素MurDの構造状態と分布を調べた。これまでの結晶学的研究やNMR研究では、MurDの3つの異なる構造状態が報告されていたが、我々のデータは、MurDがリガンドを持たない状態では、より多様な構造状態で存在することを明らかにした。MurDは感染症治療の有力なターゲットの一つであることから、本研究の成果は創薬のための重要な構造基盤を提供するものと考えられる。
A rigid double-arm lanthanide tag was utilized in electron paramagnetic resonance spectroscopy to measure the distance between two specific points on a protein, and conformational states and distribution of a multi-domain protein enzyme MurD was investigated. Although the previous crystallographic and NMR studies have reported the three distinct conformational states of MurD, our data unveiled that the protein exists in much more variety of conformational states in the absence of the ligand. Given the fact that MurD is one of the potent drug target for infectious diseases, the finding in this study will provide important structural basis for drug development.