Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
高橋 昭久*; 久保 誠*; 五十嵐 千恵*; 吉田 由香里*; 舟山 知夫; 小林 泰彦; 中野 隆史*
JAEA-Review 2014-050, JAEA Takasaki Annual Report 2013, P. 82, 2015/03
放射線によるDNA二本鎖切断(DSB)は致命的であるが、相同組換え(HR)および非相同末端結合(NHEJ)によって修復される。そこで、我々は殺細胞効果におよぼすDNA二本鎖切断修復のLET依存性を明らかにすることを目的に、DNA二本鎖切断修復の異なる細胞における高LET放射線感受性をコロニー形成法で評価した。その結果、NHEJがはたらく野生型細胞とHR欠損細胞は108keV/ mの炭素線で高いRBE値を示した。SER値はHR修復欠損ではLETの違いによらず約2と一定だったのに対して、NHEJ修復欠損ではX線に比べて、HR修復欠損よりも高い値を示した。
mの炭素線で高いRBE値を示した。SER値はHR修復欠損ではLETの違いによらず約2と一定だったのに対して、NHEJ修復欠損ではX線に比べて、HR修復欠損よりも高い値を示した。
高橋 昭久*; 久保 誠*; Ma, H.*; 中川 彰子*; 吉田 由香里*; 磯野 真由*; 金井 達明*; 大野 達也*; 古澤 佳也*; 舟山 知夫; et al.
Radiation Research, 182(3), p.338 - 344, 2014/09
被引用回数:60 パーセンタイル:89.83(Biology)DNA二本鎖切断(DSB)は相同組換え(HR)と非相同末端結合(NHEJ)により修復される。重粒子線治療における放射線増感剤の標的候補を明らかにすることを目的とした。がん抑制遺伝子p53欠損マウス胚線維芽細胞由来の野生型細胞, HR修復欠損細胞, NHEJ修復欠損細胞,二重修復欠損細胞を用いた。各細胞にX線,炭素線,鉄線,ネオン線,アルゴン線を照射し、コロニー形成法で生存率を調べた。10%生存率線量値(D10値)を用いて、増感比は(野生型細胞のD10値)/(修復欠損細胞のD10値)の式で算出した。D10値はいずれの線質においても、野生型細胞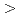 HR修復欠損細胞
HR修復欠損細胞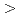 NHEJ修復欠損細胞
NHEJ修復欠損細胞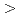 二重修復欠損細胞の順に低くなった。HR修復欠損による増感比はLET無関係に一定で約2であった。一方、NHEJ修復欠損の増感比はLETが高くなるに従い減少するものの、HR修復欠損よりも高い増感効果を示した。高LET放射線の高RBEの要因はNHEJ修復の抑制と誤修復であり、炭素線における増感剤の主要な標的候補はNHEJ修復であることが示唆された。
二重修復欠損細胞の順に低くなった。HR修復欠損による増感比はLET無関係に一定で約2であった。一方、NHEJ修復欠損の増感比はLETが高くなるに従い減少するものの、HR修復欠損よりも高い増感効果を示した。高LET放射線の高RBEの要因はNHEJ修復の抑制と誤修復であり、炭素線における増感剤の主要な標的候補はNHEJ修復であることが示唆された。
村田 和俊*; 野田 真永*; 尾池 貴洋*; 高橋 昭久*; 吉田 由香里*; 鈴木 義行*; 大野 達也*; 舟山 知夫; 小林 泰彦; 高橋 健夫*; et al.
Journal of Radiation Research, 55(4), p.658 - 664, 2014/07
被引用回数:15 パーセンタイル:51.32(Biology)ヒト肺がん細胞A549株のRhoシグナル伝達経路を介した遊走能に対し、炭素線照射が及ぼす影響を解析した。照射48時間経過後、炭素線照射したA549細胞の遊走能は大きくなり、遊走突起の形成も増加した。この遊走能の炭素線照射による増加は、X線照射後のそれと類似していた。ウェスタンブロット解析の結果は、照射した細胞がP-MLC2-S19タンパク質発現を増加させている一方で、MLC2タンパク質ファミリー全体の発現量に変化がないことを示した。ROCKタンパク質阻害剤であるY-27632の細胞への投与は、このP-MLC2-S19タンパク質の発現増加を抑制し、遊走能を低下させた。これらの結果より、ヒト肺がん細胞A549細胞への炭素線照射は、細胞遊走能をRhoシグナル伝達経路経由で増加させており、それはROCKタンパク質阻害剤で抑制されることが明らかとなった。
浜田 信行*; 今岡 達彦*; 増永 慎一郎*; 尾方 俊至*; 岡安 隆一*; 高橋 昭久*; 加藤 宝光*; 小林 泰彦; 大西 武雄*; 小野 公二*; et al.
Journal of Radiation Research, 51(4), p.365 - 383, 2010/07
被引用回数:124 パーセンタイル:90.99(Biology)Superb biological effectiveness and dose conformity represent a rationale for heavy-ion therapy, which has thus far achieved good cancer controllability while sparing critical normal organs. Immediately after irradiation, heavy ions produce dense ionization along their trajectories, cause irreparable clustered DNA damage, and alter cellular ultrastructure. These ions, as a consequence, inactivate cells more effectively with less cell-cycle and oxygen dependence than conventional photons. The modes of heavy ion-induced cell death/inactivation include apoptosis, necrosis, autophagy, premature senescence, accelerated differentiation, delayed reproductive death of progeny cells, and bystander cell death. This paper briefly reviews the current knowledge of the biological aspects of heavy-ion therapy, with emphasis on the authors' recent findings. The topics include (1) repair mechanisms of heavy ion-induced DNA damage, (2) superior effects of heavy ions on radioresistant tumor cells (intratumor quiescent cell population, TP53-mutated and BCL2-overexpressing tumors), (3) novel capacity of heavy ions in suppressing cancer metastasis and neoangiogenesis, and (4) potential of heavy ions to induce secondary (especially breast) cancer.
松本 英樹*; 浜田 信行*; 高橋 昭久*; 小林 泰彦; 大西 武雄*
Journal of Radiation Research, 48(2), p.97 - 106, 2007/03
被引用回数:123 パーセンタイル:89.73(Biology)細胞に低線量の放射線をあらかじめ照射しておくと、高線量の放射線に抵抗性を示すことが知られており、この現象は放射線適応応答と呼ばれている。本総説では、放射線適応応答と、バイスタンダー効果(放射線の生物効果が、直接照射された細胞から、その周囲の非照射細胞に伝達される現象)との関連性を概説する。
松本 英樹*; 畑下 昌範*; 高橋 昭久*; 浜田 信行*; 和田 成一*; 舟山 知夫; 坂下 哲哉; 柿崎 竹彦; 小林 泰彦
JAEA-Review 2006-042, JAEA Takasaki Annual Report 2005, P. 111, 2007/02
A classical paradigm of radiation biology asserts that all radiation effects on cells, tissues and organisms are due to the direct action of radiation. However, there has been a recent growth of interest in the indirect actions of radiation including the radiation-induced adaptive response, the bystander effect, low-dose hypersensitivity, and genomic instability, which are specific modes of stress exhibited in response to low-dose/low-dose rate radiation. However, mechanisms of these phenomena are not fully known. The objective of this project is to elucidate molecular mechanisms of the bystander effect using heavy ion microbeams in JAEA. We found that the foci of  H2A.X were formed in the unirradiated cells in the target colony including the irradiated cell 30 min after irradiation with 260 MeV
H2A.X were formed in the unirradiated cells in the target colony including the irradiated cell 30 min after irradiation with 260 MeV 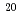 Ne beams and that this formation of the foci was almost completely suppressed by the addition of NO specific scavenger, c-PTIO. Also we found that the foci of
Ne beams and that this formation of the foci was almost completely suppressed by the addition of NO specific scavenger, c-PTIO. Also we found that the foci of  H2A.X were formed in the unirradiated cells in the untargeted colonies 6 h after irradiation with 260 MeV
H2A.X were formed in the unirradiated cells in the untargeted colonies 6 h after irradiation with 260 MeV  Ne beams and that this formation of the foci was almost completely suppressed by the addition of c-PTIO. Our findings demonstrate that NO is an initiator/mediator for evoking heavy ion microbeam-induced bystander effects.
Ne beams and that this formation of the foci was almost completely suppressed by the addition of c-PTIO. Our findings demonstrate that NO is an initiator/mediator for evoking heavy ion microbeam-induced bystander effects.
松本 英樹*; 畑下 昌範*; 高橋 昭久*; 浜田 信行*; 和田 成一*; 小林 泰彦; 舟山 知夫; 坂下 哲哉; 柿崎 竹彦
no journal, ,
標的コロニーの細胞1個に5 10粒子のNeイオンを照射30分後、同一コロニー中の非照射細胞において細胞あたり数個の
10粒子のNeイオンを照射30分後、同一コロニー中の非照射細胞において細胞あたり数個の H2AXフォーカスが認められた。このフォーカス形成は一酸化窒素(NO)ラジカル消去剤であるc-PTIOの添加により消失した。周囲の非標的コロニー内の細胞において、照射6時間後に細胞あたり1
H2AXフォーカスが認められた。このフォーカス形成は一酸化窒素(NO)ラジカル消去剤であるc-PTIOの添加により消失した。周囲の非標的コロニー内の細胞において、照射6時間後に細胞あたり1 2個の
2個の H2AXのフォーカスが認められた。このフォーカス形成はc-PTIOの添加により消失した。
H2AXのフォーカスが認められた。このフォーカス形成はc-PTIOの添加により消失した。
村田 和俊*; 野田 真永*; 尾池 貴洋*; 高橋 昭久*; 吉田 由香里*; 鈴木 義行*; 大野 達也*; 舟山 知夫; 小林 泰彦; 高橋 健夫*; et al.
no journal, ,
本研究では、Rho情報伝達経路を介したヒト肺がん細胞A549株の細胞遊走能に炭素イオン照射が及ぼす影響を明らかにすることを研究の目的とした。細胞遊走能の定量はwound-healingアッセイを、細胞表面突起の形成の評価はFアクチン染色を用いた。細胞生存率はWST-1アッセイを用いて定量し、MLC2タンパク質の発現量および同タンパクセリン19残基のリン酸化量の定量にはウエスタンハイブリダイゼーション法を用いた。炭素イオン照射したA549細胞における照射効果をこれらの方法で解析した結果、炭素イオン照射が、A549細胞の遊走能をRho情報伝達経路を介して増加させる一方で、Rho結合キナーゼ阻害剤によりその照射効果が抑制されることが明らかになった。