Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
金尾 忠芳*; 小坂 恵*; 吉田 京矢*; 中山 久之*; 玉田 太郎; 黒木 良太; 山田 秀徳; 高田 潤*; 上村 一雄*
Acta Crystallographica Section F, 69(6), p.692 - 694, 2013/06
被引用回数:10 パーセンタイル:58.18(Biochemical Research Methods)鉄硫黄酸化細菌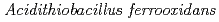 由来テトラチオン酸加水分解酵素(tetrathionate hydrolase)は無機硫黄化合物の加水分解を触媒する。組換え型酵素
由来テトラチオン酸加水分解酵素(tetrathionate hydrolase)は無機硫黄化合物の加水分解を触媒する。組換え型酵素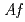 -Tthを大腸菌を用いて封入体として発現し、酸性条件下で活性体に巻き戻した後に、単一に精製した。
-Tthを大腸菌を用いて封入体として発現し、酸性条件下で活性体に巻き戻した後に、単一に精製した。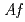 -Tthの結晶は、沈澱剤溶液を33%(
-Tthの結晶は、沈澱剤溶液を33%(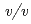 ) PEG 1000、50m
) PEG 1000、50m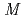 塩化ナトリウム、20m
塩化ナトリウム、20m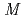 グリシン緩衝液(pH10)としたハンギングドロップ蒸気拡散法により、取得された。結晶は0.2
グリシン緩衝液(pH10)としたハンギングドロップ蒸気拡散法により、取得された。結晶は0.2 0.05
0.05 0.05mmの六角柱状で、X線回折実験の結果、2.15
0.05mmの六角柱状で、X線回折実験の結果、2.15 分解能の回折点が確認され、結晶の空間群は
分解能の回折点が確認され、結晶の空間群は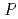 3
3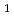 もしくは
もしくは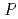 3
3 、格子定数は
、格子定数は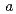 =
=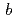 =92.1,
=92.1, 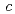 =232.6
=232.6 であった。
であった。
山田 秀徳*; 玉田 太郎; 小坂 恵*; 宮田 幸平*; 藤木 伸哉*; 田納 優*; 守屋 雅之*; 山西 守*; 本庄 栄二郎; 多田 宏子*; et al.
Protein Science, 16(7), p.1389 - 1397, 2007/07
被引用回数:41 パーセンタイル:60.11(Biochemistry & Molecular Biology)タンパク質の結晶格子は分子表面同士の相互作用からなっている。結晶格子内へのタンパク質の導入のため、ロイシンジッパー様の疎水的な相互作用をヒト膵臓RNase1のへリックス2へ導入した。野生型ヒトRNase1の結晶化はまだ報告をされていないが、4残基のロイシンを導入したRNase1では複数の結晶化条件で結晶を得た。そのX線結晶構造をウシRNaseAの立体構造を用いて分子置換法により決定した。こうして決定されたヒトRNase1の立体構造は、ウシRNaseAの立体構造と大変似ており、導入したロイシン残基を介して2分子のRNase1が疎水的なパッキングしていた。ロイシン導入の効果をさらに検討するために、導入したロイシン残基の数を3残基,2残基と減らした変異体を調製し結晶化を行った。これらの場合もロイシン残基による疎水的なパッキングが形成されていた。一方、ロイシン残基をヒトRNase1の別のへリックス(へリックス3)に導入し、効果を検証した。その結果、4残基のロイシンを導入した変異体でも結晶化し、4分子のRNase1が導入したロイシン残基を介してパッキングをしていることがわかった。これらの結果は、適切なロイシン導入により分子内対称性が生じ、より効果的に結晶化を促進する可能性を示す。
小坂 恵*; 金尾 忠芳*; 中山 久之*; 吉田 京矢*; 上村 一雄*; 高田 潤*; 山田 秀徳; 玉田 太郎; 岡崎 伸生*; 黒木 良太
no journal, ,
テトラチオン酸加水分解酵素(tetrathionate hydrolase)は、pH2以下の強酸性環境下でも生育できる好酸性化学合成独立栄養細菌の一種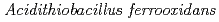 に由来する。本酵素は、硫黄を酸化するエネルギーで生育する
に由来する。本酵素は、硫黄を酸化するエネルギーで生育する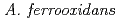 の異化的硫黄代謝において重要な役割を果たしており、他の細菌には類を見ない
の異化的硫黄代謝において重要な役割を果たしており、他の細菌には類を見ない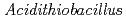 属細菌に特徴的な酵素である。また、それが触媒する反応も極めてユニークである。われわれは本酵素を生成し、これをコードする遺伝子を同定したが、推定される一次構造は極めて特異的であり、相同性が高いものでも15%程度であり、データベースからの機能推定が不可能である、新規な一次構造を持つタンパク質であった。われわれはこの遺伝子を大腸菌に導入し、組み換え発現、リフォールディング、精製により結晶化に成功した。SPring-8での測定で回折データを収集し、構造解析を行っている。
属細菌に特徴的な酵素である。また、それが触媒する反応も極めてユニークである。われわれは本酵素を生成し、これをコードする遺伝子を同定したが、推定される一次構造は極めて特異的であり、相同性が高いものでも15%程度であり、データベースからの機能推定が不可能である、新規な一次構造を持つタンパク質であった。われわれはこの遺伝子を大腸菌に導入し、組み換え発現、リフォールディング、精製により結晶化に成功した。SPring-8での測定で回折データを収集し、構造解析を行っている。