Characterization of a monofunctional catalase KatA from radioresistant bacterium 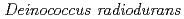
放射線抵抗性細菌デイノコッカス・ラジオデュランスの単機能性カタラーゼKatAの機能解析
小林 一聖*; 田村 隆*; Sghaier, H.; 鳴海 一成; 山口 庄太郎*; 梅田 幸一*; 稲垣 賢二*
Kobayashi, Issei*; Tamura, Takashi*; Sghaier, H.; Narumi, Issei; Yamaguchi, Shotaro*; Umeda, Koichi*; Inagaki, Kenji*
カタラーゼは、活性酸素種から細胞を防御するのに重要な役割を果たしている。この論文では、放射線抵抗性細菌デイノコッカス・ラジオデュランスのカタラーゼKatAの遺伝子クローニング,タンパク質の精製及び機能解析について報告する。KatAタンパク質単量体の分子量は65kDaであり、ゲルろ過でのサイズは240kDaであることから、KatAは溶液中でホモ4量体として存在することが示唆された。精製したKatAタンパク質の活性は、1mg当たり68,800ユニットであった。KatAの活性は、アジ化ナトリウム,シアン化ナトリウム,3-amino-1, 2, 4-triazoleによって阻害された。また、吸収スペクトルは、408nmにソレー帯を示したが、このスペクトルピークは、亜ジチオン酸塩によるKatAの還元反応によって影響を受けなかった。さらに、ペルオキシダーゼ活性は認められなかった。これらの結果は、デイノコッカス・ラジオデュランスのKatAタンパク質が典型的な単機能性のヘム含有カタラーゼであることを示している。過酸化水素ストレスに対するKatAタンパク質の安定性は、市販されているコウジカビとウシ肝臓由来カタラーゼよりも優れていた。細胞中のカタラーゼ含量が比較的豊富なことと、カタラーゼが過酸化水素に耐性を持つという性質が、ラジオデュランスの酸化損傷に対する生存戦略に役割を果たしていると考えられた。
Catalase plays a key role in protecting cells against toxic reactive oxygen species. Here we report on the cloning, purification and characterization of a catalase (KatA) from the extremely radioresistant bacterium 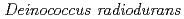 . The size of purified
. The size of purified 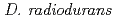 KatA monomer was 65 kDa while gel filtration revealed that the size of the enzyme was 240 kDa, suggesting that KatA formed a homotetramer in solution. Purified KatA displayed a final specific activity of 68,800 U/mg of protein. The catalase activity of KatA was inhibited by sodium azide, sodium cyanide and 3-amino-1, 2, 4-triazole. The absorption spectrum of KatA exhibited a Soret band at 408 nm. The position of the spectral peak remained unchanged following reduction of KatA with dithionite. No peroxidase activity was found for KatA. These results demonstrate that
KatA monomer was 65 kDa while gel filtration revealed that the size of the enzyme was 240 kDa, suggesting that KatA formed a homotetramer in solution. Purified KatA displayed a final specific activity of 68,800 U/mg of protein. The catalase activity of KatA was inhibited by sodium azide, sodium cyanide and 3-amino-1, 2, 4-triazole. The absorption spectrum of KatA exhibited a Soret band at 408 nm. The position of the spectral peak remained unchanged following reduction of KatA with dithionite. No peroxidase activity was found for KatA. These results demonstrate that 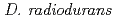 KatA is a typical monofunctional heme-containing catalase. The stability of KatA with respect to H
KatA is a typical monofunctional heme-containing catalase. The stability of KatA with respect to H O
O stress was superior to that of commercially available
stress was superior to that of commercially available 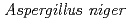 and bovine liver catalases. The relative abundance of KatA in cells in addition to the H
and bovine liver catalases. The relative abundance of KatA in cells in addition to the H O
O resistance property may play a role in the survival strategy of
resistance property may play a role in the survival strategy of 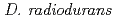 against oxidative damage.
against oxidative damage.