Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
石川 諒尚; 古場 裕介*; 古田 琢哉; Chang, W.*; 米内 俊祐*; 松本 真之介*; 橋本 慎太郎; 平井 悠大*; 佐藤 達彦
Radiological Physics and Technology, 17(2), p.553 - 560, 2024/06
At the Heavy Ion Medical Accelerator in Chiba (HIMAC), a series of retrospective studies are ongoing in patients treated with carbon ion radiotherapy (CIRT) to obtain the knowledge to improve tumor control and reveal the mechanism of the low risk of secondary cancer after CIRT. Dose-averaged linear energy transfer (LET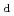 ) is generally used as a measure of treatment effectiveness or biological effects in such retrospective studies; however, it is conventionally evaluated from the relative biological effectiveness (RBE)-LET
) is generally used as a measure of treatment effectiveness or biological effects in such retrospective studies; however, it is conventionally evaluated from the relative biological effectiveness (RBE)-LET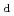 fitted function used in the treatment planning system. In this study, we calculated the physical doses and their linear energy transfer (LET) distributions for a series of treatment plans for a homogeneous rectangular phantom and a human body phantom with typical CIRT beams using Monte Carlo (MC) simulation. The LET
fitted function used in the treatment planning system. In this study, we calculated the physical doses and their linear energy transfer (LET) distributions for a series of treatment plans for a homogeneous rectangular phantom and a human body phantom with typical CIRT beams using Monte Carlo (MC) simulation. The LET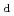 was then deduced from the MC simulation and compared with the corresponding data obtained using the conventional method. The comparison suggested that the two types of LET
was then deduced from the MC simulation and compared with the corresponding data obtained using the conventional method. The comparison suggested that the two types of LET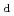 agreed well with each other, except around the distal end of the spread-out Bragg peak, where the MC simulation yielded significantly higher LET
agreed well with each other, except around the distal end of the spread-out Bragg peak, where the MC simulation yielded significantly higher LET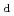 values than that of the conventional method. This is because the RBE-LET
values than that of the conventional method. This is because the RBE-LET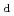 fitted function adopted in the conventional method ignores the contribution of the high-LET components, causing an overkill effect. Furthermore, an MC simulation was conducted to determine the material composition of water and realistic materials from the CT number in the planned image. The profiles of physical dose and LET
fitted function adopted in the conventional method ignores the contribution of the high-LET components, causing an overkill effect. Furthermore, an MC simulation was conducted to determine the material composition of water and realistic materials from the CT number in the planned image. The profiles of physical dose and LET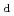 were in good agreement for both techniques. These results indicate the possibility of enhancing the efficiency of retrospective studies of CIRT using MC simulations in the future.
were in good agreement for both techniques. These results indicate the possibility of enhancing the efficiency of retrospective studies of CIRT using MC simulations in the future.
 particle impinging on Al at 230 MeV/u
particle impinging on Al at 230 MeV/u古田 稔将*; 魚住 祐介*; 山口 雄司; 岩元 洋介; 古場 裕介*; Velicheva, E.*; Kalinnikov, V.*; Tsamalaidze, Z.*; Evtoukhovitch, P.*
Journal of Nuclear Science and Technology, 61(2), p.230 - 236, 2024/02
被引用回数:0 パーセンタイル:0.00(Nuclear Science & Technology)230MeV/u 粒子のAl標的入射実験によって
粒子のAl標的入射実験によって 粒子のフラグメンテーション反応による荷電粒子生成の研究を行った。Si検出器と結晶シンチレータからなるカウンターテレスコープを用いて、p, d, t,
粒子のフラグメンテーション反応による荷電粒子生成の研究を行った。Si検出器と結晶シンチレータからなるカウンターテレスコープを用いて、p, d, t,  He、及び
He、及び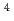 He各粒子の生成二重微分断面積を放出角15
He各粒子の生成二重微分断面積を放出角15 -60
-60 について測定した。取得データをより低い入射エネルギーの測定データと比較し分析した結果、(1)前方角の高エネルギー領域では陽子と中性子の放出スペクトルが類似している、(2)低入射エネルギー実験と同様に
について測定した。取得データをより低い入射エネルギーの測定データと比較し分析した結果、(1)前方角の高エネルギー領域では陽子と中性子の放出スペクトルが類似している、(2)低入射エネルギー実験と同様に 粒子の分解で生じたtと
粒子の分解で生じたtと Heの収量の比は1:2である、(3)
Heの収量の比は1:2である、(3) Heと
Heと 粒子の幅広いピークの分布は入射
粒子の幅広いピークの分布は入射 粒子と標的原子核との衝突過程によって説明できるという一般的な特徴を見出した。
粒子と標的原子核との衝突過程によって説明できるという一般的な特徴を見出した。
古田 琢哉; 古場 裕介*; 橋本 慎太郎; Chang, W.*; 米内 俊祐*; 松本 真之介*; 石川 諒尚*; 佐藤 達彦
Physics in Medicine & Biology, 67(14), p.145002_1 - 145002_15, 2022/07
被引用回数:8 パーセンタイル:68.93(Engineering, Biomedical)炭素線治療は従来の放射線治療よりも腫瘍部への線量集中性に関する優位性を持つが、二次的ながんの発生原因となり得る正常組織への照射を完全に無くすことは困難である。そのため、発がんリスクを照射炭素ビームの核反応によって生成される二次粒子による線量まで含めて評価するには、計算シミュレーション解析が有効となる。本研究では、PHITSコードを中核とした炭素線治療の線量再構築システムを開発した。このシステムでは、治療計画を記録したDICOMデータから自動でPHITSの入力ファイルを作成し、PHITSシミュレーションの実行によって腫瘍および周辺正常組織での線量分布を計算する。PHITSの様々な機能を利用することで、粒子毎の線量寄与や二次粒子の発生場所の特定など、詳細な解析が実施可能である。開発したシステムの妥当性は、水中での線量分布の実験結果や人体等価ファントムへの治療計画との比較により確認した。今後、本システムは量子科学技術研究開発機構において、過去の治療データを用いたシミュレーション解析による遡及的研究に利用される予定である。
Chang, W.*; 古場 裕介*; 古田 琢哉; 米内 俊祐*; 橋本 慎太郎; 松本 真之介*; 佐藤 達彦
Journal of Radiation Research (Internet), 62(5), p.846 - 855, 2021/09
被引用回数:4 パーセンタイル:32.45(Biology)炭素線治療の治療計画をモンテカルロシミュレーションによって再評価するためのツール開発の一環として二つの重要な手法を考案した。一つは治療計画装置に含まれる校正済みのCT-水阻止能表を反映しつつ、患者CT画像から物質識別を行う手法である。もう一つの手法は、粒子およびエネルギー毎に生体物質と水との阻止能比を考慮し、水等価線量を導出することを目的としたものである。これらの手法の有効性を確認するため、生体物質および水で構成される均質および不均質ファントムに対し、SOBPサイズ8cmの炭素線を400MeV/uで照射するシミュレーションをPHITSで計算し、得られた線量深さ分布を従来の治療計画装置による結果と比較した。その結果、従来の治療計画装置で採用されている生体物質を全て水に置換する手法では、異なる物質において二次粒子の発生率が一次粒子の阻止能に単純に比例するため、二次粒子による線量寄与を評価する上で不適切であることが分かった。一方、各物質の二次粒子の発生率を適切に考慮した新しい手法は炭素線治療の再評価において、重要な役割を果たすことが期待できることが分かった。
板敷 祐太朗*; 今林 洋一*; 執行 信寛*; 魚住 祐介*; 佐藤 大樹; 梶本 剛*; 佐波 俊哉*; 古場 裕介*; 松藤 成弘*
Journal of Radiation Protection and Research, 41(4), p.344 - 349, 2016/12
重粒子線治療は、根治性の高さや患者への身体的負担の小さなガン治療法として成果を上げているが、患者には術後の2次発ガンのリスクが伴う。このリスク評価では、体内の放射線挙動や核反応の理解が不可欠となり、放射線輸送計算コードが有用なツールとなる。計算コードの重イオン核反応に対する検証は十分でないため、放射線生成過程の実験データが必要となる。そこで、本研究では、新しいガン治療用のビームとして使用されている核子あたり430MeVの炭素ビームと人体構成物質との核反応から放出される中性子の二重微分断面積の実験データを整備した。実験は、放射線医学総合研究所のHIMAC加速器において実施した。核子当たり430MeVの炭素ビームを45 に傾けた5cm
に傾けた5cm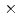 5cm
5cm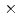 1cmの固体炭素標的に入射し、生成される中性子を15
1cmの固体炭素標的に入射し、生成される中性子を15 , 30
, 30 , 45
, 45 , 60
, 60 , 75
, 75 および90
および90 方向に設置した中性子検出器で測定した。また、中性子の運動エネルギーは飛行時間法により決定した。取得した実験データとPHITSの計算値を比較したところ、PHITSはこのエネルギー領域における炭素からの中性子生成を適切に模擬できることが分かった。
方向に設置した中性子検出器で測定した。また、中性子の運動エネルギーは飛行時間法により決定した。取得した実験データとPHITSの計算値を比較したところ、PHITSはこのエネルギー領域における炭素からの中性子生成を適切に模擬できることが分かった。
佐藤 大樹; 梶本 剛*; 執行 信寛*; 板敷 祐太朗*; 今林 洋一*; 古場 裕介*; 松藤 成弘*; 佐波 俊哉*; 中尾 徳晶*; 魚住 祐介*
Nuclear Instruments and Methods in Physics Research B, 387, p.10 - 19, 2016/11
被引用回数:5 パーセンタイル:39.52(Instruments & Instrumentation)重粒子線治療施設における治療室の合理的な遮蔽設計のためには、患者と重粒子線との核反応で生成される中性子の収量および線量分布を精度よく知る必要がある。本研究では、患者を模擬した水ファントムに治療で用いる核子当たり290MeVおよび430MeVの炭素イオンを入射して、生成される中性子を液体有機シンチレータからなる検出システムを用いて測定した。シンチレータは、ビーム軸に対して15 から90
から90 方向に15
方向に15 おきに配置した。また、測定した中性子生成二重微分収量にAP照射に対する実効線量への換算係数を乗じ、測定における検出下限エネルギーである2MeV以上で積分することで、水ファントム周りの実効線量分布を導出した。得られた実験値は、モンテカルロ計算コードPHITSの計算値と比較した。その結果、PHITSは水ファントムからの中性子収量をよく再現しており、治療室を含めた重粒子線治療施設の線量分布予測において有益な評価手段であることを示した。
おきに配置した。また、測定した中性子生成二重微分収量にAP照射に対する実効線量への換算係数を乗じ、測定における検出下限エネルギーである2MeV以上で積分することで、水ファントム周りの実効線量分布を導出した。得られた実験値は、モンテカルロ計算コードPHITSの計算値と比較した。その結果、PHITSは水ファントムからの中性子収量をよく再現しており、治療室を含めた重粒子線治療施設の線量分布予測において有益な評価手段であることを示した。
梶本 剛*; 橋口 太郎*; 執行 信寛*; 佐藤 大樹; 魚住 祐介*; Song, T. Y.*; Lee, C. W.*; Kim, J. W.*; Yang, S. C.*; 古場 裕介*; et al.
JAEA-Conf 2014-002, p.127 - 132, 2015/02
高エネルギー加速器施設の遮蔽設計には、原子力機構を中心に開発されているPHITSや欧州原子核研究機構を中心に開発されているFLUKAなどのモンテカルロ法に基づく放射線輸送コードが利用されている。これら放射線輸送コードの予測精度を検証するには、核反応の素過程に関する二重微分断面積の実験データとの比較が必要である。しかし、重イオン入射反応に関する実験データは乏しく、荷電粒子生成に関するものはほとんど存在しない。そこで、放射線医学総合研究所のHIMAC加速器を用い290MeV/uのAr入射反応に対する炭素原子核からの陽子、重陽子及び三重陽子生成二重微分断面積を測定した。生成した荷電粒子は、ビーム軸に対して15, 30, 45, 60, 75及び90度方向に配置した液体有機シンチレータで検出した。各荷電粒子は、飛行時間と検出器でのエネルギー損失の情報から識別できる。実験データをPHITS及びFLUKAと比較したところ、陽子生成については実験データの傾向を再現するものの、重陽子及び三重陽子生成については、両コードで全く再現できず、各コードによる計算値の間にも大きな差があることが分かった。これは、既存の核反応模型では重陽子や三重陽子の放出に必要な核子の同伴および癒着過程を適切に取り扱えていないためと考えられる。本研究で得られる知見は、放射線輸送コードにおける核反応模型の改良に貢献することが期待できる。
執行 信寛*; 魚住 祐介*; 今林 洋一*; 板敷 祐太朗*; 佐藤 大樹; 梶本 剛*; 佐波 俊哉*; 古場 裕介*; 高田 真志*; 松藤 成弘*; et al.
JAEA-Conf 2014-002, p.81 - 87, 2015/02
高エネルギー加速器施設の遮蔽設計には、原子力機構を中心に開発されているPHITSや欧州原子核研究機構を中心に開発されているFLUKAなどのモンテカルロ法に基づく放射線輸送コードが利用されている。これら放射線輸送コードの予測精度を検証するには、核反応の素過程に関する二重微分断面積の実験データとの比較が必要である。しかし、重イオン入射反応に関する実験データは乏しく、荷電粒子生成に関するものはほとんど存在しない。そこで、放射線医学総合研究所のHIMAC加速器を用い290MeV/uのAr入射反応に対する炭素原子核からの陽子,重陽子及び三重陽子生成二重微分断面積を測定した。生成した荷電粒子は、ビーム軸に対して15, 30, 45, 60, 75及び90度方向に配置した液体有機シンチレータで検出した。各荷電粒子は、飛行時間と検出器でのエネルギー損失の情報から識別できる。実験データをPHITS及びFLUKAと比較したところ、陽子生成については実験データの傾向を再現するものの、重陽子及び三重陽子生成については、両コードで全く再現できず、各コードによる計算値の間にも大きな差があることが分かった。これは、既存の核反応模型では重陽子や三重陽子の放出に必要な核子の同伴および癒着過程を適切に取り扱えていないためと考えられる。本研究で得られる知見は、放射線輸送コードにおける核反応模型の改良に貢献することが期待できる。
執行 信寛*; 魚住 祐介*; 上原 春彦*; 西澤 知也*; 水野 貴文*; 高宮 大義*; 橋口 太郎*; 佐藤 大樹; 佐波 俊哉*; 古場 裕介*; et al.
Nuclear Data Sheets, 119, p.303 - 306, 2014/05
被引用回数:0 パーセンタイル:0.00(Physics, Nuclear)重粒子線がん治療は、他の放射線治療に比べて正常部位への影響が小さいなどの利点により、近年注目を集めている。この治療では、患者の体内に入射した重イオンによる核反応で、中性子,  線等の二次放射線が生成される。治療施設の放射線安全設計のためには、二次放射線の生成量や角度分布を把握することが重要である。そこで、放射性医学総合研究所HIMAC加速器で、重粒子線がん治療に利用される290MeV/Aと体内での減速を想定した100MeV/Aの炭素ビームを用い、生体を構成する炭素,窒素及び酸素からの中性子生成断面積の実験データを15度から90度の角度領域で取得した。炭素ビームを入射するターゲットは、固体の炭素、アルミニウム化合物(窒化アルミニウム,酸化アルミニウム)及びアルミニウムで構成した。窒素及び酸素の断面積データは、アルミニウム化合物に対するデータから、アルミニウム単体によるデータを差し引き導出した。検出効率をSCINFUL-QMDコードで値づけた液体有機シンチレータ(NE213)を用いて中性子を検出し、運動エネルギーは飛行時間法(TOF)で求めた。取得した実験データと粒子・重イオン輸送計算コードPHITSの計算値との比較から、PHITSの核反応模型の精度を検証し、PHITSの重粒子線がん治療施設における放射線安全設計への応用についても議論する。
線等の二次放射線が生成される。治療施設の放射線安全設計のためには、二次放射線の生成量や角度分布を把握することが重要である。そこで、放射性医学総合研究所HIMAC加速器で、重粒子線がん治療に利用される290MeV/Aと体内での減速を想定した100MeV/Aの炭素ビームを用い、生体を構成する炭素,窒素及び酸素からの中性子生成断面積の実験データを15度から90度の角度領域で取得した。炭素ビームを入射するターゲットは、固体の炭素、アルミニウム化合物(窒化アルミニウム,酸化アルミニウム)及びアルミニウムで構成した。窒素及び酸素の断面積データは、アルミニウム化合物に対するデータから、アルミニウム単体によるデータを差し引き導出した。検出効率をSCINFUL-QMDコードで値づけた液体有機シンチレータ(NE213)を用いて中性子を検出し、運動エネルギーは飛行時間法(TOF)で求めた。取得した実験データと粒子・重イオン輸送計算コードPHITSの計算値との比較から、PHITSの核反応模型の精度を検証し、PHITSの重粒子線がん治療施設における放射線安全設計への応用についても議論する。
執行 信寛*; 魚住 祐介*; 上原 春彦*; 西澤 知也*; 平林 慶一*; 佐藤 大樹; 佐波 俊哉*; 古場 裕介*; 高田 真志*; 松藤 成弘*
Progress in Nuclear Science and Technology (Internet), 4, p.709 - 712, 2014/04
重粒子線治療では、患者体内に入射した重イオンビームによる核反応により、中性子をはじめとする2次放射線が生成される。重粒子線施設における治療室の遮へい設計のためには、患者を線源とした2次中性子の放出エネルギー及び角度分布を精度よく知る必要がある。これまでに測定された実験データは、独国GSIグループによる前方角度領域におけるもののみである。そこでわれわれは、放射線医学総合研究所HIMACにおいて、患者を模擬した水ファントムに治療に用いる290MeV/uの炭素ビームを入射し、15度から90度の広い角度領域で中性子生成量を測定した。水ファントムは厚さ20cmであり、入射炭素イオンはファントム内で完全に停止する。中性子検出器には、液体有機シンチレータNE213を採用し、その検出効率はSCINFUL-QMDコードを用いて求めた。中性子エネルギーは、飛行時間(TOF)法にて決定した。床散乱の寄与を評価するため、水ファントムとシンチレータの間に鉄製のシャドウバーを挿入した測定も行った。データ解析において、荷電粒子及び 線によるイベントを除去することにより、広い放出エネルギー、放出角度における中性子エネルギースペクトルの導出に成功した。また、取得した実験データとPHITSコードによる計算結果との比較を通して、PHITSコードの重粒子線治療施設の遮へい設計への応用についても議論した。
線によるイベントを除去することにより、広い放出エネルギー、放出角度における中性子エネルギースペクトルの導出に成功した。また、取得した実験データとPHITSコードによる計算結果との比較を通して、PHITSコードの重粒子線治療施設の遮へい設計への応用についても議論した。
執行 信寛*; 魚住 祐介*; 上原 春彦*; 西澤 知也*; 水野 貴文*; 佐藤 大樹; 佐波 俊哉*; 古場 裕介*; 高田 真志*; 松藤 成弘*
JAEA-Conf 2013-002, p.137 - 142, 2013/10
重粒子線がん治療では、患者の体内に入射した重イオンによる核反応で中性子や 線等の二次放射線が発生する。これら二次放射線による患部外臓器への線量付与とそれに伴う二次発がんリスクを評価するためには、核反応で生成する放射線の生成断面積データが不可欠となる。平成23年度までに、治療に用いる290MeV/u炭素イオンと生体構成元素である炭素,窒素及び酸素との核反応による中性子生成断面積データを、広い生成エネルギーと角度領域において取得し、粒子・重イオン輸送コードシステムPHITSの核反応模型の精度検証を行った。平成24年度は、人体内で減速した炭素イオンが起こす核反応を調べるため、100MeV/u炭素イオンを炭素ターゲットに入射した際の断面積を測定した。実験は、放射線医学総合研究所HIMAC加速器にて実施した。6台のNE213液体有機シンチレータを、ビーム軸から15
線等の二次放射線が発生する。これら二次放射線による患部外臓器への線量付与とそれに伴う二次発がんリスクを評価するためには、核反応で生成する放射線の生成断面積データが不可欠となる。平成23年度までに、治療に用いる290MeV/u炭素イオンと生体構成元素である炭素,窒素及び酸素との核反応による中性子生成断面積データを、広い生成エネルギーと角度領域において取得し、粒子・重イオン輸送コードシステムPHITSの核反応模型の精度検証を行った。平成24年度は、人体内で減速した炭素イオンが起こす核反応を調べるため、100MeV/u炭素イオンを炭素ターゲットに入射した際の断面積を測定した。実験は、放射線医学総合研究所HIMAC加速器にて実施した。6台のNE213液体有機シンチレータを、ビーム軸から15 , 30
, 30 , 45
, 45 , 60
, 60 , 75
, 75 及び90
及び90 方向に配置し、広い角度領域での測定を可能にした。中性子の運動エネルギーは飛行時間法によって決定し、入射エネルギーから約1MeVまでのエネルギー領域におけるデータ取得に成功した。NE213シンチレータの中性子検出効率は、機構が開発したSCINFUL-QMDコードにより求めている。取得した実験データはPHITSの計算値と比較し、核反応模型では再現の難しい低ネルギー重イオン入射反応の精度を検証した。
方向に配置し、広い角度領域での測定を可能にした。中性子の運動エネルギーは飛行時間法によって決定し、入射エネルギーから約1MeVまでのエネルギー領域におけるデータ取得に成功した。NE213シンチレータの中性子検出効率は、機構が開発したSCINFUL-QMDコードにより求めている。取得した実験データはPHITSの計算値と比較し、核反応模型では再現の難しい低ネルギー重イオン入射反応の精度を検証した。
 線生成断面積の測定
線生成断面積の測定魚住 祐介*; 執行 信寛*; 上原 春彦*; 西沢 知也*; 水野 貴文*; 佐藤 大樹; 佐波 俊哉*; 古場 裕介*; 高田 真志*; 松藤 成弘*; et al.
HIMAC-140, p.234 - 235, 2013/08
平成24年度に放射線医学総合研究所のHIMAC加速器を用いて行った研究の成果について報告する。重粒子線がん治療では、入射重イオンと生体構成元素との核反応から中性子及び 線が、患者体内で生成される。これら放射線による二次発がんリスクの推定には、重イオン核反応における生成断面積データが不可欠である。前年度までの研究により、広いエネルギー領域での断面積測定手法を確立し、治療に供される290MeV/u炭素イオンに対する炭素、窒素及び酸素原子核からの中性子生成断面積データを整備した。平成24年度は、患者体内にて減速した重イオンによる中性子及び
線が、患者体内で生成される。これら放射線による二次発がんリスクの推定には、重イオン核反応における生成断面積データが不可欠である。前年度までの研究により、広いエネルギー領域での断面積測定手法を確立し、治療に供される290MeV/u炭素イオンに対する炭素、窒素及び酸素原子核からの中性子生成断面積データを整備した。平成24年度は、患者体内にて減速した重イオンによる中性子及び 線の生成を調べるため、100MeV/u炭素イオンを炭素及び窒素ターゲットに入射する実験を行った。その結果、15
線の生成を調べるため、100MeV/u炭素イオンを炭素及び窒素ターゲットに入射する実験を行った。その結果、15 から90
から90 までの6角度において、下限エネルギー0.6MeVまでの精度の良い断面積測定に成功した。今後は、本エネルギー領域における実験データの拡充とともに、粒子・重イオン輸送コードシステムPHITSとの比較から、二体衝突近似が成立する下限エネルギーでの理論模型の妥当性について考察する。
までの6角度において、下限エネルギー0.6MeVまでの精度の良い断面積測定に成功した。今後は、本エネルギー領域における実験データの拡充とともに、粒子・重イオン輸送コードシステムPHITSとの比較から、二体衝突近似が成立する下限エネルギーでの理論模型の妥当性について考察する。
魚住 祐介*; 執行 信寛*; 梶本 剛*; 平林 慶一*; 上原 春彦*; 西澤 知也*; 佐藤 大樹; 佐波 俊哉*; 古場 裕介*; 高田 真志*; et al.
HIMAC-138, p.237 - 238, 2012/08
本発表では、平成23年度に放射線医学総合研究所のHIMAC加速器を用いて行った研究の成果について報告する。重粒子線がん治療では、入射重イオンと生体組織を構成する元素との核反応から中性子及び 線が患者体内で生成される。これらの放射線による二次発がんリスクの評価には、重イオン核反応における生成断面積のデータが不可欠である。平成22年度までの研究では、炭素+炭素及び酸素+炭素反応における中性子生成二重微分断面積を測定し、そのデータを公表した。平成23年度は290MeV/u炭素ビームを窒素化合物ターゲットに入射し、炭素+窒素反応における二重微分断面積を測定した。その結果、下限エネルギー0.6MeVまでの中性子断面積データを精度よく導出することに成功した。この成果をもって、所期の技術目標であった低エネルギー領域までの高精度中性子測定手法の確立は達せられた。今後は、確立した手法を用いて、生体構成元素に対する系統的な断面積データを整備する。また、前年度までのデータから
線が患者体内で生成される。これらの放射線による二次発がんリスクの評価には、重イオン核反応における生成断面積のデータが不可欠である。平成22年度までの研究では、炭素+炭素及び酸素+炭素反応における中性子生成二重微分断面積を測定し、そのデータを公表した。平成23年度は290MeV/u炭素ビームを窒素化合物ターゲットに入射し、炭素+窒素反応における二重微分断面積を測定した。その結果、下限エネルギー0.6MeVまでの中性子断面積データを精度よく導出することに成功した。この成果をもって、所期の技術目標であった低エネルギー領域までの高精度中性子測定手法の確立は達せられた。今後は、確立した手法を用いて、生体構成元素に対する系統的な断面積データを整備する。また、前年度までのデータから 線生成二重微分断面積の導出を行った。得られた実験データは、粒子・重イオン輸送コードシステムPHITSの計算結果と比較され、
線生成二重微分断面積の導出を行った。得られた実験データは、粒子・重イオン輸送コードシステムPHITSの計算結果と比較され、 線生成模型の検証・改良に応用される。
線生成模型の検証・改良に応用される。
 線生成断面積の測定
線生成断面積の測定魚住 祐介*; 執行 信寛*; 梶本 剛*; 森口 大輔*; 上山 正彦*; 吉岡 正勝*; 佐藤 大樹; 佐波 俊哉*; 古場 裕介*; 高田 真志*; et al.
HIMAC-136, p.248 - 249, 2011/11
本発表では、平成22年度に放射線医学総合研究所のHIMAC加速器を用いて行った測定について報告する。重粒子線がん治療では、入射重イオンと生体組織を構成する元素との核反応により中性子及び 線が患者の体内にて生成される。これらの放射線による二次発がんリスクの評価には、重イオン核反応における生成二重微分断面積を広いエネルギー範囲で精度よく測定する必要がある。平成21年度は、既存の実験データのある炭素+炭素反応に対して測定を行い、最適な測定条件を検討した。平成22年度は、前年度までの検討を踏まえ、データの存在しない酸素+炭素反応の断面積を測定した。その結果、数百MeV領域から0.6MeVまでの極めて広いエネルギー範囲に渡って精度よく中性子生成二重微分断面積を取得できた。さらに、取得した実験データを利用してPHITSコードの精度検証を行った。PHITSは、前方角度領域において断面積をわずかに過小評価するものの、全体的に実験値をよく再現することがわかった。
線が患者の体内にて生成される。これらの放射線による二次発がんリスクの評価には、重イオン核反応における生成二重微分断面積を広いエネルギー範囲で精度よく測定する必要がある。平成21年度は、既存の実験データのある炭素+炭素反応に対して測定を行い、最適な測定条件を検討した。平成22年度は、前年度までの検討を踏まえ、データの存在しない酸素+炭素反応の断面積を測定した。その結果、数百MeV領域から0.6MeVまでの極めて広いエネルギー範囲に渡って精度よく中性子生成二重微分断面積を取得できた。さらに、取得した実験データを利用してPHITSコードの精度検証を行った。PHITSは、前方角度領域において断面積をわずかに過小評価するものの、全体的に実験値をよく再現することがわかった。
佐藤 大樹; 森口 大輔*; 梶本 剛*; 古場 祐介*; 中村 泰博*; 執行 信寛*; 上山 正彦*; 魚住 祐介*; 吉岡 正勝*; 松藤 成弘*; et al.
Journal of the Korean Physical Society, 59(2), p.1741 - 1744, 2011/08
被引用回数:3 パーセンタイル:26.60(Physics, Multidisciplinary)重イオン相互作用からの中性子生成二重微分断面積に関する既存の実験データは、検出器の検出効率の評価に問題があり断面積を過大評価していることが知られていた。そこで、最新の検出効率計算コードを用いて既存のデータを再解析することにより、過大評価を改善した系統的な断面積データの評価を行った。また、放射線医学総合研究所の重イオン加速器を用いて、新たに中性子生成二重微分断面積を測定した。取得したデータは、既存のデータに比べ測定角度領域が後方角にまで及び検出下限エネルギーも10倍程度低い。両データは、同一核反応の同一角度において非常に良い一致を示した。さらに、各種シミュレーションコードの予測値と比較したところ、いずれのコードも前方角度領域の高エネルギー中性子生成を適切に再現できておらず、重イオン核反応模型の修正が必要であることが示唆された。
佐藤 大樹; 森口 大輔*; 梶本 剛*; 上原 春彦*; 執行 信寛*; 上山 正彦*; 吉岡 正勝*; 魚住 祐介*; 佐波 俊哉*; 古場 裕介*; et al.
Nuclear Instruments and Methods in Physics Research A, 644(1), p.59 - 67, 2011/07
被引用回数:19 パーセンタイル:78.40(Instruments & Instrumentation)重粒子線がん治療の普及に伴い患者体内に入射した重イオンビームの核反応で生成される二次中性子の放射線影響に関心が集まっている。しかし、二次発がんの潜在的なリスク評価のために必要となる重イオンビームと生体構成元素との核反応に関する実験データは整備されておらず、放射線輸送コードの計算精度も十分に検証されていない。そこでわれわれは、放射線医学総合研究所HIMAC加速器を利用し、炭素+炭素反応及び酸素+炭素反応における中性子生成二重微分断面積(DDX)を測定した。論文では、有機シンチレータと飛行時間法を利用した測定手法の詳細を説明し、得られた結果を過去の実験データ及びPHITSコードの計算値と比較することで、測定手法の妥当性や放射線輸送コードの有用性について議論した。実験データは、数百MeVから0.6MeVまでの極めて広いエネルギー領域で精度よく取得されており、PHITSの結果は全エネルギー領域に渡りファクター2以内で実験値を再現した。
魚住 祐介*; 岩元 大樹*; 古場 祐介*; 松藤 成弘*; 佐波 俊哉*; 佐藤 大樹; 執行 信寛*; 高田 真志*; 上山 正彦*; 吉岡 正勝*; et al.
Progress in Nuclear Science and Technology (Internet), 1, p.114 - 117, 2011/02
重イオン治療における二次的発ガンリスクを評価するために、患者の体内に入射した重イオンにより誘起される二次中性子の線量を知ることは極めて重要である。しかし、さまざまな放射線の混合場である患者体内において、高エネルギー中性子の線量を実験的に求めることは難しく、線量評価はシミュレーションコードに頼らざるを得ない。シミュレーションコードにおける重イオンと生体構成元素の核反応計算の精度向上のため、放射線医学総合研究所の重イオン加速器を用いた中性子生成二重微分断面積の測定を計画している。実験に先駆け既存のシミュレーションコードを用い、最適な実験体系を検討した。これにより、重イオンの輸送経路にある空気及びビームダンプからの寄与が大きく、精度の良い断面積データを取得するためには適切な遮蔽が必要であることがわかった。発表では、断面積測定計画の概要及びシミュレーション解析の結果を示す。
岩元 大樹; 今村 稔*; 古場 裕介*; 福井 義則*; 若林 源一郎*; 魚住 祐介*; 金 政浩; 岩元 洋介; 芳原 新也*; 中野 正博*
Physical Review C, 82(3), p.034604_1 - 034604_8, 2010/09
被引用回数:13 パーセンタイル:62.02(Physics, Nuclear)300MeV及び392MeV陽子入射反応におけるO, V, Tb, Ta, Au, Pb及びBiに対する陽子生成二重微分断面積を測定した。放出陽子のエネルギーを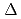
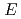 -
-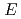 測定法によって積層型シンチレーション検出器を用いて測定した。測定結果を核内カスケードモデル及び量子分子動力学モデルと比較し、両モデルとも二重微分断面積スペクトルをよく再現するが、最前方及び後方で相違が生じることを示した。この相違は核ポテンシャルによる屈折によって説明できることを明らかにした。この知見に基づき、Kalbachの系統式と核内カスケードモデルの1ステップ計算を組合せることによって、角度分布を再現することに成功した。さらに、実験に基づく考察から、核内カスケードモデルの1ステップ計算における準弾性散乱の寄与は、標的核が軽くなるほど、また放出エネルギーが増加するほど大きくなることを示した。
測定法によって積層型シンチレーション検出器を用いて測定した。測定結果を核内カスケードモデル及び量子分子動力学モデルと比較し、両モデルとも二重微分断面積スペクトルをよく再現するが、最前方及び後方で相違が生じることを示した。この相違は核ポテンシャルによる屈折によって説明できることを明らかにした。この知見に基づき、Kalbachの系統式と核内カスケードモデルの1ステップ計算を組合せることによって、角度分布を再現することに成功した。さらに、実験に基づく考察から、核内カスケードモデルの1ステップ計算における準弾性散乱の寄与は、標的核が軽くなるほど、また放出エネルギーが増加するほど大きくなることを示した。
執行 信寛*; 魚住 祐介*; 梶本 剛*; 森口 大輔*; 上山 正彦*; 吉岡 正勝*; 古場 裕介*; 中村 泰博*; 佐藤 大樹; 佐波 俊哉*; et al.
no journal, ,
陽子や重イオンによるがん治療は、腫瘍への線量集中性の高さから注目を集めている。患者に陽子や重イオンを照射すると、患者体内の元素と原子核反応を起こしさまざまなエネルギーの中性子を生成するが、この中性子による患者への影響は十分に考慮されてこなかった。今後、治療の高精度化のためには、中性子に対する線量評価が重要となってくる。本研究では、重イオンがん治療で多く利用されている290MeV/uの炭素イオンを生体構成元素の一つである炭素ターゲットに入射し、原子核反応により生成される中性子の二重微分断面積(DDX)を測定した。実験は、放射線医学総合研究所HIMACにて行った。中性子検出器としてNE213シンチレータを採用し、測定角度は15 , 30
, 30 , 45
, 45 , 60
, 60 , 75
, 75 及び90
及び90 とした。中性子の運動エネルギーは飛行時間法に基づき決定した。データ解析の結果、2.8MeV以上のエネルギーの中性子についてDDXデータを導出することができた。これは既存の実験データの下限エネルギーに比べ約1/5であり、生物学的効果を考察するうえで重要となる低エネルギー領域の中性子をほぼ測定できている。取得したDDXデータは、汎用粒子輸送コードPHITSの計算結果と比較した。両者は全エネルギー領域において良い一致を示した。PHITSは重イオン入射の原子核反応を記述するために量子分子動力学(QMD)モデルを採用しているが、このエネルギー領域におけるQMDモデルの妥当性が確認できた。
とした。中性子の運動エネルギーは飛行時間法に基づき決定した。データ解析の結果、2.8MeV以上のエネルギーの中性子についてDDXデータを導出することができた。これは既存の実験データの下限エネルギーに比べ約1/5であり、生物学的効果を考察するうえで重要となる低エネルギー領域の中性子をほぼ測定できている。取得したDDXデータは、汎用粒子輸送コードPHITSの計算結果と比較した。両者は全エネルギー領域において良い一致を示した。PHITSは重イオン入射の原子核反応を記述するために量子分子動力学(QMD)モデルを採用しているが、このエネルギー領域におけるQMDモデルの妥当性が確認できた。
古場 裕介*; 仲田 佳広*; 松本 真之介*; 赤羽 恵一*; 小野 孝二*; 佐藤 薫; 高橋 史明; 遠藤 章; 島田 義也*; 甲斐 倫明*
no journal, ,
CT撮影は有益な診断法である一方で、撮影に伴う被ばく線量が比較的高い。そのため、被ばく線量の実態の把握に加えて、特に若年層の患者に対する過剰な被ばくを防止することが課題となっている。そのため、原子力機構では、大分県立看護科学大学、放射線医学総合研究所との共同研究において、CT撮影による患者被ばく線量評価システムWAZA-ARIの機能拡張版であるWAZA-ARI v2を開発し、平成27年1月より本格的な運用を開始した。WAZA-ARIv2では、利用者がブラウザ経由の簡単な操作により入力した患者情報(性別、年齢: 0才, 1才, 5才, 10才, 15才, 成人, 肥満度: 小柄, 平均, 大柄, 特大柄)に基づいて、患者体型を詳細に考慮した被ばく線量が正確に計算される。またWAZA-ARIv2では、利用者の協力のもとで撮影条件や被ばく線量を登録・データベース化する機能が付与されている。今回の本格運用開始により、利用者は国内全体の被ばく線量分布と自身が登録した線量を比較することが可能になることから、WAZA-ARIv2はCT撮影時の患者被ばく線量の管理・最適化に大きく寄与すると期待される。本発表では、新たに開発したWAZA-ARIv2のシステムの特徴及び将来の運用計画について報告する。