Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
勝山 千恵*; 梨本 裕晃*; 永翁 一代*; 石橋 朋剛*; 古田 一期*; 木下 剛*; 吉川 英樹; 青木 和弘; 浅野 貴博*; 佐々木 祥人; et al.
FEMS Microbiology Ecology, 86(3), p.532 - 543, 2013/12
被引用回数:15 パーセンタイル:36.67(Microbiology)嫌気性微生物活性は地下環境に影響を与える。本研究では140mの深度の2つのボアホールから低酸素濃度の地下水を採取し脱窒菌とメタン生成菌の活性について調査した。脱窒菌活性は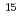 Nをトレーサとしてボアホール環境にて測定し、メタン生成菌については16S rRNAの遺伝子解析により存在を確認した。メタンの安定同位体の分析値から溶存メタンは微生物活用由来であることが分かったが、本メタン生成菌の培養中には発生が確認できなかった。地下140m深の地下水中には酸素が含まれておらず、Ehが-144から6.8mVを示し、脱窒菌の活性が有意な環境であることが分かった。
Nをトレーサとしてボアホール環境にて測定し、メタン生成菌については16S rRNAの遺伝子解析により存在を確認した。メタンの安定同位体の分析値から溶存メタンは微生物活用由来であることが分かったが、本メタン生成菌の培養中には発生が確認できなかった。地下140m深の地下水中には酸素が含まれておらず、Ehが-144から6.8mVを示し、脱窒菌の活性が有意な環境であることが分かった。
 CO
CO and a positron-emitting tracer imaging system
and a positron-emitting tracer imaging system諏訪 竜一*; 石井 里美; 鈴井 伸郎; 石岡 典子; 藤巻 秀; 松橋 信平; 藤田 耕之輔*; 河地 有木
JAEA-Review 2008-055, JAEA Takasaki Annual Report 2007, P. 109, 2008/11
Recently, Kawachi et al. (2006) established a method for the kinetic analysis of  CO
CO for studying photoassimilate transport in a leaf, using PETIS. The method quantitatively analyzes the photoassimilate transport under various light conditions. However, it is important to analyze photoassimilate transport under both dark and light conditions because leaves transport carbon under both these conditions (Mullen et al., 1988). In the present study, we developed a new method to analyze photoassimilate translocation, using PETIS, and
for studying photoassimilate transport in a leaf, using PETIS. The method quantitatively analyzes the photoassimilate transport under various light conditions. However, it is important to analyze photoassimilate transport under both dark and light conditions because leaves transport carbon under both these conditions (Mullen et al., 1988). In the present study, we developed a new method to analyze photoassimilate translocation, using PETIS, and  CO
CO . This novel method clarified the mechanism underlying photoassimilate translocation from a leaf under the dark condition by noninvasive, repeated imaging experiments, using the same specimen.
. This novel method clarified the mechanism underlying photoassimilate translocation from a leaf under the dark condition by noninvasive, repeated imaging experiments, using the same specimen.
 C tracer and coupling between source and sink organs
C tracer and coupling between source and sink organs諏訪 竜一*; 藤巻 秀; 鈴井 伸郎; 河地 有木; 石井 里美; 阪本 浩一*; Nguyen, N. T.*; 実岡 寛文*; Mohapatra, P. K.*; Moghaieb, R. E.*; et al.
Plant Science, 175(3), p.210 - 216, 2008/09
被引用回数:23 パーセンタイル:51.20(Biochemistry & Molecular Biology)Salinity stress affects photosynthate partitioning between sources and sinks of plants, but how it affects on these systems is less understood. Because sources and sinks are closely knitted, any adverse effect under sub-optimal condition on one part is often misinterpreted for the other. Knowledge on regulation of carbon partitioning is indispensable for stress resistance and good plant growth. In the present study, alteration of carbon partitioning in tomato plants (lycopersicon esculentum L. cv. Momotarou) under saline (NaCl) environment was studied by feeding radioactive  C and stable
C and stable 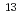 C isotopes. Pulse chases were conducted for measuring spatial and temporal distributions of
C isotopes. Pulse chases were conducted for measuring spatial and temporal distributions of 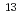 C.
C. 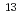 C was measured by standard conventional technique, but
C was measured by standard conventional technique, but  C distribution was monitored using by PETIS. Salt stress resulted in reduced carbon translocation towards roots. Majority of the photosynthate accumulated in the leaf. We have also observed that the reduction in translocation of carbon occurred well before salt stress symptoms of reduced photosynthesis and plant growth in salt exposed plants. The effect on sink activity also showed by decrease in stem diameter and reduced photosynthetic activity. In addition, PETIS analysis of
C distribution was monitored using by PETIS. Salt stress resulted in reduced carbon translocation towards roots. Majority of the photosynthate accumulated in the leaf. We have also observed that the reduction in translocation of carbon occurred well before salt stress symptoms of reduced photosynthesis and plant growth in salt exposed plants. The effect on sink activity also showed by decrease in stem diameter and reduced photosynthetic activity. In addition, PETIS analysis of  C translocation indicates that carbon translocation to roots was inhibited under salt conditions without direct effect of leaf Na accumulation and osmotic stress These results suggest that NaCl has direct effects on plants inhibiting carbon partitioning within few hours of salt solution exposure without inhibition of source activity.
C translocation indicates that carbon translocation to roots was inhibited under salt conditions without direct effect of leaf Na accumulation and osmotic stress These results suggest that NaCl has direct effects on plants inhibiting carbon partitioning within few hours of salt solution exposure without inhibition of source activity.
山崎 千里*; 村上 勝彦*; 藤井 康之*; 佐藤 慶治*; 原田 えりみ*; 武田 淳一*; 谷家 貴之*; 坂手 龍一*; 喜久川 真吾*; 嶋田 誠*; et al.
Nucleic Acids Research, 36(Database), p.D793 - D799, 2008/01
被引用回数:52 パーセンタイル:70.47(Biochemistry & Molecular Biology)ヒトゲノム解析のために、転写産物データベースを構築した。34057個のタンパク質コード領域と、642個のタンパク質をコードしていないRNAを見いだすことができた。
諏訪 竜一*; 石井 里美; 河地 有木; 藤巻 秀; 鈴井 伸郎; 須藤 広行*; 松橋 信平; 藤田 耕之輔*
JAEA-Review 2006-042, JAEA Takasaki Annual Report 2005, P. 123, 2007/02
Carbon is an indispensable nutrition source for crop. Until now, it has been impossible to measure carbon fixation and translocation simultaneously in real time repeatedly in intact plant. Using the technologies of PETIS, we are able to visualize the real time fixation and translocation of carbon in tomato plant. We used  CO
CO to monitor localization of fixed
to monitor localization of fixed  C in leaf.
C in leaf.
諏訪 竜一*; 石井 里美; 鈴井 伸郎; 石岡 典子; 藤巻 秀; 松橋 信平; 河地 有木; 藤田 耕之輔*
no journal, ,
近年、PETIS及び CO
CO を用いた葉における光合成産物の動態解析が行われている。これらの方法を用いることにより、植物体葉におけるさまざまな光条件下での光合成産物の動態のリアルタイム解析が可能となった。葉からの光合成産物の転流は、昼夜いずれでも行われているため、それぞれの条件における転流の様式について解析を進めていく必要がある。そこで本研究では、PETIS及び
を用いた葉における光合成産物の動態解析が行われている。これらの方法を用いることにより、植物体葉におけるさまざまな光条件下での光合成産物の動態のリアルタイム解析が可能となった。葉からの光合成産物の転流は、昼夜いずれでも行われているため、それぞれの条件における転流の様式について解析を進めていく必要がある。そこで本研究では、PETIS及び CO
CO を用い、繰り返し実験による葉における炭素動態のモニタリングから、明条件と暗条件における転流様式の解析を行った。
を用い、繰り返し実験による葉における炭素動態のモニタリングから、明条件と暗条件における転流様式の解析を行った。
勝山 千恵*; 梨本 裕晃*; 石橋 朋剛*; 古田 一期*; 永翁 一代*; 吉川 英樹; 浅野 貴博; 佐々木 祥人; 青木 和弘; 諏訪 裕一*; et al.
no journal, ,
地下圏の微酸素と無酸素境界における地球化学への微生物の寄与を理解するために、安定同位体トレーサー法と遺伝子解析を用いて、北海道幌延町の堆積層における脱窒活性と脱窒細菌群を調べた。換気立坑及び東立坑から採取した地下水サンプルに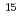 N標識の硝酸態窒素を加え、無酸素もしくは微酸素条件にて培養した。DNA抽出物からドメイン・バクテリアの16S rRNA遺伝子もしくは亜硝酸還元酵素遺伝子(
N標識の硝酸態窒素を加え、無酸素もしくは微酸素条件にて培養した。DNA抽出物からドメイン・バクテリアの16S rRNA遺伝子もしくは亜硝酸還元酵素遺伝子(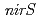 )を対象に微生物相を調べた。脱窒反応は、V140及びE140両方の地下水サンプルにおいて生じた。N
)を対象に微生物相を調べた。脱窒反応は、V140及びE140両方の地下水サンプルにおいて生じた。N ガスを生成するまでの遅延期はV140地下水の方がE140地下水よりも短かった。溶存酸素濃度が約1mg O
ガスを生成するまでの遅延期はV140地下水の方がE140地下水よりも短かった。溶存酸素濃度が約1mg O L
L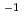 の微酸素条件では地下水サンプルにおける脱窒は検出されなかった。次に、クローニング・シーケンス解析においてほとんどの
の微酸素条件では地下水サンプルにおける脱窒は検出されなかった。次に、クローニング・シーケンス解析においてほとんどの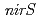 クローンは既知のクローンと高い相同性を示さなかった。
クローンは既知のクローンと高い相同性を示さなかった。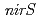 の多様性は、脱窒活性とは対照的にE140の方がV140よりも高かった。2つの立坑は同じ地層の同じ深さに位置するが、原核生物の存在量,脱窒ポテンシャル,
の多様性は、脱窒活性とは対照的にE140の方がV140よりも高かった。2つの立坑は同じ地層の同じ深さに位置するが、原核生物の存在量,脱窒ポテンシャル,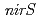 の構成とその酸素に対する応答には空間的不均一性がみられた。
の構成とその酸素に対する応答には空間的不均一性がみられた。