Extractive solubilization, structural change, and functional conversion of cytochrome 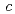 in ionic liquids via crown ether complexation
in ionic liquids via crown ether complexation
クラウンエーテルを用いたイオン液体へのシトクロム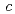 の抽出可溶化,構造変化,機能改変
の抽出可溶化,構造変化,機能改変
下条 晃司郎 

 ; 神谷 典穂*; 谷 文都*; 長縄 弘親
; 神谷 典穂*; 谷 文都*; 長縄 弘親 
 ; 成田 吉徳*; 後藤 雅宏*
; 成田 吉徳*; 後藤 雅宏*
Shimojo, Kojiro; Kamiya, Noriho*; Tani, Fumito*; Naganawa, Hirochika; Naruta, Yoshinori*; Goto, Masahiro*
ヘムタンパク質の1種であるシトクロム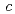 をクラウンエーテルとの錯体形成によってイオン液体中に抽出可能であることを明らかにした。その抽出効率にはイオン液体の疎水性や官能基との相互作用が大きく影響することが示された。一方、イオン液体に溶解したシトクロム
をクラウンエーテルとの錯体形成によってイオン液体中に抽出可能であることを明らかにした。その抽出効率にはイオン液体の疎水性や官能基との相互作用が大きく影響することが示された。一方、イオン液体に溶解したシトクロム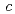 は構造変化を引き起こし、過酸化水素のような基質を取り込みやすくなることが明らかとなった。その結果、本来酵素ではないシトクロム
は構造変化を引き起こし、過酸化水素のような基質を取り込みやすくなることが明らかとなった。その結果、本来酵素ではないシトクロム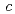 が酵素のようなペルオキシダーゼ活性を持つようになった。
が酵素のようなペルオキシダーゼ活性を持つようになった。
We have found that dicyclohexano-18-crown-6 (DCH18C6) enables transfer of Lys-rich proteins into ionic liquids (ILs) via supramolecular complexation. The hydrophobicity and functional groups of ILs have a great influence on protein partitioning, and a hydroxyl group-containing IL with DCH18C6 is capable of the quantitative partitioning of Cyt-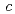 . UV-Vis, CD, and resonance Raman spectroscopic characterizations indicate that the sixth ligand Met 80 in the heme group of the Cyt-
. UV-Vis, CD, and resonance Raman spectroscopic characterizations indicate that the sixth ligand Met 80 in the heme group of the Cyt-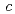 -DCH18C6 complex in IL is replaced by other amino acid residues of the peptide chain, and that a non-natural six-coordinate, low-spin ferric heme structure is induced in IL. Solubilization of Cyt-
-DCH18C6 complex in IL is replaced by other amino acid residues of the peptide chain, and that a non-natural six-coordinate, low-spin ferric heme structure is induced in IL. Solubilization of Cyt-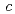 in IL causes the environmental change of the heme vicinity of Cyt-
in IL causes the environmental change of the heme vicinity of Cyt-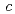 , which triggers the functional conversion of Cyt-
, which triggers the functional conversion of Cyt-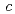 from an electron-transfer protein to peroxidase. The Cyt-
from an electron-transfer protein to peroxidase. The Cyt-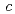 -DCH18C6 complex in IL provides remarkably high peroxidase activity compared with native Cyt-
-DCH18C6 complex in IL provides remarkably high peroxidase activity compared with native Cyt-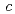 , because of enhancement of the affinity for H
, because of enhancement of the affinity for H O
O .
.