好塩性タンパク質におけるCs 選択性結合部位の発見
選択性結合部位の発見
Discovery of Cs selective binding site on a halophilic protein
selective binding site on a halophilic protein
新井 栄揮; 安達 基泰; 玉田 太郎; 徳永 廣子*; 石橋 松二郎*; 徳永 正雄*; 黒木 良太
Arai, Shigeki; Adachi, Motoyasu; Tamada, Taro; Tokunaga, Hiroko*; Ishibashi, Matsujiro*; Tokunaga, Masao*; Kuroki, Ryota
数多くの金属イオンと相互作用する可能性がある好塩性タンパク質分子を利用して、希少金属・有害金属イオンの結合部位を見出す研究を進めてきた。今回我々は、X線結晶解析により、中度好塩菌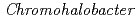 sp.560由来・HaBLAの立体構造を解明するとともに、X線異常分散測定により、HaBLA結晶構造中のCs
sp.560由来・HaBLAの立体構造を解明するとともに、X線異常分散測定により、HaBLA結晶構造中のCs , Sr
, Sr 結合部位の抽出を試みた。Cs
結合部位の抽出を試みた。Cs の同定にはSAGA-LSのBL7、Sr
の同定にはSAGA-LSのBL7、Sr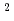 +の同定にはSPring-8のBL38B1およびPFのNW12Aを使用した。本研究の結果、HaBLAの結晶構造中に、Cs
+の同定にはSPring-8のBL38B1およびPFのNW12Aを使用した。本研究の結果、HaBLAの結晶構造中に、Cs に由来する17.5
に由来する17.5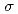 レベル以上、Sr
レベル以上、Sr に由来する7.0
に由来する7.0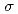 レベル以上の異常分散差フーリエ電子密度を見出し、HaBLA分子上に少なくとも1ヶ所のCs
レベル以上の異常分散差フーリエ電子密度を見出し、HaBLA分子上に少なくとも1ヶ所のCs 結合部位、3ヶ所のSr
結合部位、3ヶ所のSr 結合部位を発見した。特に、今回発見したCs
結合部位を発見した。特に、今回発見したCs 結合部位は、Trp側鎖のベンゼン環によるカチオン-
結合部位は、Trp側鎖のベンゼン環によるカチオン-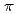 相互作用、および、主鎖の2つの酸素原子によってCs
相互作用、および、主鎖の2つの酸素原子によってCs を結合しており、Na
を結合しており、Na がCs
がCs の9倍量存在する条件下(Na
の9倍量存在する条件下(Na /Cs
/Cs = 90mM/10mM)でもCs
= 90mM/10mM)でもCs を選択的に結合できることが明らかになった。
を選択的に結合できることが明らかになった。
Because various metal ion binding sites exist on halophilic proteins, we proposed that the metal ion binding sites with an affinity to harmful metals and rare metals could be identified using X-ray crystallographic analysis in the presence of those metal ions. In this study, we attempted to identify metal ion binding sites for Sr and Cs
and Cs on a halophilic protein HaBLA derived from
on a halophilic protein HaBLA derived from 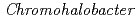 sp.560 (HaBLA) by X-ray crystallographic analysis and anomalous X-ray diffraction analysis. By these analyses, we succeeded in discovering one Cs
sp.560 (HaBLA) by X-ray crystallographic analysis and anomalous X-ray diffraction analysis. By these analyses, we succeeded in discovering one Cs binding site and three Sr
binding site and three Sr binding site for one molecule of HaBLA. Moreover, discovered Cs
binding site for one molecule of HaBLA. Moreover, discovered Cs binding site showed high Cs
binding site showed high Cs selectivity, which binds Cs
selectivity, which binds Cs even in the presence of 9-fold molar excess of Na
even in the presence of 9-fold molar excess of Na (90 mM Na
(90 mM Na / 10 mM Cs
/ 10 mM Cs ).
).