Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
 Pt-labeled platinum complex and evaluation of its biodistribution in healthy mice
Pt-labeled platinum complex and evaluation of its biodistribution in healthy mice面川 真里奈*; 木村 寛之*; 初川 雄一*; 河嶋 秀和*; 塚田 和明; 屋木 祐介*; 内藤 行基*; 安井 裕之*
Bioorganic & Medicinal Chemistry, 97, p.117557_1 - 117557_6, 2024/01
被引用回数:0 パーセンタイル:0.01(Biochemistry & Molecular Biology)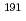 Pt was produced via the (n,2n) reaction induced by accelerator neutrons. [
Pt was produced via the (n,2n) reaction induced by accelerator neutrons. [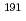 Pt]FGC-Pt was obtained through the accelerator neutron irradiation of FGC-Pt and K
Pt]FGC-Pt was obtained through the accelerator neutron irradiation of FGC-Pt and K PtCl
PtCl . Highly purified [
. Highly purified [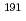 Pt]FGC-Pt was obtained using the latter method, which suggests that the synthetic method using a
Pt]FGC-Pt was obtained using the latter method, which suggests that the synthetic method using a 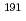 Pt-labeled platinum reagent is suitable for the radioactivation of platinum complexes. We also investigated whether a significant correlation existed between the biodistribution of FGC-Pt and [
Pt-labeled platinum reagent is suitable for the radioactivation of platinum complexes. We also investigated whether a significant correlation existed between the biodistribution of FGC-Pt and [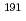 Pt]FGC-Pt in healthy mice 24 h after tail vein administration. These results suggest that
Pt]FGC-Pt in healthy mice 24 h after tail vein administration. These results suggest that 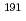 Pt-labeled compounds, synthesized using radioactive platinum reagents, can be used to confirm the biodistribution of platinum compounds. Our study on the biodistribution of [
Pt-labeled compounds, synthesized using radioactive platinum reagents, can be used to confirm the biodistribution of platinum compounds. Our study on the biodistribution of [ Pt]FGC-Pt is expected to contribute to the development of novel platinum-based drugs in the future.
Pt]FGC-Pt is expected to contribute to the development of novel platinum-based drugs in the future.
 Re-labeled antibody (A7) for radioimmunotherapy with rhenium(I) tricarbonyl core as a chelate site
Re-labeled antibody (A7) for radioimmunotherapy with rhenium(I) tricarbonyl core as a chelate site小川 数馬*; 河嶋 秀和*; 絹谷 清剛*; 柴 和弘*; 小野口 昌久*; 木村 寛之*; 橋本 和幸; 小谷 明*; 佐治 英郎*
Annals of Nuclear Medicine, 23(10), p.843 - 848, 2009/12
被引用回数:9 パーセンタイル:31.42(Radiology, Nuclear Medicine & Medical Imaging)レニウム-186及び188は、がんの放射免疫療法に適した物理的性質を有する核種であるにもかかわらず、臨床への応用は十分に検討されていない。これは、抗体(高分子)に標識する方法が複雑であることが問題点としてあげられる。そこで、われわれは、簡便な標識法として、 Re(I)トリカルボニル錯体とモノクローナル抗体(A7)を直接反応させる方法を検討した。その結果、2時間の反応で、収率23%及び28%で
Re(I)トリカルボニル錯体とモノクローナル抗体(A7)を直接反応させる方法を検討した。その結果、2時間の反応で、収率23%及び28%で Re標識抗体が合成できることを確認した。また、精製直後の放射化学的純度は95%以上であった。次に、本
Re標識抗体が合成できることを確認した。また、精製直後の放射化学的純度は95%以上であった。次に、本 Re標識抗体を腫瘍モデルマウスへ投与した結果、投与24時間後において、腫瘍へ集積(13.1, 13.2% Dose/g)すること及び選択的集積性の指標となる腫瘍と血中の放射能濃度比が2以上であることが観察された。以上、レニウムトリカルボニル錯体により抗体(A7)が簡便に標識可能であること、標識体である
Re標識抗体を腫瘍モデルマウスへ投与した結果、投与24時間後において、腫瘍へ集積(13.1, 13.2% Dose/g)すること及び選択的集積性の指標となる腫瘍と血中の放射能濃度比が2以上であることが観察された。以上、レニウムトリカルボニル錯体により抗体(A7)が簡便に標識可能であること、標識体である Re(CO)
Re(CO) -A7は高い安定性を有し、担癌モデル動物において腫瘍への選択的な集積を示すことを明らかにした。今後は、収率を増加させるための標識法の改良が必要である。
-A7は高い安定性を有し、担癌モデル動物において腫瘍への選択的な集積を示すことを明らかにした。今後は、収率を増加させるための標識法の改良が必要である。
 Re-complex-conjugated bisphosphonate for the palliation of metastatic bone pain in an animal model
Re-complex-conjugated bisphosphonate for the palliation of metastatic bone pain in an animal model小川 数馬*; 向 高弘*; 浅野 大悟*; 河嶋 秀和*; 絹谷 清剛*; 柴 和弘*; 橋本 和幸; 森 厚文*; 佐治 英郎*
Journal of Nuclear Medicine, 48(1), p.122 - 127, 2007/01
転移性骨腫瘍の疼痛緩和を目的とした薬剤として、高い安定性を示す Re-MAG3錯体結合ビスホスホネート(
Re-MAG3錯体結合ビスホスホネート( Re-MAG3-HBP)を開発した。この化合物は、従来から検討されている
Re-MAG3-HBP)を開発した。この化合物は、従来から検討されている Re-HEDPに比べて、正常マウスにおいて、骨指向性薬剤として優れた体内分布を示した。
Re-HEDPに比べて、正常マウスにおいて、骨指向性薬剤として優れた体内分布を示した。 Re-MAG3-HBPの治療効果を骨転移モデル動物を用いて評価した。治療効果と副作用を評価するために、腫瘍の大きさと末梢血球数を計測し、骨痛の疼痛緩和は、機械刺激を加えるテスト法により評価した。その結果、
Re-MAG3-HBPの治療効果を骨転移モデル動物を用いて評価した。治療効果と副作用を評価するために、腫瘍の大きさと末梢血球数を計測し、骨痛の疼痛緩和は、機械刺激を加えるテスト法により評価した。その結果、 Re-HEDP投与群においては、腫瘍の大きさは未治療群と同等であった。それに対して、
Re-HEDP投与群においては、腫瘍の大きさは未治療群と同等であった。それに対して、 Re-MAG3-HBP投与群においては、有意に腫瘍増殖は抑制された。さらに、骨転移によって生じる痛みは、
Re-MAG3-HBP投与群においては、有意に腫瘍増殖は抑制された。さらに、骨転移によって生じる痛みは、 Re-MAG3-HBP又は
Re-MAG3-HBP又は Re -HEDPの投与により減弱した。しかも、その効果は、
Re -HEDPの投与により減弱した。しかも、その効果は、 Re-MAG3-HBP投与群の方が強い傾向を示した。これら結果は、
Re-MAG3-HBP投与群の方が強い傾向を示した。これら結果は、 Re-MAG3-HBPが転移性骨腫瘍の疼痛緩和薬剤として有用である可能性を示唆するものである。
Re-MAG3-HBPが転移性骨腫瘍の疼痛緩和薬剤として有用である可能性を示唆するものである。
 Re-labeled bisphosphonate in a rat model of bone metastasis
Re-labeled bisphosphonate in a rat model of bone metastasis小川 数馬*; 向 高弘*; 浅野 大悟*; 河嶋 秀和*; 橋本 和幸; 柴 和弘*; 森 厚文*; 佐治 英郎*
no journal, ,
われわれは、患者のQOL(生活の質)の向上を目指した癌性骨転移の疼痛緩和薬剤として、二官能性放射性医薬品の概念に基づき、安定な Re単核錯体である
Re単核錯体である Re-MAG3(メルカプトトリグリシン)をビスホスホネート骨格を持つ化合物に導入した新規薬剤
Re-MAG3(メルカプトトリグリシン)をビスホスホネート骨格を持つ化合物に導入した新規薬剤 Re-MAG3-HBPを開発し、その特性を調べてきた。本化合物は、従来から検討されている
Re-MAG3-HBPを開発し、その特性を調べてきた。本化合物は、従来から検討されている Re-HEDP(ビスホスホネートの一種)に比べて、高い骨への集積,速い血中クリアランス及び低い胃への集積を示し、癌性骨転移の疼痛緩和薬剤として優れた特性を有していることがわかった。さらに、骨転移がんモデルのラットを用いた実験から、本化合物は、疼痛緩和効果を示すこと及び
Re-HEDP(ビスホスホネートの一種)に比べて、高い骨への集積,速い血中クリアランス及び低い胃への集積を示し、癌性骨転移の疼痛緩和薬剤として優れた特性を有していることがわかった。さらに、骨転移がんモデルのラットを用いた実験から、本化合物は、疼痛緩和効果を示すこと及び Re-HEDPは、腫瘍の増殖を抑える効果は見られなかったのに対して、本化合物は、腫瘍増殖の抑制効果を示すことが明らかになった。以上の結果、
Re-HEDPは、腫瘍の増殖を抑える効果は見られなかったのに対して、本化合物は、腫瘍増殖の抑制効果を示すことが明らかになった。以上の結果、 Re-MAG3-HBPを用いた内部放射線治療は、骨転移がんモデルのラットにおいて有効であり、
Re-MAG3-HBPを用いた内部放射線治療は、骨転移がんモデルのラットにおいて有効であり、 Re-HEDPより優れていることを示した。
Re-HEDPより優れていることを示した。
 Re-labeled antibody (A7) by a simple method using rhenium(I) tricarbonyl complex
Re-labeled antibody (A7) by a simple method using rhenium(I) tricarbonyl complex小川 数馬*; 河嶋 秀和*; 絹谷 清剛*; 吉本 光喜*; 柴 和弘*; 木村 寛之*; 橋本 和幸; 森 厚文*; 佐治 英郎*
no journal, ,
 Reは、優れた核的性質に加え、ジェネレータ核種であるため、RI内部投与治療用として最も有用なRIの一つである。しかしながら、抗体等蛋白質に標識する方法が複雑であることが問題点としてあげられる。そこで、われわれは、簡便な標識法として、
Reは、優れた核的性質に加え、ジェネレータ核種であるため、RI内部投与治療用として最も有用なRIの一つである。しかしながら、抗体等蛋白質に標識する方法が複雑であることが問題点としてあげられる。そこで、われわれは、簡便な標識法として、 Re(I)トリカルボニル錯体とモノクローナル抗体(A7)を直接反応させる方法を検討した。その結果、2時間の反応で、収率27%で
Re(I)トリカルボニル錯体とモノクローナル抗体(A7)を直接反応させる方法を検討した。その結果、2時間の反応で、収率27%で Re標識抗体が合成できることを確認した。また、精製直後の放射化学的純度は98%以上、24時間経過後も約93%が元の化学形を保っており、本
Re標識抗体が合成できることを確認した。また、精製直後の放射化学的純度は98%以上、24時間経過後も約93%が元の化学形を保っており、本 Re標識抗体が安定であることが認められた。さらに、本
Re標識抗体が安定であることが認められた。さらに、本 Re標識抗体を腫瘍モデルマウスへ投与した結果、投与24時間後において、腫瘍へ集積(11.2% Dose/g)すること及び腫瘍と血中の放射能濃度比が1以上であることが観察された。今後は、収率を増加させるための標識法の改良が必要である。
Re標識抗体を腫瘍モデルマウスへ投与した結果、投与24時間後において、腫瘍へ集積(11.2% Dose/g)すること及び腫瘍と血中の放射能濃度比が1以上であることが観察された。今後は、収率を増加させるための標識法の改良が必要である。
 Re)標識ビオチンの作製
Re)標識ビオチンの作製平沢 真*; 河嶋 秀和*; 小川 数馬*; 木村 寛之*; 小野 正博*; 橋本 和幸; 佐治 英郎*
no journal, ,
放射免疫療法では、抗体の血中クリアランスが遅いため、放射能の腫瘍血液比が低くなり、放射線感受性の高い骨髄の被曝量が増すことが問題となっている。そこで、ビオチン-ストレプトアビジン(SA)の特異的結合システムを用いたプレターゲティングの概念による新規RI-DDS治療薬剤の開発を目指し、放射性レニウムをSA化抗体へ効率的に導入するため、 Reトリカルボニル錯体によるヒスチジン化ビオチン(His-biotin)の標識を試みた。
Reトリカルボニル錯体によるヒスチジン化ビオチン(His-biotin)の標識を試みた。 Re-His-biotinは放射化学的収率7.1%、純度90%以上で合成できた。次に、得られた
Re-His-biotinは放射化学的収率7.1%、純度90%以上で合成できた。次に、得られた Re-His-biotinのマウス血漿中での安定性を評価するとともに、SAへの結合性を測定した結果、本標識体は37
Re-His-biotinのマウス血漿中での安定性を評価するとともに、SAへの結合性を測定した結果、本標識体は37 Cの血漿中において、24時間経過後も95%以上が未変化体として存在し、安定であった。また、SAに
Cの血漿中において、24時間経過後も95%以上が未変化体として存在し、安定であった。また、SAに Re-His-biotinを添加したところ、85.4%がSAと結合し、この結合はビオチンを共存させることで98%が阻害された。以上の結果、
Re-His-biotinを添加したところ、85.4%がSAと結合し、この結合はビオチンを共存させることで98%が阻害された。以上の結果、 Re-His-biotinはSA化抗体の標識試薬として有用であることが示唆された。本研究は、文部科学省原子力基礎基盤戦略研究イニシアティブ「先進的ながん診断・治療を実現するRI-DDS開発研究」の成果である。
Re-His-biotinはSA化抗体の標識試薬として有用であることが示唆された。本研究は、文部科学省原子力基礎基盤戦略研究イニシアティブ「先進的ながん診断・治療を実現するRI-DDS開発研究」の成果である。
河嶋 秀和*; 平沢 真*; 木村 寛之*; 小野 正博*; 橋本 和幸; 佐治 英郎*
no journal, ,
RI内用放射線療法による腫瘍の治療において、RI標識抗体は、その腫瘍特異性を利用して腫瘍への放射能送達が期待できるため注目されているが、抗体の血液中からの消失が遅いために骨髄被ばく量が増大することが問題となっている。そこで、骨髄被ばくを低減させる放射性レニウム標識内用放射線治療薬剤の開発を行った。「ストレプトアビジン化抗腫瘍抗体」を投与し、その後血中からの抗体の消失を促進する薬剤を投与し、最後に「ストレプトアビジン化抗腫瘍抗体」に特異的に結合する「放射性レニウム標識ビオチン誘導体」を投与して腫瘍部位への選択的な放射能送達を達成するという、プレターゲティング法を開発し、その有効性を評価した。まず、放射性レニウム標識ビオチン誘導体を新規に設計・合成し、内用放射線治療を行ううえで有用な基本的性質を有していることを明らかにした。そこで、担がんマウスに対して内用放射線治療を行ったところ、非治療群を比較して有意な腫瘍増殖抑制効果が認められた。一方、白血球数と血小板数はいずれも一過性に減少したが、治療開始3週間後には全個体で回復し、重篤な骨髄抑制は確認されず、今回考案した方法の有効性を認めた。