Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
仲庭 哲津子*; 深田 はるみ*; 井上 達矢*; 合田 正貴*; 中井 良子*; 桐井 康行*; 安達 基泰; 玉田 太郎; 瀬川 新一*; 黒木 良太; et al.
Biochemistry, 51(42), p.8410 - 8421, 2012/10
被引用回数:20 パーセンタイル:44.63(Biochemistry & Molecular Biology)タンパク質キナーゼは、さまざまな疾病の治療のための創薬標的タンパク質となっている。C-Jun-N末端キナーゼ1(JNK1)に存在する遊離型システインの機能・安定性・構造への効果を調べるために、そのシステイン残基に系統的に変異導入を実施した。JNK1の3つ及び7つのシステインに変異導入したM3変異体とM7変異体は、大腸菌発現実験において、M0野生型JNK1よりも、それぞれ5及び2倍高く発現した。凝集の時間依存性を分析したSDS-PAGEの結果から、M3とM7は凝集しにくいことが示された。走査型熱量計で熱安定性を評価したところ、M0野生型JNK1, M3変異体及びM7変異体は、いずれも3状態で遷移し、熱変性することが示された。2.6 分解能の結晶構造解析の結果、M3変異体の構造は野生型と同等であった。以上より、(1)最も高く生産され、(2)凝集に対する安定性が改善され、(3)構造も野生型と同等であったM3変異体が、今後JNK1の構造と機能の関係を調べるために最も適した変異体であると結論した。
分解能の結晶構造解析の結果、M3変異体の構造は野生型と同等であった。以上より、(1)最も高く生産され、(2)凝集に対する安定性が改善され、(3)構造も野生型と同等であったM3変異体が、今後JNK1の構造と機能の関係を調べるために最も適した変異体であると結論した。
玉田 太郎; 木下 誉富*; 多田 俊治*; 黒木 良太
日本結晶学会誌, 52(2), p.133 - 138, 2010/04
セリンプロテアーゼの触媒機構を理解することを目的として、ブタ膵臓エラスターゼの高分解能中性子(1.65 resolution)及びX線(0.94
resolution)及びX線(0.94 resolution)構造解析を正四面体型中間体を模倣する阻害剤と複合体の状態で実施した。中性子とX線の両解析結果から、His57とAsp102の間に形成された水素結合は強い水素結合ではあるものの、低障壁水素結合の特徴(水素原子がドナーとアクセプターの中間付近に存在する)は満たしていなかった。また、中性子解析結果から、いわゆるオキシアニオンホールの形成とオキシアニオンホール中に阻害剤由来の酸素原子が酸素陰イオンの状態で存在していることが明瞭に示された。これより、セリンプロテアーゼの触媒機構において正四面体型中間体構造の安定化に対するオキシアニオンホールの役割が明らかになった。
resolution)構造解析を正四面体型中間体を模倣する阻害剤と複合体の状態で実施した。中性子とX線の両解析結果から、His57とAsp102の間に形成された水素結合は強い水素結合ではあるものの、低障壁水素結合の特徴(水素原子がドナーとアクセプターの中間付近に存在する)は満たしていなかった。また、中性子解析結果から、いわゆるオキシアニオンホールの形成とオキシアニオンホール中に阻害剤由来の酸素原子が酸素陰イオンの状態で存在していることが明瞭に示された。これより、セリンプロテアーゼの触媒機構において正四面体型中間体構造の安定化に対するオキシアニオンホールの役割が明らかになった。
玉田 太郎; 木下 誉富*; 栗原 和男; 安達 基泰; 大原 高志; 今井 啓祐*; 黒木 良太; 多田 俊治*
Journal of the American Chemical Society, 131(31), p.11033 - 11040, 2009/07
被引用回数:61 パーセンタイル:79.67(Chemistry, Multidisciplinary)セリンプロテアーゼの触媒機構を理解することを目的として、ブタ膵臓エラスターゼの高分解能中性子及びX線構造解析を正四面体型中間体を模倣する阻害剤と複合体の状態で実施した。同一の大型単結晶を用いた室温における測定の結果、1.65 分解能の中性子回折データ及び1.2
分解能の中性子回折データ及び1.2 分解能のX線回折データを取得した。また、別の結晶を用いて100K下で0.94
分解能のX線回折データを取得した。また、別の結晶を用いて100K下で0.94 分解能のX線回折データも併せて取得した。今回の解析は、セリンプロテアーゼとしてはこれまでで最も高分解能で実施された中性子構造解析例である。中性子とX線の両解析結果から、His57とAsp102の間に形成された水素結合は結合距離が2.60
分解能のX線回折データも併せて取得した。今回の解析は、セリンプロテアーゼとしてはこれまでで最も高分解能で実施された中性子構造解析例である。中性子とX線の両解析結果から、His57とAsp102の間に形成された水素結合は結合距離が2.60 と短く、強い水素結合であると判明したものの、水素原子はHis57に結合していた。この結果は、一説として唱えられている低障壁水素結合の特徴(水素原子がドナーとアクセプターの中間付近に存在する)は満たすものではなく、低障壁水素結合仮説を否定するものであった。また、中性子解析結果から、いわゆるオキシアニオンホールの形成とオキシアニオンホール中に阻害剤由来の酸素原子が酸素陰イオンの状態で存在していることが明瞭に示された。これより、セリンプロテアーゼの触媒機構において正四面体型中間体構造の安定化に対するオキシアニオンホールの役割が明らかになった。
と短く、強い水素結合であると判明したものの、水素原子はHis57に結合していた。この結果は、一説として唱えられている低障壁水素結合の特徴(水素原子がドナーとアクセプターの中間付近に存在する)は満たすものではなく、低障壁水素結合仮説を否定するものであった。また、中性子解析結果から、いわゆるオキシアニオンホールの形成とオキシアニオンホール中に阻害剤由来の酸素原子が酸素陰イオンの状態で存在していることが明瞭に示された。これより、セリンプロテアーゼの触媒機構において正四面体型中間体構造の安定化に対するオキシアニオンホールの役割が明らかになった。
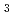 Ni
Ni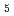 Al
Al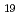
芳賀 芳範; 松田 達磨; 池田 修悟; Galatanu, A.; 松本 拓也*; 杉本 豊成*; 多田 俊治*; 野口 悟*; 大貫 惇睦
Physica B; Condensed Matter, 359-361, p.1006 - 1008, 2005/04
被引用回数:3 パーセンタイル:16.33(Physics, Condensed Matter)新しいウラン化合物U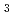 Ni
Ni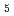 Al
Al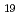 を発見し、単結晶育成に成功した。斜方晶の結晶構造を有し、ウランは結晶学的に2つのサイトを占める。磁化の異方性から、そのうち一つのサイトのウランだけが反強磁性秩序を起こし、もう一つのウランは低温まで常磁性状態にあると考えられる。
を発見し、単結晶育成に成功した。斜方晶の結晶構造を有し、ウランは結晶学的に2つのサイトを占める。磁化の異方性から、そのうち一つのサイトのウランだけが反強磁性秩序を起こし、もう一つのウランは低温まで常磁性状態にあると考えられる。
玉田 太郎; 木下 誉富*; 大原 高志; 栗原 和男; 多田 俊治*; 黒木 良太
no journal, ,
エラスターゼは、立体構造情報を基盤とした創薬手法いわゆるStructure-Based Drug Design(SBDD)研究の代表的な題材として用いられてきたセリンプロテアーゼである。エラスターゼの活性部位に存在する触媒基の状態や阻害剤との相互作用を詳細に解析することは、SBDDにおいて有用な知見を与えると考えられる。そこで、エラスターゼと阻害剤複合体の中性子構造解析を実施した。中性子回折実験から得られた核密度図からその立体構造モデル(全原子座標: 約4,000個、そのうち水素及び重水素原子座標: 約2,000個)を構築し、1.75 分解能において、結晶学的R値: 23.4%まで精密化を終了している。中性子回折実験により得られた核密度図から、活性部位の解離状態や薬物候補化合物との水素結合様式が詳細に明らかになってきた。また、同一結晶から取得した核密度図(中性子)と電子密度図(X線)の差分を取ることにより、各原子の原子散乱長(因子)の特徴を反映したさまざまな情報を得ることができた。
分解能において、結晶学的R値: 23.4%まで精密化を終了している。中性子回折実験により得られた核密度図から、活性部位の解離状態や薬物候補化合物との水素結合様式が詳細に明らかになってきた。また、同一結晶から取得した核密度図(中性子)と電子密度図(X線)の差分を取ることにより、各原子の原子散乱長(因子)の特徴を反映したさまざまな情報を得ることができた。
玉田 太郎; 木下 誉富*; 大原 高志; 栗原 和男; 多田 俊治*; 黒木 良太
no journal, ,
エラスターゼは、立体構造情報を基盤とした創薬手法いわゆるStructure-Based Drug Design(SBDD)研究の代表的な題材として用いられてきたセリンプロテアーゼである。エラスターゼの活性部位に存在する触媒基の状態や阻害剤との相互作用を詳細に解析することは、SBDDにおいて有用な知見を与えると考えられる。そこで、エラスターゼと阻害剤複合体の中性子構造解析を実施した。中性子回折実験から得られた核密度図からその立体構造モデル(全原子座標: 約4,000個、そのうち水素及び重水素原子座標: 約2,000個)を構築した。構築した立体構造は1.75 分解能において、結晶学的R値: 23.4%まで精密化を終了している。中性子回折実験により得られた核密度図から、活性部位の解離状態や薬物候補化合物との水素結合様式が詳細に明らかになってきた。また、同一結晶から取得した核密度図(中性子)と電子密度図(X線)の差分を取ることにより、各原子の原子散乱長(因子)の特徴を反映したさまざまな情報を得ることができた。
分解能において、結晶学的R値: 23.4%まで精密化を終了している。中性子回折実験により得られた核密度図から、活性部位の解離状態や薬物候補化合物との水素結合様式が詳細に明らかになってきた。また、同一結晶から取得した核密度図(中性子)と電子密度図(X線)の差分を取ることにより、各原子の原子散乱長(因子)の特徴を反映したさまざまな情報を得ることができた。
玉田 太郎; 木下 誉富*; 山田 貢; 栗原 和男; 大原 高志; 安達 基泰; 多田 俊治*; 黒木 良太
no journal, ,
エラスターゼは、蛋白質の立体構造に基づく薬物設計(SBDD)研究の代表的な題材として用いられてきたセリンプロテアーゼである。エラスターゼの全原子構造情報取得によってセリンプロテアーゼの触媒機構解明を目指すとともに、SBDD研究に供するため、ブタ膵臓由来のエラスターゼ(PPE)の単独及び阻害剤複合体での中性子結晶構造解析を実施した。中性子回折実験はJRR3に設置された生体高分子用回折計BIX-3において実施し、同一結晶を用いた取得したX線回折データを相補的に用いた構造精密化により高精度の全原子構造情報を取得した。PPE単独(1.9 分解能)、及びエラスターゼの基質を模倣したペプチド様の阻害剤との複合体状態(1.65
分解能)、及びエラスターゼの基質を模倣したペプチド様の阻害剤との複合体状態(1.65 分解能)での中性子構造解析に成功した。今回取得した阻害剤結合前・後の水素原子を含む全原子構造情報は、これまでにセリンプロテアーゼの触媒機構において議論されてきた反応開始時の活性化制御機構や遷移状態における低障壁水素結合の存在や酸素陰イオンホールの形成について重要な知見を与えると同時に、活性部位の水和構造の変化についても重要な知見を与えた。
分解能)での中性子構造解析に成功した。今回取得した阻害剤結合前・後の水素原子を含む全原子構造情報は、これまでにセリンプロテアーゼの触媒機構において議論されてきた反応開始時の活性化制御機構や遷移状態における低障壁水素結合の存在や酸素陰イオンホールの形成について重要な知見を与えると同時に、活性部位の水和構造の変化についても重要な知見を与えた。
玉田 太郎; 木下 誉富*; 栗原 和男; 多田 俊治*; 黒木 良太
no journal, ,
エラスターゼは、蛋白質の立体構造に基づく薬物設計(Structure Based Drug Design: SBDD)研究の代表的な題材として用いられてきたセリンプロテアーゼである。エラスターゼの全原子構造情報取得によってセリンプロテアーゼの触媒機構解明を目指すとともに、SBDD研究に供するため、ブタ膵臓由来のエラスターゼ(PPE)の単独および阻害剤複合体での中性子結晶構造解析を実施した。中性子回折実験はJRR3に設置された生体高分子用回折計BIX-3において実施し、同一結晶を用いて取得したX線回折データを相補的に用いた構造精密化により高精度の全原子構造情報を取得した。PPE単独(1.9 分解能)、およびエラスターゼの基質を模倣したペプチド様の阻害剤との複合体状態(1.65
分解能)、およびエラスターゼの基質を模倣したペプチド様の阻害剤との複合体状態(1.65 分解能)での中性子構造解析に成功した。今回取得した阻害剤結合前・後の水素原子を含む全原子構造情報は、これまでにセリンプロテアーゼの触媒機構において議論されてきた反応開始時の活性化制御機構や遷移状態における低障壁水素結合の存在や酸素陰イオンホールの形成について重要な知見を与えると同時に、活性部位の水和構造の変化についても重要な知見を与えた。
分解能)での中性子構造解析に成功した。今回取得した阻害剤結合前・後の水素原子を含む全原子構造情報は、これまでにセリンプロテアーゼの触媒機構において議論されてきた反応開始時の活性化制御機構や遷移状態における低障壁水素結合の存在や酸素陰イオンホールの形成について重要な知見を与えると同時に、活性部位の水和構造の変化についても重要な知見を与えた。
玉田 太郎; 木下 誉富*; 大原 高志; 栗原 和男; 今井 啓介*; 黒木 良太; 多田 俊治*
no journal, ,
エラスターゼは、立体構造情報を基盤とした創薬手法(Structure-Based Drug Design: SBDD)研究の代表的な題材として用いられてきたセリンプロテアーゼである。しかしながら、X線結晶構造に基づいた多くのSBDD研究の実施にもかかわらず、特異性の高い阻害剤の作製が困難であるのが現状である。よって、エラスターゼの全原子構造情報の取得を目指して、エラスターゼとその阻害剤(FR130180)の中性子結晶構造解析を実施した。試料にはブタ膵臓由来のエラスターゼ(Porcine Pancreatic Elastase: PPE)を用い、FR130180との複合体結晶を作製した。取得した結晶はマクロシーディング法を繰り返すことにより3mm 程度まで成長させた後、JRR3に設置した生体高分子用中性子回折計BIX3で回折実験を行い、1.65
程度まで成長させた後、JRR3に設置した生体高分子用中性子回折計BIX3で回折実験を行い、1.65 分解能の回折データを収集した。中性子とX線回折データを組合せた精密化により、約2000個の水素及び重水素原子を含むPPEとFR130180の複合体構造を決定した。今回用いた阻害剤FR130180は、エラスターゼの基質を模倣したペプチド様の構造を持っており、PPEとFR130180複合体はセリンプロテアーゼの反応中間体状態を示していると考えられ、セリンプロテアーゼの触媒機構の理解を深めることができた。また、阻害剤とPPE間に、興味深い相互作用の形成も確認され、特異性の高い阻害剤設計に有用な構造情報を取得することができた。
分解能の回折データを収集した。中性子とX線回折データを組合せた精密化により、約2000個の水素及び重水素原子を含むPPEとFR130180の複合体構造を決定した。今回用いた阻害剤FR130180は、エラスターゼの基質を模倣したペプチド様の構造を持っており、PPEとFR130180複合体はセリンプロテアーゼの反応中間体状態を示していると考えられ、セリンプロテアーゼの触媒機構の理解を深めることができた。また、阻害剤とPPE間に、興味深い相互作用の形成も確認され、特異性の高い阻害剤設計に有用な構造情報を取得することができた。
玉田 太郎; 木下 誉富*; 栗原 和男; 安達 基泰; 大原 高志; 多田 俊治*; 黒木 良太
no journal, ,
セリンプロテアーゼの触媒機構を理解することを目的として、ブタ膵臓エラスターゼの高分解能中性子及びX線構造解析を正四面体型中間体を模倣する阻害剤と複合体の状態で実施した。同一の大型単結晶を用いた室温における測定の結果、1.65 分解能の中性子回折データ及び1.20
分解能の中性子回折データ及び1.20 分解能のX線回折データを取得した。また、別の結晶を用いて100K下で0.94
分解能のX線回折データを取得した。また、別の結晶を用いて100K下で0.94 分解能のX線回折データも併せて取得した。今回の解析は、セリンプロテアーゼとしてはこれまでで最も高分解能で実施された中性子構造解析例である。中性子とX線の両解析結果からHis57とAsp102の間に形成された水素結合は結合距離が2.60
分解能のX線回折データも併せて取得した。今回の解析は、セリンプロテアーゼとしてはこれまでで最も高分解能で実施された中性子構造解析例である。中性子とX線の両解析結果からHis57とAsp102の間に形成された水素結合は結合距離が2.60 と短く、強い水素結合であると判明したものの、水素原子はHis57に結合してしていた。この結果は、一説として唱えられている低障壁水素結合の特徴(水素原子がドナーとアクセプターの中間付近に存在する)は満たすものではなく、低障壁水素結合仮説を否定するものであった。また、中性子解析結果から、いわゆるオキシアニオンホールの形成とオキシアニオンホール中に阻害剤由来の酸素原子が酸素陰イオンの状態で存在していることが明瞭に示された。これより、セリンプロテアーゼの触媒機構において正四面体型中間体構造の安定化に対するオキシアニオンホールの役割が明らかになった。
と短く、強い水素結合であると判明したものの、水素原子はHis57に結合してしていた。この結果は、一説として唱えられている低障壁水素結合の特徴(水素原子がドナーとアクセプターの中間付近に存在する)は満たすものではなく、低障壁水素結合仮説を否定するものであった。また、中性子解析結果から、いわゆるオキシアニオンホールの形成とオキシアニオンホール中に阻害剤由来の酸素原子が酸素陰イオンの状態で存在していることが明瞭に示された。これより、セリンプロテアーゼの触媒機構において正四面体型中間体構造の安定化に対するオキシアニオンホールの役割が明らかになった。
玉田 太郎; 木下 誉富*; 黒木 良太; 多田 俊治*
no journal, ,
エラスターゼは、古くから構造情報を基盤とした創薬手法いわゆるStructure-Based Drug Design(SBDD)研究が盛んに行われているセリンプロテアーゼである。したがってエラスターゼの活性部位に存在する触媒基の解離状態を調べることは、SBDDによる創薬に重要な知見を与えると考えられる。そこで、エラスターゼの活性部位の詳細な構造を水素原子の情報を含めて詳細に明らかにするために、超高分解能X線及び中性子構造解析に着手した。結晶化試料はブタ由来のエラスターゼを用い、薬物候補化合物との複合体結晶を作成した。X線回折実験はSPring-8 BL41XUで行い、約0.3mm角の結晶を用いて100Kにて測定した。一方、中性子回折実験は日本原子力研究開発機構の研究用原子炉(JRR3)にある中性子回折計(BIX3)で行い、重水溶液に浸漬させた1.5 1.3
1.3 0.9mmの結晶を用いて室温で実施した。X線では0.94
0.9mmの結晶を用いて室温で実施した。X線では0.94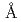 分解能で、Rmerge=7.5%, completeness=99%、中性子では2.4
分解能で、Rmerge=7.5%, completeness=99%、中性子では2.4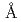 分解能で、Rmerge=13%, completeness=83%の回折データを収集できた。X線回折データから得られた電子密度では、蛋白質の炭素に結合する水素原子の位置が明瞭に確認できた。また、中性子回折データから得られた核密度では、活性残基であるヒスチジン残基(His-57)のプロトン化の状態が明らかになった。
分解能で、Rmerge=13%, completeness=83%の回折データを収集できた。X線回折データから得られた電子密度では、蛋白質の炭素に結合する水素原子の位置が明瞭に確認できた。また、中性子回折データから得られた核密度では、活性残基であるヒスチジン残基(His-57)のプロトン化の状態が明らかになった。
仲庭 哲津子*; 深田 はるみ*; 井上 達矢*; 木下 誉富*; 安達 基泰; 玉田 太郎; 黒木 良太; 多田 俊治*
no journal, ,
JNK1はストレス応答性のMAPキナーゼである。本研究はJNK1と阻害剤との複合体の構造をX線及び中性子回折法により超高分解能で決定し、構造情報に基づいた創薬法の新たな展開を図るものである。JNK1には構造内部に4か所と表面に3か所のCys残基があり、これらが酸化的条件下において失活や凝集を引き起こす原因となり、安定した巨大な結晶を作ることが困難であると考えられる。これまで本研究ではCysを変異したJNK1変異体を2種調製し、そのうち分子表面3か所のCysを変異させることで構造安定性を保持したまま大量発現が可能なM3を見いだした。しかし2種の変異体の構造解析より、両者ともに格子定数が100 以上、分解能2.7
以上、分解能2.7 程度と中性子回折に不適当であった。そこで既に報告されているJNK1アイソザイムの結晶系は中性子回折の条件を満たしていたことから、変異体との結晶パッキングの比較を行った。アイソザイムは変異型に比べて分子間の塩橋や水素結合が多いことがわかった。本発表ではアイソザイムのみで形成している相互作用2か所に注目し、それらをM3に導入した変異体のパッキング変化について報告する。
程度と中性子回折に不適当であった。そこで既に報告されているJNK1アイソザイムの結晶系は中性子回折の条件を満たしていたことから、変異体との結晶パッキングの比較を行った。アイソザイムは変異型に比べて分子間の塩橋や水素結合が多いことがわかった。本発表ではアイソザイムのみで形成している相互作用2か所に注目し、それらをM3に導入した変異体のパッキング変化について報告する。
玉田 太郎; 木下 誉富*; 多田 俊治*; 栗原 和男; 大原 高志; 黒木 良太
no journal, ,
エラスターゼは、古くから構造情報を基盤とした創薬手法いわゆるStructure-Based Drug Design (SBDD)研究が盛んに行われているセリンプロテアーゼである。したがってエラスターゼの活性部位に存在する触媒基の解離状態を調べることは、SBDDによる創薬に重要な知見を与えると考えられる。そこで、エラスターゼの活性部位の詳細な構造を水素原子の情報を含めて詳細に明らかにするために、中性子構造解析を実施した。結晶化試料はブタ由来のエラスターゼを用い、薬物候補化合物との複合体結晶を作成した。取得した結晶はマクロシーディング法を繰り返すことにより3mm 程度まで成長させた後に回折実験に供した。中性子回折実験は日本原子力研究開発機構の研究用原子炉(JRR3)にある中性子回折計(BIX3)で行い、重水溶液に浸漬させた結晶を用いて室温で実施した。1.75
程度まで成長させた後に回折実験に供した。中性子回折実験は日本原子力研究開発機構の研究用原子炉(JRR3)にある中性子回折計(BIX3)で行い、重水溶液に浸漬させた結晶を用いて室温で実施した。1.75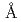 分解能で
分解能で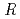
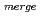 =9.5%, completeness=92%の回折データを収集した。得られた核密度から、全原子の半分に相当する約1,700個の水素及び重水素原子を同定し、活性残基であるヒスチジン残基(His45)のプロトン化の状態が明らかになった。
=9.5%, completeness=92%の回折データを収集した。得られた核密度から、全原子の半分に相当する約1,700個の水素及び重水素原子を同定し、活性残基であるヒスチジン残基(His45)のプロトン化の状態が明らかになった。