Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
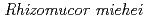 の微弱酵素活性の除去
の微弱酵素活性の除去酒井 和哉*; 小林 弘幸*; 清水 仁聡*; 大島 章夫*; 加藤 重昭*; 佐藤 勝也; 鳴海 一成
JAEA-Review 2008-055, JAEA Takasaki Annual Report 2007, P. 85, 2008/11
接合菌の一種である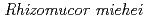 が菌体外に分泌する凝乳酵素(乳蛋白質の特定部分を分解するプロテアーゼの一種)はチーズ製造に広く使用されている。しかし、
が菌体外に分泌する凝乳酵素(乳蛋白質の特定部分を分解するプロテアーゼの一種)はチーズ製造に広く使用されている。しかし、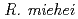 は凝乳酵素を大量に生産する一方で異なる部位を分解するプロテアーゼ,油脂分解酵素のリパーゼ、及びアミラーゼなどチーズ製造には好ましくない少量の酵素を生産する。本研究では、イオンビームを用いた突然変異育種によって、このような夾雑酵素活性がない変異株を作出することである。オリーブ油を加えた寒天培地上に形成されるハロウを指標に、2株のリパーゼ低生産変異株を選抜した。得られた2株について、単胞子分離を行い安定した低生産性変異株の確立を試みたが、不安定な生産性を示すのみであった。一方、炭素イオンビーム照射により凝乳活性低下変異株を分離した。凝乳活性低下の原因を明らかにするため、液体培養後の菌体内と菌体外の酵素活性を比較したところ、生産株及び凝乳活性低下変異株ともに、菌体内1に対し菌体外5の比であり、菌体外への酵素の分泌には異常がないことがわかった。
は凝乳酵素を大量に生産する一方で異なる部位を分解するプロテアーゼ,油脂分解酵素のリパーゼ、及びアミラーゼなどチーズ製造には好ましくない少量の酵素を生産する。本研究では、イオンビームを用いた突然変異育種によって、このような夾雑酵素活性がない変異株を作出することである。オリーブ油を加えた寒天培地上に形成されるハロウを指標に、2株のリパーゼ低生産変異株を選抜した。得られた2株について、単胞子分離を行い安定した低生産性変異株の確立を試みたが、不安定な生産性を示すのみであった。一方、炭素イオンビーム照射により凝乳活性低下変異株を分離した。凝乳活性低下の原因を明らかにするため、液体培養後の菌体内と菌体外の酵素活性を比較したところ、生産株及び凝乳活性低下変異株ともに、菌体内1に対し菌体外5の比であり、菌体外への酵素の分泌には異常がないことがわかった。
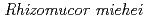 by heavy ion beam irradiation
by heavy ion beam irradiation酒井 和哉*; 小林 弘幸*; 大島 章夫*; 加藤 重昭*; 佐藤 勝也; 鳴海 一成
JAEA-Review 2007-060, JAEA Takasaki Annual Report 2006, P. 95, 2008/03
レンネットは乳蛋白に作用して乳の凝固を引き起こす酵素であり、仔牛や子羊などの胃粘膜に含まれるキモシンに加えて、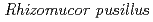 や
や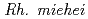 由来の凝乳活性を示す酵素や、遺伝子工学を応用した組換えキモシンも使用されている。しかし、
由来の凝乳活性を示す酵素や、遺伝子工学を応用した組換えキモシンも使用されている。しかし、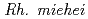 は凝乳酵素とともに、チーズに好ましくない風味を生じさせるリパーゼも夾雑酵素として生産するため低pH処理等で夾雑活性を低下させる処理が必要になる。したがって、リパーゼ活性がない、又は非常に低い変異株の育種が望まれる。今回、イオンビーム照射した菌株からはリパーゼ活性生産能力を失った変異株は見つからなかった。しかし、リパーゼ活性が低下したと思われる変異株は見つかっており、培養を経時的に観察して活性低下の確認を進めている。一方、リパーゼ活性や凝乳活性が向上したと思われる変異株も分離された。
は凝乳酵素とともに、チーズに好ましくない風味を生じさせるリパーゼも夾雑酵素として生産するため低pH処理等で夾雑活性を低下させる処理が必要になる。したがって、リパーゼ活性がない、又は非常に低い変異株の育種が望まれる。今回、イオンビーム照射した菌株からはリパーゼ活性生産能力を失った変異株は見つからなかった。しかし、リパーゼ活性が低下したと思われる変異株は見つかっており、培養を経時的に観察して活性低下の確認を進めている。一方、リパーゼ活性や凝乳活性が向上したと思われる変異株も分離された。
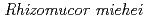 by irradiation of heavy-ion beam
by irradiation of heavy-ion beam酒井 和哉*; 小林 弘幸*; 大島 章夫*; 加藤 重昭*; 佐藤 勝也; 長谷 純宏; 鳴海 一成; 坂下 哲哉; 小林 泰彦
JAEA-Review 2006-042, JAEA Takasaki Annual Report 2005, P. 97, 2007/02
カビの一種である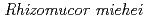 は、チーズ製造に広く用いられる微生物レンネットとも呼ばれる特異性が高いプロテアーゼの生産に用いられる。しかし、目的のプロテアーゼを生産するほかにもさまざまな酵素を少量生産し、微小な活性の混入がチーズのフレーバーや味など品質に好ましくない影響を与える。発酵液から夾雑活性を除去するために塩析やクロマトグラフィーを用いることは実際的に不可能であり、また化学的処理では主活性の低下も避けられないので、夾雑活性の生産能力を失った変異株を分離して、夾雑活性を含まない培養液を得ることが望ましい。凝乳酵素を生産する
は、チーズ製造に広く用いられる微生物レンネットとも呼ばれる特異性が高いプロテアーゼの生産に用いられる。しかし、目的のプロテアーゼを生産するほかにもさまざまな酵素を少量生産し、微小な活性の混入がチーズのフレーバーや味など品質に好ましくない影響を与える。発酵液から夾雑活性を除去するために塩析やクロマトグラフィーを用いることは実際的に不可能であり、また化学的処理では主活性の低下も避けられないので、夾雑活性の生産能力を失った変異株を分離して、夾雑活性を含まない培養液を得ることが望ましい。凝乳酵素を生産する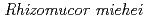 の胞子に以下の重イオンビームを照射し、ビーム種と胞子の生存率・変異率との関係を調べ、最適な照射条件を決定した。今後、決定した条件で胞子にビームを照射し、変異を起こした胞子を培養して、凝乳酵素の活性が低下せずリパーゼ,アミラーゼ活性などが検出されない変異株を検索する。
の胞子に以下の重イオンビームを照射し、ビーム種と胞子の生存率・変異率との関係を調べ、最適な照射条件を決定した。今後、決定した条件で胞子にビームを照射し、変異を起こした胞子を培養して、凝乳酵素の活性が低下せずリパーゼ,アミラーゼ活性などが検出されない変異株を検索する。
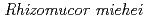 の育種
の育種坂下 哲哉; 小林 泰彦; 佐藤 勝也; 長谷 純宏; 鳴海 一成; 酒井 和哉*; 大島 章夫*; 加藤 重昭*
no journal, ,
微生物由来の凝乳酵素には、夾雑酵素としてリパーゼやアミラーゼが含まれ、チーズの風味などに悪影響を及ぼす。そのため、夾雑活性のないあるいは非常に低い変異体を育種することを目的として、チーズ生産菌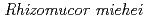 の分生胞子に各種イオンビームを照射して、突然変異体を取得するのに最適な線量を調査し、突然変異体選抜のための条件検討を行った。その結果、100Gyから200Gyが最適線量であると考えられた。また、凝乳活性を損なわず、夾雑酵素であるリパーゼとアミラーゼ活性が欠損した変異体を選抜するために有効な寒天培地を作成し、照射菌体の酵素活性検出法として有効であることを確認した。
の分生胞子に各種イオンビームを照射して、突然変異体を取得するのに最適な線量を調査し、突然変異体選抜のための条件検討を行った。その結果、100Gyから200Gyが最適線量であると考えられた。また、凝乳活性を損なわず、夾雑酵素であるリパーゼとアミラーゼ活性が欠損した変異体を選抜するために有効な寒天培地を作成し、照射菌体の酵素活性検出法として有効であることを確認した。
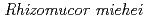 の微弱酵素活性の除去; 変異株のスクリーニング
の微弱酵素活性の除去; 変異株のスクリーニング酒井 和哉*; 大島 章夫*; 加藤 重昭*; 佐藤 勝也; 鳴海 一成
no journal, ,
レンネットは乳蛋白に作用して乳の凝固を引き起こす酵素であり、仔牛や子羊などの第4胃粘膜に含まれるキモシンに加えて、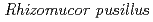 や
や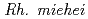 由来の凝乳活性を示す酵素や、遺伝子工学を応用した組換えキモシンも使用されている。しかし、
由来の凝乳活性を示す酵素や、遺伝子工学を応用した組換えキモシンも使用されている。しかし、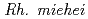 は凝乳酵素とともに、チーズに好ましくない風味を生じさせるリパーゼも夾雑酵素として生産するため低pH処理等で夾雑活性を低下させる処理が必要になる。したがって、リパーゼ活性がない、又は非常に低い変異株の育種が望まれる。今回、イオンビーム照射した菌株からはリパーゼ活性生産能力を失った変異株は見つからなかった。しかし、リパーゼ活性が低下したと思われる変異株は見つかっており、培養を経時的に観察して活性低下の確認を進めている。一方、リパーゼ活性や凝乳活性が向上したと思われる変異株も分離された。
は凝乳酵素とともに、チーズに好ましくない風味を生じさせるリパーゼも夾雑酵素として生産するため低pH処理等で夾雑活性を低下させる処理が必要になる。したがって、リパーゼ活性がない、又は非常に低い変異株の育種が望まれる。今回、イオンビーム照射した菌株からはリパーゼ活性生産能力を失った変異株は見つからなかった。しかし、リパーゼ活性が低下したと思われる変異株は見つかっており、培養を経時的に観察して活性低下の確認を進めている。一方、リパーゼ活性や凝乳活性が向上したと思われる変異株も分離された。