Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
池部 仁善; 梅澤 公二*; 肥後 順一*
Biophysical Reviews, 8(1), p.45 - 62, 2016/03
Molecular dynamics (MD) simulations with both of all-atom and explicit solvent models provide the detailed behavior of protein-partner substrate binding at the atomic level. As the power of computational resources rise, MD simulations are being used more widely and easily. However it is still difficult to investigate thermodynamic properties of protein-partner substrate binding as well as protein folding with conventional MD simulations. Enhanced sampling methods have been developed to sample conformations reflecting equilibrium conditions in a more efficient manner than conventional MD simulations allowing the construction of accurate free energy landscapes. In this review, we discuss these enhanced sampling methods using a series of case by case examples. In particular we review enhanced sampling methods conforming to trivial trajectory parallelization (TTP), virtual-system coupled McMD (V-McMD), and adaptive lambda square dynamics (ALSD). These methods have been recently developed based on the existing method of multicanonical MD (McMD) simulation. Their applications are reviewed with an emphasis on describing their practical implementation. In our concluding remarks we explore extensions of the enhanced sampling methods that may allow for even more efficient sampling.
池部 仁善; 桜庭 俊*; 河野 秀俊
PLOS Computational Biology, 12(3), p.e1004788_1 - e1004788_13, 2016/03
被引用回数:45 パーセンタイル:90.91(Biochemical Research Methods)Acetylation of lysine residues in histone tails is associated with gene transcription. Because histone tails are structurally flexible and intrinsically disordered, it is difficult to experimentally determine the tail conformations and the impact of acetylation. In this work, we performed simulations to sample H3 tail conformations with and without acetylation. The results show that irrespective of the presence or absence of the acetylation, the H3 tail remains in contact with the DNA and assumes an alpha-helix structure in some regions. Acetylation slightly weakened the interaction between the tail and DNA and enhanced alpha-helix formation, resulting in a more compact tail conformation. We inferred that this compaction induces unwrapping and exposure of the linker DNA, enabling DNA-binding proteins (e.g., transcription factors) to bind to their target sequences. In addition, our simulation also showed that acetylated lysine was more often exposed to the solvent, which is consistent with the fact that acetylation functions as a post-translational modification recognition site marker.
池部 仁善; 櫻庭 俊; 河野 秀俊
Journal of Computational Chemistry, 35(1), p.39 - 50, 2014/01
被引用回数:14 パーセンタイル:42.33(Chemistry, Multidisciplinary)A novel, efficient sampling method for biomolecules is proposed. The partial McMD was recently developed as a method that improved generalized ensemble (GE) methods to focus sampling only on a part of a system (GEPS); however, it was not tested well. We found that partial McMD did not work well for poly-lysine decapeptide and gave significantly worse sampling efficiency than a conventional GE. Herein, we elucidate the fundamental reason for this and propose a novel GEPS, adaptive lambda square dynamics (ALSD), which can resolve the problem faced when using partial McMD. We demonstrate that ALSD greatly increases the sampling efficiency over a conventional GE. We believe that ALSD is an effective method and is applicable to the conformational sampling of larger and more complicated biomolecule systems.
池部 仁善
no journal, ,
真核生物のDNAはクロマチン構造を形成することで核内にコンパクトに収納されているが、DNA機能発現の際にはこの構造は一時的に解きほぐされる。この構造の解体と再形成のメカニズムは、DNA機能制御において重要であり、クロマチンを構成する要素の一つであるヒストンテイルへの官能基修飾によりコントロールされることが知られている。本研究は、ヒストンテイルの一種であるH3ヒストンテイルの状態を、partial McMDと呼ばれるシミュレーション手法を用いて明らかにし、このメカニズムの解明に挑戦する。今回の発表では、ヒストンテイルの生物学的重要性、partial McMDという計算手法について簡単に説明した後、partial McMDという計算方法が持つ問題点について言及する。
池部 仁善; 河野 秀俊
no journal, ,
ヌクレオソームのヒストンテイル領域は、クロマチン構造の形成や、ヒストンテイルへの官能基修飾によってDNA機能が制御されるヒストンコード仮説などに深くかかわっていることが知られており、生物学的に重要である。これらの現象のメカニズムを解明するには、ヌクレオソームコア粒子(Nucleosome Core Particle: NCP)と違って特定の安定構造を持たないと考えられる、ヒストンテイルの動態を詳細に調べる必要がある。分子動力学シミュレーションは、このような構造的揺らぎの大きい生体分子の構造変化を原子レベルで解析できる優れた手法であるが、従来の手法では計算資源の問題等から、ヌクレオソームから切り離されたヒストンテイル断片のシミュレーション研究しか行われていなかった。そこで本研究では、われわれが新たに開発した、高い効率でヒストンテイルの安定構造を探索できるadaptive 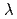 dynamicsという手法を用いて、ヒストンテイル周辺のNCPと溶媒水分子をあらわに計算に取り入れたシミュレーションを行う。本発表では、本計算の途中経過について発表する。
dynamicsという手法を用いて、ヒストンテイル周辺のNCPと溶媒水分子をあらわに計算に取り入れたシミュレーションを行う。本発表では、本計算の途中経過について発表する。
池部 仁善
no journal, ,
Free energy landscapes of biomolecules provide valuable information on how the molecule behaves and obtaining them is one of the most important objectives in biology. Multicanonical molecular dynamics (MD) simulation is a powerful technique developed to efficiently investigate the landscape. However, we need still a more efficient method to obtain a reliable ensemble for a larger and more complicate biomolecule system. To this end, Okumura developed partial McMD that enhances the sampling only for partial energy term. The focused sampling will reduce the space to be sampled and increase the sampling efficiency. However, we found that partial McMD can have a less sampling efficiency than McMD in a system for a poly-lysine decapeptide. In this seminar, we address the fundamental reason and report that a new simulation method, adaptive lambda square dynamics (ALSD), which can resolve the problem occurring when using partial McMD, greatly increased the sampling efficiency over McMD.
池部 仁善
no journal, ,
Free energy landscapes of biomolecules provide valuable information on how the molecule behaves and obtaining them is one of the most important objectives in biology. Multicanonical molecular dynamics (MD) simulation is a powerful technique developed to efficiently investigate the landscape. However, we need still a more efficient method to obtain a reliable ensemble for a larger and more complicate biomolecule system. To this end, Okumura developed partial McMD that enhances the sampling only for partial energy term. The focused sampling will reduce the space to be sampled and increase the sampling efficiency. However, we found that partial McMD can have a less sampling efficiency than McMD in a system for a poly-lysine decapeptide. In this seminar, we address the fundamental reason and report that a new simulation method, adaptive lambda square dynamics (ALSD), which can resolve the problem occurring when using partial McMD, greatly increased the sampling efficiency over McMD.
河野 秀俊; 米谷 佳晃; 池部 仁善; 櫻庭 俊; 石田 恒
no journal, ,
Eukaryotic Genome is stored in a nucleus in the form of chromatin. Along with DNA binding proteins, this chromatin structure plays a key role in gene regulation. The chromatin has the fundamental structural unit called nucleosome which is composed of two copies of histones H2A, H2B, H3 and H4 and DNA wrapped around the histone proteins almost twice. Transcription does not occur until nucleosome is unwrapped to expose DNA, which can then be recognized by regulatory proteins. To understand this unwrapping process, MD simulations were performed on two nucleosomes: the canonical H3 and the H3 variant called CENP-A, essential for the kinetochore assembly. In the talk, how these nucleosomes are different in free energy profiles and what causes the differences are discussed.
池部 仁善; 櫻庭 俊; 河野 秀俊
no journal, ,
A novel, efficient sampling method for biomolecules is proposed. The partial multicanonical molecular dynamics (partial McMD) was recently developed as a generalized ensemble (GE) method to focus sampling only on a part of a system (GEPS); however, it was not tested well. We found that partial McMD did not work well for poly-lysine decapeptide and gave significantly worse sampling efficiency than a conventional GE. Herein, we elucidate the fundamental reason for this and propose a novel GEPS, adaptive lambda square dynamics (ALSD), which can resolve the problem faced when using partial McMD. We demonstrate that ALSD greatly increases the sampling efficiency over a conventional GE.
池部 仁善; 櫻庭 俊; 河野 秀俊
no journal, ,
A novel, efficient sampling method for biomolecules is proposed. The partial Multicanonical Molecular Dynamics (partial McMD, Okumura (2008)) simulation was recently developed as an improved generalized ensemble (GE) methods to focus sampling only on a part of a system (GEPS); he expected that the focused sampling reduced the energy space to be sampled and concomitantly increased the efficiency of the conformational sampling. However, the partial McMD has not been tested well except for an alanine dipeptide system. We found that partial McMD did not work well for poly-lysine decapeptide and gave significantly worse sampling efficiency than a conventional GE. Herein, we elucidate the fundamental reason for this and propose a novel GEPS, adaptive lambda square dynamics (ALSD), which can resolve the problem faced when using partial McMD. We demonstrate that ALSD greatly increases the sampling efficiency of the peptide conformation over a conventional GE by scaling of a partial potential energy: electrostatic, van der Waals, and torsion energies relevant to the peptide. We believe that ALSD is an effective method and is applicable to the conformational sampling of larger and more complicated biomolecule systems. Furthermore, ALSD can be available for conformational sampling of biomolecules with intrinsically disordered regions.
池部 仁善; 櫻庭 俊; 河野 秀俊
no journal, ,
ヒトをはじめとする全ての真核生物では、DNAはヒストンと呼ばれるタンパク質との複合体(ヌクレオソーム)として存在し、DNAの機能発現はヌクレオソームの凝集体(クロマチン)の形成と解体によって調節されることが知られている。近年では、ヒストン蛋白質の末端領域であるヒストンテール(テール)への化学修飾が、このクロマチンの状態変化を引き起こしていると考えられている。このメカニズムの詳細を知るには、化学修飾の有無によるテールの状態変化について正しく理解する必要があるが、従来の実験的手法では、特定の立体構造を持たないタンパク質領域(IDR)であるテールの詳細な構造情報を得ることが難しかった。そこで本研究では、我々が新たに開発した構造探索用計算手法であるALSDシミュレーションにより、ヌクレオソーム上のテールの構造探索を行い、その描像を明らかにした。IDRの一種であるテールは自由に動き回るランダム鎖のようなものだと考えられがちだが、正電荷を持つリジン,アルギニン残基を多く持ち、負電荷を持つDNAのリン酸骨格と強く静電相互作用するため、水中に向かって伸びた様な構造はほとんどとらないことが明らかとなった。また、化学修飾のターゲットとなるリジンはアルギニンと比べてヌクレオソーム表面に露出する確率が高いことから、クロマチン形成時において、強い負電荷を持つヌクレオソーム同士を凝集させる役割を果たしていることが示唆された。
池部 仁善; 櫻庭 俊; 河野 秀俊
no journal, ,
真核生物のDNAはクロマチン構造を形成することで核内にコンパクトに収納されているが、DNA機能発現の際にはこの構造は一時的に解きほぐされる。この構造の解体と再形成のメカニズムはDNA機能制御において重要であり、クロマチンを構成する要素の一つであるヒストンテールへの化学修飾によりコントロールされることが知られている。しかし天然変性蛋白領域(Intrinsically Disordered Region: IDR)であるテールの構造を実験的に調査することは難しく、これまでそのメカニズムの詳細は明らかとなっていなかった。このメカニズムを解明するための第一段階として、我々はまず化学修飾なしのテールの状態を明らかにすべく、全原子モデルを用いたシミュレーションを行っている。我々は当初、partial McMDと呼ばれるシミュレーション手法を用いて計算を行っていたが、その計算の過程で本手法が抱える問題点を発見した。前回の発表ではpartial McMDの問題点とその原因について発表を行った。今回の発表では、partial McMDが抱える問題点を解決すべく我々が新たに開発した計算手法、Adaptive Lambda Square Dynamics(ALSD)法について紹介し、本手法を用いたH3ヒストンテールの構造探索計算の結果を発表する。
 ヒストンテールの構造とダイナミクス
ヒストンテールの構造とダイナミクス河野 秀俊; 池部 仁善
no journal, ,
ヒストンテールは化学修飾のターゲットであり、エピゲノムのマーカーとしての重要性から多くの研究がなされている。立体構造の観点からヒストンテールを見ると、モノヌクレソームのX線結晶構造解析では結晶中での構造多形のため、構造を決定することができない。本研究では、計算機シミュレーションにより、ヌクレオソーム構造下でのヒストンテールの構造を探った。ヒストンテールは、正電荷をもつリジン,アルギニン残基を多く持つため、負電荷を持つDNAのリン酸骨格と強い静電相互作用で貼りつく。そのため、数 秒の分子動力学計算ではテールがとり得る構造を網羅的にサンプリングすることができない。そこで、我々は高効率に構造をサンプリングすることができる計算方法を開発し、ヌクレオソーム下でのテールの構造を求めている。現在までのサンプリング結果では、H
秒の分子動力学計算ではテールがとり得る構造を網羅的にサンプリングすることができない。そこで、我々は高効率に構造をサンプリングすることができる計算方法を開発し、ヌクレオソーム下でのテールの構造を求めている。現在までのサンプリング結果では、H テールはほぼ常時リン酸骨格の表面に接触した状態にあり(水中に向かって伸びている構造は室温ではほとんどとらない)、構造アンサンブルの大半は特定の二次構造を持っていないが一部ヘリックス構造をとっていることがわかった。
テールはほぼ常時リン酸骨格の表面に接触した状態にあり(水中に向かって伸びている構造は室温ではほとんどとらない)、構造アンサンブルの大半は特定の二次構造を持っていないが一部ヘリックス構造をとっていることがわかった。
河野 秀俊; 池部 仁善
no journal, ,
ヒストンテールは、化学修飾を受けエピゲノムのマーカーとして働くことから多くの研究がなされているが、ヒストンテールは天然変性領域であり、構造面からの研究はあまり進んでいない。ヒストンテールは、正電荷をもつリジン、アルギニン残基を多く持つため、負電荷を持つDNAのリン酸骨格と強い静電相互作用でDNAに貼りつき、数 秒のシミュレーション計算を行っても、網羅的に構造をサンプリングすることができない。そこで、我々は高効率にサンプリングする計算方法を開発し、H3ヒストンテールの構造分布を解析した。結果、テールは天然変性状態ではあるが、構造分布に偏りがあり、ほぼ常時リン酸骨格の表面に接触した状態にあることがわかった。また、構造アンサンブル中のDNAコンタクト率や埋没度の解析から、リジンはアルギニンに比べてDNAコンタクト率が低く水中に露出している確率が高いことがわかった。このようなアミノ酸残基の構造アンサンブルの違いが、多くの場合、リジンがエピゲノムマーカーとして機能している所以であると推察される。
秒のシミュレーション計算を行っても、網羅的に構造をサンプリングすることができない。そこで、我々は高効率にサンプリングする計算方法を開発し、H3ヒストンテールの構造分布を解析した。結果、テールは天然変性状態ではあるが、構造分布に偏りがあり、ほぼ常時リン酸骨格の表面に接触した状態にあることがわかった。また、構造アンサンブル中のDNAコンタクト率や埋没度の解析から、リジンはアルギニンに比べてDNAコンタクト率が低く水中に露出している確率が高いことがわかった。このようなアミノ酸残基の構造アンサンブルの違いが、多くの場合、リジンがエピゲノムマーカーとして機能している所以であると推察される。
池部 仁善; 櫻庭 俊; 河野 秀俊
no journal, ,
A nucleosome, 146 or 147 base-pair DNA wrapped around a histone octamer composed of two copies of each H3, H4, H2A, and H2B histone proteins, is a compact unit structure to store eukaryotic DNA into the cell nucleus. Although the X-ray conformations of the core region have been already determined, the conformations of the disordered histone terminal regions (histone tails) remain poorly understood. Recent experimental evidences suggest that chemical modifications on the histone tails regulate DNA functions, such as transcription, duplication, and splicing. To understand the regulation mechanism, it is necessary to elucidate difference between conformational states of unmodified and modified histone tails. Thus, we applied adaptive lambda square dynamics (ALSD) simulation we developed recently to investigate the conformations of H3 histone tails. ALSD dynamically scales the simulation parameters (charge, van der Walls and torsion energies) only for the histone tails during the simulations. This successfully sampled various histone tail conformations. In this poster, we introduce the ALSD simulation results and the differences in conformational ensembles between unmodified and acetylated H3 histone tails.
池部 仁善; 櫻庭 俊; 河野 秀俊
no journal, ,
多数の正電荷アミノ酸(リジンとアルギニン)を含むヒストンテールは、クロマチン形成において、DNA由来の強い負電荷を持つヌクレオソーム同士の凝集を仲介することが知られている。また、ヒストンテールは化学修飾のターゲットでもあり、エピゲノムのマーカーとしての重要性から多くの研究がなされている。数ある化学修飾の中でも、リジン残基のアセチル化は転写を活性化する代表的なマーカーとして知られる。リジンの正電荷を中性化するアセチル化修飾は、DNAとヒストンテール間の引力相互作用を減少させる。その結果クロマチンの凝集が緩み、転写因子がDNAに結合できるようになることで転写が活性化される、という転写制御メカニズムが提唱されているが、その詳細は未だ明らかになっていない。そこで我々は、我々が新たに開発した、ヒストンテールのとりうる立体構造を効率的に探索する分子動力学シミュレーション手法、adaptive lambda square dynamics (ALSD)法によって、2パターンのH3ヒストンテール系[(1)修飾無しの系、(2)14残基目のリジンがアセチル化(K14Ac)された系]がどのような立体構造集団を形成するのかを明らかにした。本発表では、2つの構造集団の比較から、ヒストンテールのアセチル化がその立体構造に与える影響について紹介する。
池部 仁善; 櫻庭 俊; 河野 秀俊
no journal, ,
多数の正電荷アミノ酸(リジンとアルギニン)を含むヒストンテールは、クロマチン形成において、DNA由来の強い負電荷を持つヌクレオソーム同士の凝集を仲介することが知られている。また、ヒストンテールは化学修飾のターゲットでもあり、エピゲノムのマーカーとしての重要性から多くの研究がなされている。数ある化学修飾 の中でも、リジン残基のアセチル化は転写を活性化する代表的なマーカーとして知られる。リジンの正電荷を中性 化するアセチル化修飾は、DNAとヒストンテール間の引力相互作用を減少させ、その結果クロマチンの凝集が緩み、転写因子がDNAに結合できるようになることで転写が活性化される、という転写制御メカニズムが提唱されているが、その詳細は未だ明らかになっていない。そこで我々は、新たに開発した、ヒストンテールのとりうる立体構造を効率的に探索する分子動力学シミュレーション手法、adaptive lambda square dynamics (ALSD)法 によって、2パターンのH3ヒストンテール系(1: 修飾無しの系、2: 14残基目のリジンがアセチル化(K14Ac)された系)がどのような立体構造集団を形成するのかを明らかにした。本発表では、2つの構造集団の比較から、ヒストン テールのアセチル化がその立体構造に与える影響について紹介する。
池部 仁善; 桜庭 俊*; 河野 秀俊
no journal, ,
In eukaryotic cells, genome DNA forms nucleosomes composed of DNA wrapped around a histone octamer: two copies of H3, H4, H2A, and H2B histone proteins, and it is compactly stored in the nucleus. The nucleosomes fold into a higher order aggregate, called as chromatin. Although the highly condensed chromatin packing disturbs access of transcriptional factors to DNA, transcription is systematically regulated in vivo. Probably, acetylation will direct dissociation of the tails from DNA, which will result in allowing DNA-binding proteins to access DNA. However, the detailed mechanism has not yet been verified because the conformational information of histone tails is difficult to obtain experimentally and is missing. To elucidate the information, we performed conformational sampling for H3 histone tails with and without acetylation. The results showed that whether acetylated or not, the tails were almost always located nearby DNA and would not dissociate from DNA contrary to the conventional view. The acetylation slightly weakens interactions between the tail and DNA and enhances the alpha-helix formation. We infer that the tail compaction caused by the alpha-helix formation induces unwrapping of DNA at entry and exit regions more and increases the chance of DNA-binding proteins bind to DNA. The results give a new view of how acetylation affects chromatin conformation.
河野 秀俊; 池部 仁善; 桜庭 俊*; 石田 恒
no journal, ,
Dynamics of the nucleosome and accessibility of nucleosomal DNA play critical roles in many nuclear processes. Nucleosomes themselves are highly dynamic and the nucleosomal DNA is spontaneously unwrapped to make it accessible to various DNA-binding proteins. Histone variants are known for each of histone proteins and are supposed to have different roles in the regulation of nuclear processes. In addition, post-translational modifications of histones have been known to affect the regulation, but it is still unknown how they affect changes of the structure and dynamics of chromatin. Through computer simulations, we are investigating the following topics to understand the dynamics of nucleosomes: (1) how much it costs for unwrapping nucleosomal DNA from the histone core, (2) how different the dynamics are among nucleosomes composed of histone variants and (3) how acetylation of histone tails impacts on nucleosome structures. Our simulations suggest that the cost for unwrapping 1bp of DNA from histone core is 0.1 to 0.4 kcal/mol and it changes according to nucleosome types. In the dissociation of nucleosomal DNA, asymmetric unwrapping (unwrapping either end of DNA) became remarkable when the DNA unwrapping reached the inner turn, probably because DNA-DNA repulsion disappeared at this stage, thereby histone-DNA interactions were stabilized. Acetylation of K14 of H3 tail enhanced the DNA flexibility.
池部 仁善; 桜庭 俊*; 河野 秀俊
no journal, ,
In eukaryotic cells, genome DNA is stored in a complex with histone proteins (H3, H4, H2A and H2B). Acetylation to terminal regions of histones (histone tails) is generally believed to regulate gene expression through dissociation of tails from DNA, although conformations of disordered tails remain poorly understood. In this work, we examined differences in conformational ensembles of H3 tail with or without K14 acetylation using adaptive lambda square dynamics simulation. The result suggested that the acetylation does not make the tail dissociate from DNA. Instead, it enhanced secondary structure formation of the tail and unwrapping of DNA from the structured histone core regions. This study elucidated the first step of the gene regulation mechanism.