Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
山本 和喜; 熊田 博明; 中井 啓*; 遠藤 聖*; 山本 哲哉*; 松村 明*
Proceedings of 11th World Congress on Neutron Capture Therapy (ISNCT-11) (CD-ROM), 14 Pages, 2004/10
放射線治療上、細胞密度分布を考慮した線量分布が要求されている。次世代ホウ素中性子捕捉療法(BNCT)用線量評価システムの開発に向けて、照射領域を決定するための新しい方法を提案する。医療画像を用いては腫瘍細胞の拡散浸潤度を十分に評価することはできない。そのためBNCTの治療プロトコールを参考に、腫瘍を囲む照射領域はガドリニウムを用いた核磁気共鳴画像(MRI)のT1画像上に強調される領域から通常2cm余裕を見た任意の距離に拡張する領域として設定されている。この研究では、照射領域境界の細胞濃度を時間-空間球座標系の腫瘍細胞拡散モデルによって議論し、BNCT照射後に生存する腫瘍細胞密度分布を仮想脳ファントムのための2領域拡散モデルによって予測した。
熊田 博明; 山本 和喜; 鳥居 義也; 松村 明*; 山本 哲哉*; 能勢 忠男*; 中川 義信*; 影治 照喜*; 内山 順三
JAERI-Tech 2003-002, 49 Pages, 2003/03
JRR-4に整備した中性子ビーム設備によって、熱外中性子ビームを用いたホウ素中性子捕捉療法(BNCT)を実施することが可能となった。熱外中性子ビームBNCTの実施に必要な治療計画を作成するためには、患者への吸収線量を事前に評価することが不可欠である。患者頭部内の線量分布を数値シミュレーションによって評価し、治療計画作成を支援するBNCT線量評価システム(JCDS)の開発を行った。JCDSは、医療画像であるCT,MRIデータをもとに患者の頭部モデルを作成し、頭部内の中性子及び 線の線束分布をモンテカルロ・コードMCNPで計算するための入力データを自動作成して線量計算を行い、この計算結果を医療画像上に表示させることのできるソフトウェアである。JCDSの特徴として、(1)CTデータとMRIデータの両方を取り扱うことにより、患者の正確な頭部モデルを簡便に作成する機能,(2)日本で実施されている開頭手術を伴ったBNCTに対応し、頭部モデルの形状を編集する機能,(3)計算によって導かれた照射位置に患者を正確にセッティングするための情報を出力する機能などを有している。本報告は、JCDSの基本設計と各処理機能、及びJCDSの計算性能を検証した結果について記述したものである。
線の線束分布をモンテカルロ・コードMCNPで計算するための入力データを自動作成して線量計算を行い、この計算結果を医療画像上に表示させることのできるソフトウェアである。JCDSの特徴として、(1)CTデータとMRIデータの両方を取り扱うことにより、患者の正確な頭部モデルを簡便に作成する機能,(2)日本で実施されている開頭手術を伴ったBNCTに対応し、頭部モデルの形状を編集する機能,(3)計算によって導かれた照射位置に患者を正確にセッティングするための情報を出力する機能などを有している。本報告は、JCDSの基本設計と各処理機能、及びJCDSの計算性能を検証した結果について記述したものである。
熊田 博明; 鳥居 義也
JAERI-Data/Code 2002-018, 158 Pages, 2002/09
熱外中性子ビームを使ったホウ素中性子捕捉療法(Boron Neutron Capture Therapy: BNCT)は、脳内の深部にある悪性脳腫瘍の治療に効果があると期待されている。この熱外中性子を用いたBNCTを実施するためには、患者への照射線量を事前に評価することが不可欠である。これを踏まえ、頭部内の線量分布を計算によって求めるBNCT線量評価システム(JCDS)の開発を行った。JCDSは、医療画像であるCT,MRIデータを基に患者の頭部モデルを作成し、頭部内の中性子及び 線の線束分布をモンテカルロ・コード:MCNPで計算するための入力データを自動作成して線量計算を行うソフトウェアである。さらにMCNPで計算した結果を再び読込み、線量分布を表示させるものである。JCDSの特徴として、(1)CTデータとMRIデータの両方を取り扱うことにより、患者の正確な頭部モデルを簡便に作成する機能,(2)日本で実施されている開頭手術を伴ったBNCTに対応し、頭部モデルの形状を編集する機能,(3)計算によって導かれた照射位置に患者を正確にセッティングするための情報を出力する機能などを有している。本報告書は、JCDS(Ver.1.0)の基本設計と線量評価手順,操作方法と各処理のデータ構造,ライブライリー構造等について記述したものである。
線の線束分布をモンテカルロ・コード:MCNPで計算するための入力データを自動作成して線量計算を行うソフトウェアである。さらにMCNPで計算した結果を再び読込み、線量分布を表示させるものである。JCDSの特徴として、(1)CTデータとMRIデータの両方を取り扱うことにより、患者の正確な頭部モデルを簡便に作成する機能,(2)日本で実施されている開頭手術を伴ったBNCTに対応し、頭部モデルの形状を編集する機能,(3)計算によって導かれた照射位置に患者を正確にセッティングするための情報を出力する機能などを有している。本報告書は、JCDS(Ver.1.0)の基本設計と線量評価手順,操作方法と各処理のデータ構造,ライブライリー構造等について記述したものである。
松村 明*; 山本 哲哉*; 柴田 靖*; 中井 敬*; Zhang, T.*; 松下 明*; 高野 晋吾*; 遠藤 聖*; 阿久津 博義*; 山本 和喜; et al.
Research and Development in Neutron Capture Therapy, p.1073 - 1078, 2002/09
原研のJRR-4の中性子ビーム設備を使って、1999年から2002にかけて9例の患者に対して熱-熱外混合ビームによる術中ホウ素中性子捕捉療法(IO-BNCT)を実施した。グリオブラストーマの生存中央値は、9.8カ月であり星細胞腫は、16.8カ月であった。熱-熱外混合ビームによる術中BNCTは、従来の治療法に比べ初期の放射線効果は良好であった。これらのフェーズI/IIの臨床試験は局所の腫瘍コントロールで有効でした。今後、IO-BNCTの有効性を証明するするため、革新的な手法を伴った臨床試験を継続して実施していくものである。これまで実施した臨床試験の結果を紹介するとともに、今後の展望について記述する。
中井 敬*; 松村 明*; 山本 哲哉*; 柴田 靖*; Zhang, T.*; 阿久津 博義*; 松田 真秀*; 松下 明*; 安田 貢*; 高野 晋吾*; et al.
Research and Development in Neutron Capture Therapy, p.1135 - 1138, 2002/09
原研JRR-4を使って、悪性グリオーマの患者15例に対してホウ素中性子捕捉療法が行われた。このうち2002年4月までに筑波大学が実施した7例の患者について事後の経過を観察し、その結果を報告する。MRIを使った検証では、1例の術野内の再発がみられ、2例の術野外での再発がみられた。また、1例において照射によるネクローシスがみられた。
遠藤 聖*; 松村 明*; 山本 哲哉*; 能勢 忠男*; 山本 和喜; 熊田 博明; 岸 敏明; 鳥居 義也; 樫村 隆則*; 大竹 真一*
Research and Development in Neutron Capture Therapy, p.425 - 430, 2002/09
光造形技術を用いて、患者頭部の造形モデルとして写実的なファントムを製作した。この実体ファントムは将来的に線量計画システムの検証に寄与するものである。しかし、外科手術後の脳及び熱中性子遮へい材のモデル化に含まれる困難性のため、線量評価システム(JCDS:JAERI Computational Dosimetry System)を用いた計算,実体ファントム及びin vivo測定(医療照射)との間では十分な一致が見られなかった。幾つか課題があるものの、実体ファントムを用いた実験的シミュレーション技術は、術中BNCTに対してより確実な線量計画のための有効なツールである。
 NCT trial
NCT trialZhang, T.*; 松村 明*; 山本 哲哉*; 吉田 文代*; 桜井 良憲*; 熊田 博明; 山本 和喜; 能勢 忠男*
Research and Development in Neutron Capture Therapy, p.819 - 824, 2002/09
本研究はホウ素とガドリニウムを組み合わせた中性子捕捉療法を前提に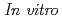 照射実験を行い、ガドリニウム濃度に依存して、ホウ素の照射効果がさまざま変化することを見いだした。この相乗効果の特徴は、ガドリニウムが低濃度の場合、ホウ素の殺細胞効果とガドリニウムの殺細胞効果とに相乗的な効果が現れ、ガドリニウムの濃度を高めていくとホウ素濃度に対する相乗効果が弱くなり、最終的にホウ素濃度に依存しないようになる。臨床照射に置き換えると、腫瘍中内のガドリニウムとボロンの適した濃度比が治療効果を高め、過剰なガドリニウム濃度は負の治療的効果を引き起こす可能性がある。
照射実験を行い、ガドリニウム濃度に依存して、ホウ素の照射効果がさまざま変化することを見いだした。この相乗効果の特徴は、ガドリニウムが低濃度の場合、ホウ素の殺細胞効果とガドリニウムの殺細胞効果とに相乗的な効果が現れ、ガドリニウムの濃度を高めていくとホウ素濃度に対する相乗効果が弱くなり、最終的にホウ素濃度に依存しないようになる。臨床照射に置き換えると、腫瘍中内のガドリニウムとボロンの適した濃度比が治療効果を高め、過剰なガドリニウム濃度は負の治療的効果を引き起こす可能性がある。
中川 義信*; Pooh, K. H.*; 影治 照喜*; 宇山 慎一*; 古林 徹*; 桜井 良憲*; 松村 明*; 山本 哲哉*; 熊田 博明
Research and Development in Neutron Capture Therapy, p.1113 - 1116, 2002/09
高グレードのグリオーマ患者に対して熱外中性子ビームを用いた中性子捕捉療法を実行するための新しいプロトコルを作成するため、これまで実施されたBNCTの照射線量,組織学的腫瘍度数及び臨床結果の相関について解明した。1968から183例の脳腫瘍患者に対して実施されたBNCTのうち、1978年から1997年の間に実施した脳腫瘍患者105例の患者に対して回顧的な研究を行った。放射線的影響については、1977年から2001までに実施された159例全員に対して解析を行った。グリオブラストーマの10例の患者に対しては、熱外中性子ビームを使った新しいプロトコルに基づいて治療が行われた。
松村 明*; 山本 哲哉*; 柴田 靖*; 中井 啓*; Zhang, T.*; 阿久津 博義*; 松下 明*; 安田 貢*; 高野 晋吾*; 能勢 忠男*; et al.
ポストシークエンス時代における脳腫瘍の研究と治療, p.427 - 435, 2002/07
新しく整備されたJRR-4号炉にて混合(熱・熱外)中性子を用いた術中中性子捕捉療法( 粒子線治療)のphaseI/II臨床治験を行い、その有用性を検討し、さらに患者位置セッテイングシステムと線量評価システムの検証も行う。1999年10月よりJRR-4号炉にて混合中性子を用いてPhaseI/IIの臨床研究を開始した。対象は7例で悪性神経膠腫GradeIII)3例・神経膠芽腫(GradeIV)が4例の初発例で、治療対象は以前に放射線治療を受けていないもの,一側の脳半球に限局している,全身的な合併症や多重癌なし,年齢は18-70歳までとした。Follow up期間は2ヶ月から21ヶ月であり、平均(median生存期間は神経膠芽腫で15.7ヶ月でこれまでに1例が腫瘍の遠隔再発により死亡し、もう1例は脳以外の原因で15ヶ月目に死亡したが腫瘍再発はなかった。悪性神経膠腫は平均(median)生存期間 16.3ヶ月であり、3例中1例が脳以外の原因で死亡したが、残り2例は生存中で経過観察中である。神経膠芽腫は1年生存率が75%,悪性神経膠腫は1年生存率は100%で、全体としても1年以内の死亡は1例のみである。症例数も少なく、症例選択の問題もあり、他の成績と直接比較できないが、初期段階としては満足すべき成績と考えられる。今後さらに症例を増やして検討したい。なお、原研の本研究に対する協力は、臨床研究を補助する熱中性子及び血液中ホウ素濃度測定並びに物理線量評価,患者セッティングシステムについて行った。
粒子線治療)のphaseI/II臨床治験を行い、その有用性を検討し、さらに患者位置セッテイングシステムと線量評価システムの検証も行う。1999年10月よりJRR-4号炉にて混合中性子を用いてPhaseI/IIの臨床研究を開始した。対象は7例で悪性神経膠腫GradeIII)3例・神経膠芽腫(GradeIV)が4例の初発例で、治療対象は以前に放射線治療を受けていないもの,一側の脳半球に限局している,全身的な合併症や多重癌なし,年齢は18-70歳までとした。Follow up期間は2ヶ月から21ヶ月であり、平均(median生存期間は神経膠芽腫で15.7ヶ月でこれまでに1例が腫瘍の遠隔再発により死亡し、もう1例は脳以外の原因で15ヶ月目に死亡したが腫瘍再発はなかった。悪性神経膠腫は平均(median)生存期間 16.3ヶ月であり、3例中1例が脳以外の原因で死亡したが、残り2例は生存中で経過観察中である。神経膠芽腫は1年生存率が75%,悪性神経膠腫は1年生存率は100%で、全体としても1年以内の死亡は1例のみである。症例数も少なく、症例選択の問題もあり、他の成績と直接比較できないが、初期段階としては満足すべき成績と考えられる。今後さらに症例を増やして検討したい。なお、原研の本研究に対する協力は、臨床研究を補助する熱中性子及び血液中ホウ素濃度測定並びに物理線量評価,患者セッティングシステムについて行った。
山本 和喜; 山本 哲哉*; 熊田 博明; 鳥居 義也; 岸 敏明; 松村 明*; 能勢 忠男*; 堀口 洋二
JAERI-Tech 2001-017, 38 Pages, 2001/03
中性子ビーム線質の効果を観察するために、筑波大学と協力して、放射線感受性の異なる2種類のガン細胞を用いた細胞照射実験を実施した。使用したファントムは、円筒型のもので、内部に水を満たすことができるものである。培養した細胞懸濁液をウェルプレートに充填し、各モードで同じフルエンスになるよう照射を行った。結果、BSHを含んだ場合、最低生存率が0.001程度まで下がることがわかった。また、熱外中性子ビームが示すフラックス分布に比例し、深さ約2cmのところに最低生存率を示すこともわかった。線量単位についての考察から、熱外混合中性子ビームに対して従来から行ってきたホウ素+窒素線量を用いて整理、評価を行っても、十分対応可能であることを示した。