Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
 Br-
Br- -methyl-phenylalanine for tumor PET imaging
-methyl-phenylalanine for tumor PET imaging花岡 宏史*; 大島 康宏; 鈴木 結利花*; 山口 藍子*; 渡辺 茂樹; 上原 知也*; 永森 收志*; 金井 好克*; 石岡 典子; 対馬 義人*; et al.
Journal of Nuclear Medicine, 56(5), p.791 - 797, 2015/05
被引用回数:21 パーセンタイル:62.87(Radiology, Nuclear Medicine & Medical Imaging)Radiolabeled amino acids are superior PET tracers for imaging of malignant tumors, and amino acids labeled with  Br, an attractive positron emitter due to its relatively long half-life (t
Br, an attractive positron emitter due to its relatively long half-life (t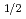 =16.2 h), could potentially be widely usable tumor imaging tracer. In this study, in consideration of stability and tumor specificity, 2-
=16.2 h), could potentially be widely usable tumor imaging tracer. In this study, in consideration of stability and tumor specificity, 2- Br-bromo-
Br-bromo- -methyl-L-phenylalanine (2-
-methyl-L-phenylalanine (2- Br-BAMP) and 4-
Br-BAMP) and 4- Br-bromo-
Br-bromo- -methyl-L-phenylalanine (4-
-methyl-L-phenylalanine (4- Br-BAMP) were designed and their potential as a tumor imaging agent was evaluated. No-carrier-added
Br-BAMP) were designed and their potential as a tumor imaging agent was evaluated. No-carrier-added  Br and
Br and  Br, the latter of which is suitable radiobromine for basic studies due to its longer half-life (t
Br, the latter of which is suitable radiobromine for basic studies due to its longer half-life (t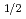 = 57.1 h), were produced. Both
= 57.1 h), were produced. Both  Br-BAMPs were stable in the plasma and in the murine body. In biodistribution studies, 2-
Br-BAMPs were stable in the plasma and in the murine body. In biodistribution studies, 2- Br-BAMP showed more rapid blood clearance and lower renal accumulation than did 4-
Br-BAMP showed more rapid blood clearance and lower renal accumulation than did 4- Br-BAMP. More than 90% of injected radioactivity was excreted in the urine by 6 h post-injection of 2-
Br-BAMP. More than 90% of injected radioactivity was excreted in the urine by 6 h post-injection of 2- Br-BAMP. High tumor accumulation of 2-
Br-BAMP. High tumor accumulation of 2- Br-BAMP was observed in tumor-bearing mice and PET imaging with 2-
Br-BAMP was observed in tumor-bearing mice and PET imaging with 2- Br-BAMP enabled clear visualization of the tumor. These findings suggest that 2-
Br-BAMP enabled clear visualization of the tumor. These findings suggest that 2- Br-BAMP would constitute a potential new PET tracer for tumor imaging and may eventually enable the wider use of amino acid tracers.
Br-BAMP would constitute a potential new PET tracer for tumor imaging and may eventually enable the wider use of amino acid tracers.
執行 信寛*; 魚住 祐介*; 上原 春彦*; 西澤 知也*; 水野 貴文*; 高宮 大義*; 橋口 太郎*; 佐藤 大樹; 佐波 俊哉*; 古場 裕介*; et al.
Nuclear Data Sheets, 119, p.303 - 306, 2014/05
被引用回数:0 パーセンタイル:0.00(Physics, Nuclear)重粒子線がん治療は、他の放射線治療に比べて正常部位への影響が小さいなどの利点により、近年注目を集めている。この治療では、患者の体内に入射した重イオンによる核反応で、中性子,  線等の二次放射線が生成される。治療施設の放射線安全設計のためには、二次放射線の生成量や角度分布を把握することが重要である。そこで、放射性医学総合研究所HIMAC加速器で、重粒子線がん治療に利用される290MeV/Aと体内での減速を想定した100MeV/Aの炭素ビームを用い、生体を構成する炭素,窒素及び酸素からの中性子生成断面積の実験データを15度から90度の角度領域で取得した。炭素ビームを入射するターゲットは、固体の炭素、アルミニウム化合物(窒化アルミニウム,酸化アルミニウム)及びアルミニウムで構成した。窒素及び酸素の断面積データは、アルミニウム化合物に対するデータから、アルミニウム単体によるデータを差し引き導出した。検出効率をSCINFUL-QMDコードで値づけた液体有機シンチレータ(NE213)を用いて中性子を検出し、運動エネルギーは飛行時間法(TOF)で求めた。取得した実験データと粒子・重イオン輸送計算コードPHITSの計算値との比較から、PHITSの核反応模型の精度を検証し、PHITSの重粒子線がん治療施設における放射線安全設計への応用についても議論する。
線等の二次放射線が生成される。治療施設の放射線安全設計のためには、二次放射線の生成量や角度分布を把握することが重要である。そこで、放射性医学総合研究所HIMAC加速器で、重粒子線がん治療に利用される290MeV/Aと体内での減速を想定した100MeV/Aの炭素ビームを用い、生体を構成する炭素,窒素及び酸素からの中性子生成断面積の実験データを15度から90度の角度領域で取得した。炭素ビームを入射するターゲットは、固体の炭素、アルミニウム化合物(窒化アルミニウム,酸化アルミニウム)及びアルミニウムで構成した。窒素及び酸素の断面積データは、アルミニウム化合物に対するデータから、アルミニウム単体によるデータを差し引き導出した。検出効率をSCINFUL-QMDコードで値づけた液体有機シンチレータ(NE213)を用いて中性子を検出し、運動エネルギーは飛行時間法(TOF)で求めた。取得した実験データと粒子・重イオン輸送計算コードPHITSの計算値との比較から、PHITSの核反応模型の精度を検証し、PHITSの重粒子線がん治療施設における放射線安全設計への応用についても議論する。
執行 信寛*; 魚住 祐介*; 上原 春彦*; 西澤 知也*; 平林 慶一*; 佐藤 大樹; 佐波 俊哉*; 古場 裕介*; 高田 真志*; 松藤 成弘*
Progress in Nuclear Science and Technology (Internet), 4, p.709 - 712, 2014/04
重粒子線治療では、患者体内に入射した重イオンビームによる核反応により、中性子をはじめとする2次放射線が生成される。重粒子線施設における治療室の遮へい設計のためには、患者を線源とした2次中性子の放出エネルギー及び角度分布を精度よく知る必要がある。これまでに測定された実験データは、独国GSIグループによる前方角度領域におけるもののみである。そこでわれわれは、放射線医学総合研究所HIMACにおいて、患者を模擬した水ファントムに治療に用いる290MeV/uの炭素ビームを入射し、15度から90度の広い角度領域で中性子生成量を測定した。水ファントムは厚さ20cmであり、入射炭素イオンはファントム内で完全に停止する。中性子検出器には、液体有機シンチレータNE213を採用し、その検出効率はSCINFUL-QMDコードを用いて求めた。中性子エネルギーは、飛行時間(TOF)法にて決定した。床散乱の寄与を評価するため、水ファントムとシンチレータの間に鉄製のシャドウバーを挿入した測定も行った。データ解析において、荷電粒子及び 線によるイベントを除去することにより、広い放出エネルギー、放出角度における中性子エネルギースペクトルの導出に成功した。また、取得した実験データとPHITSコードによる計算結果との比較を通して、PHITSコードの重粒子線治療施設の遮へい設計への応用についても議論した。
線によるイベントを除去することにより、広い放出エネルギー、放出角度における中性子エネルギースペクトルの導出に成功した。また、取得した実験データとPHITSコードによる計算結果との比較を通して、PHITSコードの重粒子線治療施設の遮へい設計への応用についても議論した。
執行 信寛*; 魚住 祐介*; 上原 春彦*; 西澤 知也*; 水野 貴文*; 佐藤 大樹; 佐波 俊哉*; 古場 裕介*; 高田 真志*; 松藤 成弘*
JAEA-Conf 2013-002, p.137 - 142, 2013/10
重粒子線がん治療では、患者の体内に入射した重イオンによる核反応で中性子や 線等の二次放射線が発生する。これら二次放射線による患部外臓器への線量付与とそれに伴う二次発がんリスクを評価するためには、核反応で生成する放射線の生成断面積データが不可欠となる。平成23年度までに、治療に用いる290MeV/u炭素イオンと生体構成元素である炭素,窒素及び酸素との核反応による中性子生成断面積データを、広い生成エネルギーと角度領域において取得し、粒子・重イオン輸送コードシステムPHITSの核反応模型の精度検証を行った。平成24年度は、人体内で減速した炭素イオンが起こす核反応を調べるため、100MeV/u炭素イオンを炭素ターゲットに入射した際の断面積を測定した。実験は、放射線医学総合研究所HIMAC加速器にて実施した。6台のNE213液体有機シンチレータを、ビーム軸から15
線等の二次放射線が発生する。これら二次放射線による患部外臓器への線量付与とそれに伴う二次発がんリスクを評価するためには、核反応で生成する放射線の生成断面積データが不可欠となる。平成23年度までに、治療に用いる290MeV/u炭素イオンと生体構成元素である炭素,窒素及び酸素との核反応による中性子生成断面積データを、広い生成エネルギーと角度領域において取得し、粒子・重イオン輸送コードシステムPHITSの核反応模型の精度検証を行った。平成24年度は、人体内で減速した炭素イオンが起こす核反応を調べるため、100MeV/u炭素イオンを炭素ターゲットに入射した際の断面積を測定した。実験は、放射線医学総合研究所HIMAC加速器にて実施した。6台のNE213液体有機シンチレータを、ビーム軸から15 , 30
, 30 , 45
, 45 , 60
, 60 , 75
, 75 及び90
及び90 方向に配置し、広い角度領域での測定を可能にした。中性子の運動エネルギーは飛行時間法によって決定し、入射エネルギーから約1MeVまでのエネルギー領域におけるデータ取得に成功した。NE213シンチレータの中性子検出効率は、機構が開発したSCINFUL-QMDコードにより求めている。取得した実験データはPHITSの計算値と比較し、核反応模型では再現の難しい低ネルギー重イオン入射反応の精度を検証した。
方向に配置し、広い角度領域での測定を可能にした。中性子の運動エネルギーは飛行時間法によって決定し、入射エネルギーから約1MeVまでのエネルギー領域におけるデータ取得に成功した。NE213シンチレータの中性子検出効率は、機構が開発したSCINFUL-QMDコードにより求めている。取得した実験データはPHITSの計算値と比較し、核反応模型では再現の難しい低ネルギー重イオン入射反応の精度を検証した。
 線生成断面積の測定
線生成断面積の測定魚住 祐介*; 執行 信寛*; 上原 春彦*; 西沢 知也*; 水野 貴文*; 佐藤 大樹; 佐波 俊哉*; 古場 裕介*; 高田 真志*; 松藤 成弘*; et al.
HIMAC-140, p.234 - 235, 2013/08
平成24年度に放射線医学総合研究所のHIMAC加速器を用いて行った研究の成果について報告する。重粒子線がん治療では、入射重イオンと生体構成元素との核反応から中性子及び 線が、患者体内で生成される。これら放射線による二次発がんリスクの推定には、重イオン核反応における生成断面積データが不可欠である。前年度までの研究により、広いエネルギー領域での断面積測定手法を確立し、治療に供される290MeV/u炭素イオンに対する炭素、窒素及び酸素原子核からの中性子生成断面積データを整備した。平成24年度は、患者体内にて減速した重イオンによる中性子及び
線が、患者体内で生成される。これら放射線による二次発がんリスクの推定には、重イオン核反応における生成断面積データが不可欠である。前年度までの研究により、広いエネルギー領域での断面積測定手法を確立し、治療に供される290MeV/u炭素イオンに対する炭素、窒素及び酸素原子核からの中性子生成断面積データを整備した。平成24年度は、患者体内にて減速した重イオンによる中性子及び 線の生成を調べるため、100MeV/u炭素イオンを炭素及び窒素ターゲットに入射する実験を行った。その結果、15
線の生成を調べるため、100MeV/u炭素イオンを炭素及び窒素ターゲットに入射する実験を行った。その結果、15 から90
から90 までの6角度において、下限エネルギー0.6MeVまでの精度の良い断面積測定に成功した。今後は、本エネルギー領域における実験データの拡充とともに、粒子・重イオン輸送コードシステムPHITSとの比較から、二体衝突近似が成立する下限エネルギーでの理論模型の妥当性について考察する。
までの6角度において、下限エネルギー0.6MeVまでの精度の良い断面積測定に成功した。今後は、本エネルギー領域における実験データの拡充とともに、粒子・重イオン輸送コードシステムPHITSとの比較から、二体衝突近似が成立する下限エネルギーでの理論模型の妥当性について考察する。
魚住 祐介*; 執行 信寛*; 梶本 剛*; 平林 慶一*; 上原 春彦*; 西澤 知也*; 佐藤 大樹; 佐波 俊哉*; 古場 裕介*; 高田 真志*; et al.
HIMAC-138, p.237 - 238, 2012/08
本発表では、平成23年度に放射線医学総合研究所のHIMAC加速器を用いて行った研究の成果について報告する。重粒子線がん治療では、入射重イオンと生体組織を構成する元素との核反応から中性子及び 線が患者体内で生成される。これらの放射線による二次発がんリスクの評価には、重イオン核反応における生成断面積のデータが不可欠である。平成22年度までの研究では、炭素+炭素及び酸素+炭素反応における中性子生成二重微分断面積を測定し、そのデータを公表した。平成23年度は290MeV/u炭素ビームを窒素化合物ターゲットに入射し、炭素+窒素反応における二重微分断面積を測定した。その結果、下限エネルギー0.6MeVまでの中性子断面積データを精度よく導出することに成功した。この成果をもって、所期の技術目標であった低エネルギー領域までの高精度中性子測定手法の確立は達せられた。今後は、確立した手法を用いて、生体構成元素に対する系統的な断面積データを整備する。また、前年度までのデータから
線が患者体内で生成される。これらの放射線による二次発がんリスクの評価には、重イオン核反応における生成断面積のデータが不可欠である。平成22年度までの研究では、炭素+炭素及び酸素+炭素反応における中性子生成二重微分断面積を測定し、そのデータを公表した。平成23年度は290MeV/u炭素ビームを窒素化合物ターゲットに入射し、炭素+窒素反応における二重微分断面積を測定した。その結果、下限エネルギー0.6MeVまでの中性子断面積データを精度よく導出することに成功した。この成果をもって、所期の技術目標であった低エネルギー領域までの高精度中性子測定手法の確立は達せられた。今後は、確立した手法を用いて、生体構成元素に対する系統的な断面積データを整備する。また、前年度までのデータから 線生成二重微分断面積の導出を行った。得られた実験データは、粒子・重イオン輸送コードシステムPHITSの計算結果と比較され、
線生成二重微分断面積の導出を行った。得られた実験データは、粒子・重イオン輸送コードシステムPHITSの計算結果と比較され、 線生成模型の検証・改良に応用される。
線生成模型の検証・改良に応用される。
 Re]Organorhenium-labeled antibody fragments with renal enzyme-cleavable linkage for low renal radioactivity levels
Re]Organorhenium-labeled antibody fragments with renal enzyme-cleavable linkage for low renal radioactivity levels上原 知也*; 小池 美穂*; 中田 英夫*; 花岡 宏史*; 飯田 靖彦*; 橋本 和幸; 秋澤 宏行*; 遠藤 啓吾*; 荒野 泰*
Bioconjugate Chemistry, 18(1), p.190 - 198, 2007/01
被引用回数:23 パーセンタイル:57.65(Biochemical Research Methods)抗体を標識母体とする薬剤は、その緩やかな血液クリアランスのため骨髄障害が広汎な応用を妨げる。標識母体を低分子化抗体(Fab)やペプチドに変換することで骨髄障害は解消されるが、腎臓への放射能滞留による腎障害が問題とされる。本研究では、腎臓刷子縁膜酵素の作用で標識Fabから尿排泄性の放射性代謝物を遊離する放射性レニウム標識薬剤を新規開発し、腎障害の解消を検討した。シクロペンタジエニルトリカルボニルレニウム(CpTR)をRe標識試薬の基本構造に選択し、CpTRにカルボン酸とグリシンを結合したCpTR-Glyの体内動態を検討した。その結果、CpTR-Glyは、マウス血清中で安定であること,血漿蛋白との結合が少ないことを明らかにした。また、CpTR-Glyをマウスに投与したとき、いずれの臓器にも滞留することなく、腎臓から速やかに尿中へと排泄されることを認めた。次に腎臓刷子縁膜酵素の作用でCpTR-GlyをFabから選択的に遊離するアミノ酸配列(マレイミド基)を導入した新規薬剤([ Re]CpTR-GK-Fab)を設計・合成し、マウス体内放射能動態を検討した。その結果、[
Re]CpTR-GK-Fab)を設計・合成し、マウス体内放射能動態を検討した。その結果、[ Re]CpTR-GK-Fabは、尿排泄性の放射性代謝物[
Re]CpTR-GK-Fabは、尿排泄性の放射性代謝物[ Re]CpTR-Glyを遊離して、腎臓への放射能集積を投与早期から大きく低減することを認めた。以上より、刷子縁膜酵素を利用した標識薬剤の設計は、金属RI標識低分子化抗体の腎臓への放射能集積の低減に有用であることを明らかにした。
Re]CpTR-Glyを遊離して、腎臓への放射能集積を投与早期から大きく低減することを認めた。以上より、刷子縁膜酵素を利用した標識薬剤の設計は、金属RI標識低分子化抗体の腎臓への放射能集積の低減に有用であることを明らかにした。
 Re chelate-conjugated bisphosphonate for the development of new radiopharmaceuticals for bones
Re chelate-conjugated bisphosphonate for the development of new radiopharmaceuticals for bones上原 知也*; Jin, Z. L.*; 小川 数馬*; 秋澤 宏行*; 橋本 和幸; 中山 守雄*; 荒野 泰*
Nuclear Medicine and Biology, 34(1), p.79 - 87, 2007/01
被引用回数:27 パーセンタイル:60.21(Radiology, Nuclear Medicine & Medical Imaging) Reとビスホスホネートの一つであるHEDPとが形成する
Reとビスホスホネートの一つであるHEDPとが形成する Re-HEDP多核錯体は、癌性骨転移の疼痛緩和剤として、その臨床応用が期待されている。しかしながら、血液からの消失速度が遅いため、骨髄被曝が危惧されている。そのため、速やかな血液クリアランスを示す
Re-HEDP多核錯体は、癌性骨転移の疼痛緩和剤として、その臨床応用が期待されている。しかしながら、血液からの消失速度が遅いため、骨髄被曝が危惧されている。そのため、速やかな血液クリアランスを示す Re標識薬剤の開発が望まれている。そこで、ビスホスホネート部位(APD)に安定な放射性レニウム錯体([
Re標識薬剤の開発が望まれている。そこで、ビスホスホネート部位(APD)に安定な放射性レニウム錯体([ Re]CpTR-Gly)を結合させた薬剤として、[
Re]CpTR-Gly)を結合させた薬剤として、[ Re]CpTR-Gly-APDを設計・合成し、そのマウス体内動態を
Re]CpTR-Gly-APDを設計・合成し、そのマウス体内動態を Re-HEDPと比較検討し、その有用性を評価した。まず、生体内で非常に安定であることが確認された。また、マウス体内動態の実験から、[
Re-HEDPと比較検討し、その有用性を評価した。まず、生体内で非常に安定であることが確認された。また、マウス体内動態の実験から、[ Re]CpTR-Gly-APDは
Re]CpTR-Gly-APDは Re-HEDPに比べて骨への有意に高い集積を示す一方で、血液から速やかな放射能消失を示した。さらに、
Re-HEDPに比べて骨への有意に高い集積を示す一方で、血液から速やかな放射能消失を示した。さらに、 Re-HEDPで観察された胃への放射能集積は観察されなかった。以上の結果は[
Re-HEDPで観察された胃への放射能集積は観察されなかった。以上の結果は[ Re]CpTR-Gly-APDの設計の有用性を示すものであり、生体内で安定かつ血漿タンパク質との結合が少なく、さらに低濃度の配位子による標識が可能な二官能性キレート構造をビスホスホネートと結合させることにより、より有用な薬剤の開発が可能となると考えられる。
Re]CpTR-Gly-APDの設計の有用性を示すものであり、生体内で安定かつ血漿タンパク質との結合が少なく、さらに低濃度の配位子による標識が可能な二官能性キレート構造をビスホスホネートと結合させることにより、より有用な薬剤の開発が可能となると考えられる。
小川 数馬*; 向 高弘*; 荒野 泰*; 大高 章*; 上田 真史*; 上原 知也*; 間賀田 泰寛*; 橋本 和幸; 佐治 英郎*
Nuclear Medicine and Biology, 33(4), p.513 - 520, 2006/05
被引用回数:57 パーセンタイル:80.60(Radiology, Nuclear Medicine & Medical Imaging)患者のQOL(生活の質)の向上を目指した癌性骨転移の疼痛緩和薬剤の開発を目指して、二官能性放射性薬剤の概念に基づき、安定な Re化合物である
Re化合物である Re-MAMA(モノアミンモノアミドジチオール)を骨への集積能を有するビスホスホネート骨格を持つ化合物に導入した新規薬剤を合成し、その特性を調べた。ビスホスホネートの中央炭素に水酸基を有した
Re-MAMA(モノアミンモノアミドジチオール)を骨への集積能を有するビスホスホネート骨格を持つ化合物に導入した新規薬剤を合成し、その特性を調べた。ビスホスホネートの中央炭素に水酸基を有した Re-MAMA-HBPと、水酸基を持たない
Re-MAMA-HBPと、水酸基を持たない Re-MAMA-BPを合成し、骨の主成分であるハイドロキシアパタイトへの結合親和性及びマウス体内分布を比較検討した。レニウム-186標識MAMA結合ビスホスホネートは、レニウムの還元剤として塩化スズを用い、クエン酸中で
Re-MAMA-BPを合成し、骨の主成分であるハイドロキシアパタイトへの結合親和性及びマウス体内分布を比較検討した。レニウム-186標識MAMA結合ビスホスホネートは、レニウムの還元剤として塩化スズを用い、クエン酸中で ReO
ReO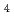
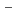 とMAMA結合ビスホスホネートを反応させ、逆相HPLCによる精製後、95%以上の放射化学的純度で得られた。
とMAMA結合ビスホスホネートを反応させ、逆相HPLCによる精製後、95%以上の放射化学的純度で得られた。 Re-MAMA-HBPは、
Re-MAMA-HBPは、 Re-MAMA-BPと比べ、インビトロにおいて、より高いハイドロキシアパタイトへの結合親和性を示し、インビボにおいて、より高い大腿骨への放射能集積を示した。したがって、
Re-MAMA-BPと比べ、インビトロにおいて、より高いハイドロキシアパタイトへの結合親和性を示し、インビボにおいて、より高い大腿骨への放射能集積を示した。したがって、 Re標識ビスホスホネートへの水酸基の導入は、骨集積増加に効果的であると考えられる。これらの結果は、骨指向性放射性治療薬剤のドラッグデザインに有用な指針を示すものである。
Re標識ビスホスホネートへの水酸基の導入は、骨集積増加に効果的であると考えられる。これらの結果は、骨指向性放射性治療薬剤のドラッグデザインに有用な指針を示すものである。
上原 知也*; 小池 美穂*; 中田 英夫*; 宮本 重彦*; 本石 章司; 橋本 和幸; 奥 直人*; 中山 守雄*; 荒野 泰*
Nuclear Medicine and Biology, 30(3), p.327 - 334, 2003/04
被引用回数:20 パーセンタイル:49.32(Radiology, Nuclear Medicine & Medical Imaging) Re標識低分子化抗体やペプチドによる癌の治療には、腎臓への放射能集積を示さない一方で、癌組織には長時間に渡る選択的な放射能集積を与える標識体の設計が必要である。そのためには、生体内で安定であり、かつ尿細管で母体タンパク質から遊離された際に、腎細胞へ取り込まれることなく、速やかに尿中へと排泄を受けるRe錯体の選択が重要である。本研究では、Cyclopentadienyltricarbonylrhenium(CpTR)をタンパク質やペプチドの
Re標識低分子化抗体やペプチドによる癌の治療には、腎臓への放射能集積を示さない一方で、癌組織には長時間に渡る選択的な放射能集積を与える標識体の設計が必要である。そのためには、生体内で安定であり、かつ尿細管で母体タンパク質から遊離された際に、腎細胞へ取り込まれることなく、速やかに尿中へと排泄を受けるRe錯体の選択が重要である。本研究では、Cyclopentadienyltricarbonylrhenium(CpTR)をタンパク質やペプチドの Re標識薬剤へ応用する目的で,CpTR-COOH及びそのグリシン(Gly)結合体の生体内での代謝を検討した。その結果、両者はともに血漿中及び緩衝液中で安定であった。一方、マウスに投与した場合、脂溶性の高いCpTR-COOHは胆汁排泄と尿排泄を受けたが、水溶性の高いCpTR-Glyは尿排泄のみを受けた。さらにCpTR-COOHは、複数の水溶性代謝物として排泄されるのに対して、CpTR-Glyは、代謝を受けずにそのまま排泄された。これらの結果から、腎臓刷子縁膜酵素の作用で母体ペプチドから[
Re標識薬剤へ応用する目的で,CpTR-COOH及びそのグリシン(Gly)結合体の生体内での代謝を検討した。その結果、両者はともに血漿中及び緩衝液中で安定であった。一方、マウスに投与した場合、脂溶性の高いCpTR-COOHは胆汁排泄と尿排泄を受けたが、水溶性の高いCpTR-Glyは尿排泄のみを受けた。さらにCpTR-COOHは、複数の水溶性代謝物として排泄されるのに対して、CpTR-Glyは、代謝を受けずにそのまま排泄された。これらの結果から、腎臓刷子縁膜酵素の作用で母体ペプチドから[ Re]CpTR-Glyを遊離する標識試薬は、腎臓での放射能滞留の解消に有用と考えられる。
Re]CpTR-Glyを遊離する標識試薬は、腎臓での放射能滞留の解消に有用と考えられる。
小川 数馬*; 小野 正博*; 藤岡 泰*; 佐治 英郎*; 向 高弘*; 小西 淳二*; 上原 知也*; 荒野 泰*; 小野間 克行
核医学, 37(5), P. 577, 2000/09
 Reとbisphosphonate(BP)のひとつであるHEDPとの多核錯体である
Reとbisphosphonate(BP)のひとつであるHEDPとの多核錯体である Re-HEDPは、癌性骨転移の疼痛緩和薬剤として期待されているが、生体内での安定性が乏しいことが問題である。そこで生体内で安定な
Re-HEDPは、癌性骨転移の疼痛緩和薬剤として期待されているが、生体内での安定性が乏しいことが問題である。そこで生体内で安定な Re標識骨疼痛緩和剤の開発を目的として、BPの炭素側鎖に
Re標識骨疼痛緩和剤の開発を目的として、BPの炭素側鎖に Reと安定な錯体を形成する部位を結合した化合物を設計した。目的とする化合物は総収率2.7%で合成された。
Reと安定な錯体を形成する部位を結合した化合物を設計した。目的とする化合物は総収率2.7%で合成された。 Re標識は、
Re標識は、 Re標識glucoheptonateとの配位子交換反応により行い、放射化学的純度は95%以上であった。なお、本標識化合物の体内動態については、現在検討をすすめている最中である。
Re標識glucoheptonateとの配位子交換反応により行い、放射化学的純度は95%以上であった。なお、本標識化合物の体内動態については、現在検討をすすめている最中である。
 Br標識抗体フラグメントの開発
Br標識抗体フラグメントの開発花岡 宏史*; 渡邉 茂樹; 渡辺 智; 大島 康宏; 上原 知也*; 秋澤 宏行*; 飯田 靖彦*; 石岡 典子; 荒野 泰*; 遠藤 啓吾*
no journal, ,
ポジトロン放出核種の一つである Brは半減期が16.1hと比較的長いことから、集積に時間を要するFab等の抗体フラグメントの標識にも利用できる。しかし
Brは半減期が16.1hと比較的長いことから、集積に時間を要するFab等の抗体フラグメントの標識にも利用できる。しかし Br標識Fabを生体内に投与した場合、腎臓への非特異的集積やFabより遊離したBrの血中滞留など、非標的臓器での放射能滞留が問題となる。そこで本研究では、
Br標識Fabを生体内に投与した場合、腎臓への非特異的集積やFabより遊離したBrの血中滞留など、非標的臓器での放射能滞留が問題となる。そこで本研究では、 Br標識Fabの非標的臓器への放射能集積低減を目的として、生体内で安定かつ腎放射能集積を大きく低減することが可能な代謝性スペーサーhippuryl-N-maleoyl-L-lysine(HML)を利用した
Br標識Fabの非標的臓器への放射能集積低減を目的として、生体内で安定かつ腎放射能集積を大きく低減することが可能な代謝性スペーサーhippuryl-N-maleoyl-L-lysine(HML)を利用した Br標識Fabを合成し、非標的組織における放射能集積について評価した。Br-HML-Fabを作製し、ノーマルマウスにおける体内動態を検討したところ、Br-HML-Fabは直接標識体と比較して血液から速やかにクリアランスされ、また代謝性スペーサーを含まないBr安息香酸標識体と比較して腎臓への放射能集積が大きく低減した。以上より、Br-HML-Fabは非標的臓器における放射能集積が低く、イメージング剤として有用である可能性が示された。
Br標識Fabを合成し、非標的組織における放射能集積について評価した。Br-HML-Fabを作製し、ノーマルマウスにおける体内動態を検討したところ、Br-HML-Fabは直接標識体と比較して血液から速やかにクリアランスされ、また代謝性スペーサーを含まないBr安息香酸標識体と比較して腎臓への放射能集積が大きく低減した。以上より、Br-HML-Fabは非標的臓器における放射能集積が低く、イメージング剤として有用である可能性が示された。
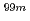 Tc及び
Tc及び Re標識オリゴアスパラギン酸の設計
Re標識オリゴアスパラギン酸の設計清田 幸子*; 上原 知也*; 石井 大輔*; 秋澤 宏行*; 橋本 和幸; 荒野 泰*
no journal, ,
 Reは、
Reは、 線を放出することからがん治療に有用と考えられている核種であり、一方、
線を放出することからがん治療に有用と考えられている核種であり、一方、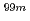 Tcは、
Tcは、 線を放出することから画像診断に使用されている核種である。本研究では、骨を標的とした
線を放出することから画像診断に使用されている核種である。本研究では、骨を標的とした Re,
Re, 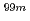 Tc標識化合物の開発を目的に、L, L-1, 2-Ethylene dicysteine(EC)1分子にペンタアスパラギン酸(Asp)
Tc標識化合物の開発を目的に、L, L-1, 2-Ethylene dicysteine(EC)1分子にペンタアスパラギン酸(Asp)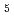 が1分子及び2分子結合したEC-(D-Asp)
が1分子及び2分子結合したEC-(D-Asp)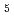 及びEC-[(D-Asp)
及びEC-[(D-Asp)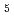 ]
] ,EC1分子に1分子の(D-Asp)
,EC1分子に1分子の(D-Asp)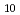 が結合したEC-(D-Asp)
が結合したEC-(D-Asp)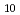 を設計・合成し、
を設計・合成し、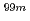 Tc及び
Tc及び Re標識体の安定性,体内動態を比較した。その結果、すべての
Re標識体の安定性,体内動態を比較した。その結果、すべての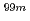 Tc標識体は血漿中で安定で、血漿タンパク質との結合も示さなかった。マウスに投与したところ、
Tc標識体は血漿中で安定で、血漿タンパク質との結合も示さなかった。マウスに投与したところ、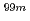 Tc- EC-[(D-Asp)
Tc- EC-[(D-Asp)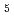 ]
] が最も速やかな血液からの消失を示した。
が最も速やかな血液からの消失を示した。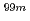 Tc-EC-[(D-Asp)
Tc-EC-[(D-Asp)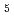 ]
] と
と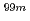 Tc-EC-(D-Asp)
Tc-EC-(D-Asp)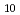 の骨への集積は同程度であったが、
の骨への集積は同程度であったが、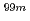 Tc-EC-(D-Asp)
Tc-EC-(D-Asp)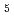 は骨への集積低減と経時的な消失を示した。
は骨への集積低減と経時的な消失を示した。 Re標識体も同様の結果を与えた。以上の結果は、新たな骨機能の画像診断並びに癌性骨転移の疼痛緩和薬剤の開発に対する本薬剤設計の有用性を示したものである。
Re標識体も同様の結果を与えた。以上の結果は、新たな骨機能の画像診断並びに癌性骨転移の疼痛緩和薬剤の開発に対する本薬剤設計の有用性を示したものである。
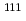 In標識馬尿酸誘導体の合成と
In標識馬尿酸誘導体の合成と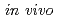 評価
評価鈴木 博元; 金井 彩香*; 上原 知也*; 花岡 宏史*; 荒野 泰*
no journal, ,
Radiolabeled antibody fragments show rapid elimination rate from blood, which can improve bone marrow toxicities of radiolabeled intact IgG. However, high and persistent localization in kidney is observed, which impairs diagnostic accuracy and therapeutic effectiveness. Brush border strategy succeeded to reduce renal radioactivity by using the radioiodine labeled antibody fragment in which a cleavable peptide linker is introduced. In the strategy, the radiometabolite is liberated by the action of renal brush border enzymes before incorporating into renal cells, and excreted into urine. In order to apply this molecular design to radiometals such as 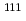 In and
In and 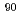 Y, the radiometabolite with high urinary excretion, which includes a radiometal-chelating moiety is required. In this study, we synthesized and evaluated a hippuric acid derivative, Bn-CHX-A"-DTPA-Gly labeled with
Y, the radiometabolite with high urinary excretion, which includes a radiometal-chelating moiety is required. In this study, we synthesized and evaluated a hippuric acid derivative, Bn-CHX-A"-DTPA-Gly labeled with 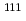 In as a radiometabolite.
In as a radiometabolite.
執行 信寛*; 魚住 祐介*; 上原 春彦*; 西澤 知也*; 平林 慶一*; 佐藤 大樹; 佐波 俊哉*; 古場 裕介*; 高田 真志*; 松藤 成弘*
no journal, ,
粒子線がん治療において照射時に患者体内で生成される中性子や 線などの二次放射線の放出エネルギーや角度分布を把握することは、施設の安全設計とそれによる運転員や公衆の放射線防護にとって重要である。本研究では、重粒子線がん治療に利用される290MeV/u炭素ビームを人体を模擬した水ファントムに入射し、生成される中性子の二重微分収量を測定した。実験は、放射線医学総合研究所HIMAC施設にて行った。ファントムは、奥行き20cm,高さ32cm,厚さ1cmのアクリル容器からなり、内部を純水で満たした。中性子検出器には、直径と長さがともに12.7cm及び5.08cmである2種類の液体有機シンチレータを採用した。中性子エネルギーは飛行時間法に基づき導出した。測定角度は15
線などの二次放射線の放出エネルギーや角度分布を把握することは、施設の安全設計とそれによる運転員や公衆の放射線防護にとって重要である。本研究では、重粒子線がん治療に利用される290MeV/u炭素ビームを人体を模擬した水ファントムに入射し、生成される中性子の二重微分収量を測定した。実験は、放射線医学総合研究所HIMAC施設にて行った。ファントムは、奥行き20cm,高さ32cm,厚さ1cmのアクリル容器からなり、内部を純水で満たした。中性子検出器には、直径と長さがともに12.7cm及び5.08cmである2種類の液体有機シンチレータを採用した。中性子エネルギーは飛行時間法に基づき導出した。測定角度は15 から90
から90 までの6点である。実験値と粒子・重イオン輸送コードシステムPHITSの計算値との比較において、PHITSは実験値をおおむね再現した。しかし、高エネルギー側で実験値を過小評価、低エネルギー側で過大評価することが明らかになった。
までの6点である。実験値と粒子・重イオン輸送コードシステムPHITSの計算値との比較において、PHITSは実験値をおおむね再現した。しかし、高エネルギー側で実験値を過小評価、低エネルギー側で過大評価することが明らかになった。
 Br標識アミノ酸2-
Br標識アミノ酸2- Br-bromo-
Br-bromo- -methyl-L-phenylalanineの開発
-methyl-L-phenylalanineの開発大島 康宏; 花岡 宏史*; 鈴木 結利花*; 山口 藍子*; 渡辺 茂樹; 上原 知也*; 永森 收志*; 金井 好克*; 石岡 典子; 対馬 義人*; et al.
no journal, ,
本研究では、より生体内安定性の高い Br標識アミノ酸として、新たに2-
Br標識アミノ酸として、新たに2- Br-bromo-
Br-bromo- -methyl-L-phenylalanine (2-
-methyl-L-phenylalanine (2- Br-BAMP)を合成し、新規PETイメージング薬としての有用性について検討した。放射性Br(
Br-BAMP)を合成し、新規PETイメージング薬としての有用性について検討した。放射性Br( Br及び
Br及び Br)はセレン化銅ターゲットに対してプロトンビーム(20MeV)を照射することで製造した。
Br)はセレン化銅ターゲットに対してプロトンビーム(20MeV)を照射することで製造した。 Brは半減期16.2時間の陽電子放出核種であることからPETイメージングに使用し、
Brは半減期16.2時間の陽電子放出核種であることからPETイメージングに使用し、 Brは半減期57.1時間の
Brは半減期57.1時間の 線放出核種であることから基礎検討に使用した。酸化剤存在下において、放射性Brと標識前駆体(2-trimethylstannyl-N-trifluoroacetyl-
線放出核種であることから基礎検討に使用した。酸化剤存在下において、放射性Brと標識前駆体(2-trimethylstannyl-N-trifluoroacetyl- -methyl-L-phenylalanine methyl ester)を反応させ、2-
-methyl-L-phenylalanine methyl ester)を反応させ、2- Br-BAMP及び2-
Br-BAMP及び2- Br-BAMPを合成した。HPLC分析の結果、標識率52.6
Br-BAMPを合成した。HPLC分析の結果、標識率52.6 11.9%、放射化学的純度95%以上で2-
11.9%、放射化学的純度95%以上で2- Br-BAMPの合成が可能であった。血清及びマウス体内における2-
Br-BAMPの合成が可能であった。血清及びマウス体内における2- Br-BAMPの分解はほとんど認められず、非常に高い安定性を示した。体内分布では、2-
Br-BAMPの分解はほとんど認められず、非常に高い安定性を示した。体内分布では、2- Br-BAMPは癌へ高度に集積する一方、血中からの消失は早く、投与放射能の90%以上が6時間以内に尿中に排泄され、正常臓器へ非常に低い集積を示した。さらに2-
Br-BAMPは癌へ高度に集積する一方、血中からの消失は早く、投与放射能の90%以上が6時間以内に尿中に排泄され、正常臓器へ非常に低い集積を示した。さらに2- Br-BAMPを用いてPET撮像を行った結果、癌を明瞭にイメージングすることができた。これらの結果より、2-
Br-BAMPを用いてPET撮像を行った結果、癌を明瞭にイメージングすることができた。これらの結果より、2- Br-BAMPの新規PETイメージング薬としての有用性が示唆された。
Br-BAMPの新規PETイメージング薬としての有用性が示唆された。