Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
 I]-sansalvamide A derivative
I]-sansalvamide A derivative渡邉 茂樹; 山田 圭一*; 津久井 匠隆*; 花岡 宏史*; 大島 康宏; 山口 藍子*; 奥 浩之*; 石岡 典子
JAEA-Review 2012-046, JAEA Takasaki Annual Report 2011, P. 88, 2013/01
Sansalvamide A (SA), a penta cyclic peptide isolated marine fungus, is a lead compound of anti-cancer reagent because the peptide has cytotoxicity against various cancer cell lines. Halogenated SA derivatives (SA-X, X = Cl, Br, I) was prepared and remarkable cytotocity against malignant human breast cancer. In this study, a radiohalogenated SA derivative [ I]SA-I was prepared to conduct in vivo evaluation of SA derivatives. Synthetic scheme of [
I]SA-I was prepared to conduct in vivo evaluation of SA derivatives. Synthetic scheme of [ I]SA-I are as follows: an iodinated linear peptide, Boc-F(p-I)LLVL-OMe, was prepared by the conventional solid phase peptide synthesis. After preparation of stannylated peptide, Boc-F(p-SnBu
I]SA-I are as follows: an iodinated linear peptide, Boc-F(p-I)LLVL-OMe, was prepared by the conventional solid phase peptide synthesis. After preparation of stannylated peptide, Boc-F(p-SnBu )LLVL-OMe,
)LLVL-OMe,  I was labeled with electrophilic destannylation in the presence of oxidizing reagent. After deprotection of N- and C-termius, [
I was labeled with electrophilic destannylation in the presence of oxidizing reagent. After deprotection of N- and C-termius, [ I]SA-I was obtained successfully by macrocyclization in liquid phase. Overall labeled yield was 7%. To our best knowledge, this report is the first on the synthesis of radiolabeled SA derivative. In vivo evaluation of the SA derivative using [
I]SA-I was obtained successfully by macrocyclization in liquid phase. Overall labeled yield was 7%. To our best knowledge, this report is the first on the synthesis of radiolabeled SA derivative. In vivo evaluation of the SA derivative using [ I]SA-I is being undertaken.
I]SA-I is being undertaken.
山田 圭一*; 渡邉 茂樹; 大島 康宏; 花岡 宏史*; 津久井 匠隆*; 高野 智香子*; 山口 藍子*; 奥 浩之*; 石岡 典子
no journal, ,
Sansalvamide A (SA) is a marin-derived cyclic depsipeptide that exhibits cytotoxicity against colon cancer cell line. Recently, a series of cyclic pentapeptide analogs of SA in which Hmp ((2S)-2-hydroxy-4-methylpentanoic acid) residue was replaced by amino acids or N-methyl-amino acids were synthesized. We previously reported that the haogenated analog of [MeLeu ]SA, namely SA-Br, SA-I, SA-Cl, exhibited potent cytotoxicity against MDA-MB-231. In the present study, we considered to evaluate in vivo biodistribution, stability and antitumor activity of these halogenated SA peptides in tumor-bearing mice. For this purpose, radiohalogen atoms are most suitable for labeling without changing their primary structure and biological activity. Here, we report the synthesis and in vivo biodistribution of
]SA, namely SA-Br, SA-I, SA-Cl, exhibited potent cytotoxicity against MDA-MB-231. In the present study, we considered to evaluate in vivo biodistribution, stability and antitumor activity of these halogenated SA peptides in tumor-bearing mice. For this purpose, radiohalogen atoms are most suitable for labeling without changing their primary structure and biological activity. Here, we report the synthesis and in vivo biodistribution of  I-labeled SA analog (SA-[
I-labeled SA analog (SA-[ I]).
I]).
渡邉 茂樹; 山田 圭一*; 花岡 宏史*; 大島 康宏; 高野 智香子*; 津久井 匠隆*; 山口 藍子*; 須郷 由美; 奥 浩之*; 石岡 典子
no journal, ,
がん細胞に対する細胞障害活性を持つ生理活性ペプチドは、抗がん剤開発におけるリード化合物(化学修飾することで活性の向上、毒性の減弱などが期待できる新規化合物)となりうる。中でも環状ペプチドは、ペプチド分解酵素に対する耐性が高く、リジッドな構造を持つことから、生体内において安定で標的細胞に対して選択性が高い抗がん薬剤のリード化合物として期待できる。本発表では、4つのアミノ酸と1つのヒドロキシ酸から構成される海洋真菌類由来の環状ペプチドSansalvamide A(SA)をリード化合物として開発した難治性乳がん細胞に対する細胞障害活性を持つSA-Iの体内動態を明らかにするために、放射性ヨウ素であるI-125(半減期59.4日)を導入した[ I]SA-Iの合成、及び、ノーマルマウス及び難治性乳がん移植マウスにおける体内動態の検討について報告する。
I]SA-Iの合成、及び、ノーマルマウス及び難治性乳がん移植マウスにおける体内動態の検討について報告する。
津久井 匠隆; 渡邉 茂樹; 山田 圭一*; 花岡 宏史*; 奥 浩之*; 松尾 一郎*; 遠藤 啓吾*; 石岡 典子
no journal, ,
生理活性ペプチドの中には、抗がん作用,抗菌作用を示すものやホルモン様作用を示して受容体と結合するものがあり、創薬のリード化合物となり得る。われわれが開発したパラ位に臭素原子が置換された芳香族アミノ酸を構造中に有する環状ペプチドは、インビトロ実験において乳がん細胞の増殖抑制能を有することが明らかになっている。そこで、インビボ実験における体内分布の取得を目指し、開発した環状ペプチドへの放射性臭素の標識に関する基礎検討を実施した。構成アミノ酸である芳香族アミノ酸誘導体の標識条件では、前駆体に対しCATを1等量、NCSでは4等量加え、室温15分間反応させることで、それぞれ標識率70%で反応が進行し、効率よくBr-77を導入できることを確認した。標識前駆体の合成では、Boc-SPPS法により生成した化合物についてESI-MS分析を行った結果、目的物に相当するイオンピークは得られず、トリブチルスズアミノ酸を用いるBoc-SPPS法は環状ペプチド合成に適していないことが明らかとなった。そこで、現在新たな合成法として脱保護に塩基を用いるFmoc-SPPSによる合成について検討を行っている。
 Br標識アミノ酸誘導体の開発
Br標識アミノ酸誘導体の開発花岡 宏史*; 渡邉 茂樹; 富永 英之*; 大島 康宏; 津久井 匠隆; 渡辺 智; 山田 圭一*; 飯田 靖彦*; 織内 昇*; 樋口 徹也*; et al.
no journal, ,
 Cや
Cや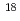 Fで標識したアミノ酸誘導体は、がん診断用のPET薬剤として、臨床使用されているものも少なくない。しかしながら
Fで標識したアミノ酸誘導体は、がん診断用のPET薬剤として、臨床使用されているものも少なくない。しかしながら Cや
Cや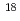 Fは短半減期であるため、それぞれの病院で製造する必要があり、限られた施設でしか使えないのが現状である。一方で
Fは短半減期であるため、それぞれの病院で製造する必要があり、限られた施設でしか使えないのが現状である。一方で Brは半減期が16.1時間とポジトロン放出核種としては比較的長く、また
Brは半減期が16.1時間とポジトロン放出核種としては比較的長く、また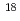 Fと同じハロゲン核種であるため、
Fと同じハロゲン核種であるため、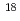 F標識アミノ酸製剤と同様の分子設計を行うことができるという利点を有する。そこで本研究では、広く臨床使用することが可能な、新規がん診断用PETイメージング薬剤として
F標識アミノ酸製剤と同様の分子設計を行うことができるという利点を有する。そこで本研究では、広く臨床使用することが可能な、新規がん診断用PETイメージング薬剤として Br標識アミノ酸誘導体を開発することを計画した。基礎的検討には半減期が長い放射性臭素である
Br標識アミノ酸誘導体を開発することを計画した。基礎的検討には半減期が長い放射性臭素である Br(半減期57時間)を用いて行うこととした。Br標識アミノ酸としては、
Br(半減期57時間)を用いて行うこととした。Br標識アミノ酸としては、 -メチルフェニルアラニンのパラ位にBrを導入したp-Bromo-
-メチルフェニルアラニンのパラ位にBrを導入したp-Bromo- -methyl-Pheを設計した。
-methyl-Pheを設計した。 Br標識Phe誘導体は標識率25
Br標識Phe誘導体は標識率25 40%で合成することができた。ノーマルマウスにおける体内動態を検討した結果、膵臓に高い集積が認められたことから、本化合物はアミノ酸トランスポーターに認識されていることが示唆された。一方で腎臓に対しても高い集積がみられた。担癌マウスに投与したところ、腫瘍への高い集積性を示し、投与3時間後の腫瘍血液比は3.94、腫瘍筋肉比は3.51となった。以上の結果から、Br標識Phe誘導体は、新規がんイメージング剤として有用である可能性が示された。
40%で合成することができた。ノーマルマウスにおける体内動態を検討した結果、膵臓に高い集積が認められたことから、本化合物はアミノ酸トランスポーターに認識されていることが示唆された。一方で腎臓に対しても高い集積がみられた。担癌マウスに投与したところ、腫瘍への高い集積性を示し、投与3時間後の腫瘍血液比は3.94、腫瘍筋肉比は3.51となった。以上の結果から、Br標識Phe誘導体は、新規がんイメージング剤として有用である可能性が示された。
津久井 匠隆; 山田 圭一*; 渡邉 茂樹; 花岡 宏史*; 奥 浩之*; 遠藤 啓吾*; 石岡 典子; 松尾 一郎*
no journal, ,
p-(tri-n-butyl-stannyl)-phenylalanine (Phe(p-Bu Sn)) is an useful building blocks for synthesizing radiolabeled pharmaceutics. To best of our knowledge, there are few studies of the synthesis of Phe(p-Bu
Sn)) is an useful building blocks for synthesizing radiolabeled pharmaceutics. To best of our knowledge, there are few studies of the synthesis of Phe(p-Bu Sn)-containing peptides. In this study, we report solid-phase synthesis of cyclic peptides containing Phe(p-Bu
Sn)-containing peptides. In this study, we report solid-phase synthesis of cyclic peptides containing Phe(p-Bu Sn) residue, cyclo(Phe(p-Bu
Sn) residue, cyclo(Phe(p-Bu Sn)-Leu-MeLeu-Val-Leu) (I). Boc-Phe(p-Bu
Sn)-Leu-MeLeu-Val-Leu) (I). Boc-Phe(p-Bu Sn)-OH was synthesized from Boc-Phe(p-I)-OMe by treatment with bis(tri-n-butyl)tin and Pd(0) catalyst followed by saponification. The linear peptide containing Phe(p-Bu
Sn)-OH was synthesized from Boc-Phe(p-I)-OMe by treatment with bis(tri-n-butyl)tin and Pd(0) catalyst followed by saponification. The linear peptide containing Phe(p-Bu Sn) residue was assembled on Kaiser-oxime resin. On-resin macrocyclization of the linear peptide, however, did not afford the cyclic peptide I. Cross coupling of cyclic peptide containing Phe(p-I) residue, cyclo(Phe(p-I)-Leu-MeLeu-Val-Leu) with bis(tri-n-butyl)tin and Pd(0) catalyst gave the desired peptide, which was confirmed by ESI-MS. In this presentation, we will report the Fmoc-SPPS of the peptide I.
Sn) residue was assembled on Kaiser-oxime resin. On-resin macrocyclization of the linear peptide, however, did not afford the cyclic peptide I. Cross coupling of cyclic peptide containing Phe(p-I) residue, cyclo(Phe(p-I)-Leu-MeLeu-Val-Leu) with bis(tri-n-butyl)tin and Pd(0) catalyst gave the desired peptide, which was confirmed by ESI-MS. In this presentation, we will report the Fmoc-SPPS of the peptide I.
津久井 匠隆; 渡邉 茂樹; 花岡 宏史*; 山田 圭一*; 奥 浩之*; 石岡 典子; 遠藤 啓吾*; 松尾 一郎*
no journal, ,
生理活性ペプチドには顕著な抗腫瘍活性を示すものがあり、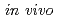 での治療効果に興味が持たれている。これらの生理活性ペプチドにおける構造活性相関等の創薬研究は、さまざまな所で行われている。創薬研究では、薬剤の体内分布や腫瘍への集積能が重要な因子となり得る。演者らは、放射性核種を標識した生理活性ペプチドを用いて体内での薬剤挙動と治療効果を同時に計測できれば薬剤開発の効率化が可能になると考え、その標識化法を検討している。本発表では、Boc-Phe(
での治療効果に興味が持たれている。これらの生理活性ペプチドにおける構造活性相関等の創薬研究は、さまざまな所で行われている。創薬研究では、薬剤の体内分布や腫瘍への集積能が重要な因子となり得る。演者らは、放射性核種を標識した生理活性ペプチドを用いて体内での薬剤挙動と治療効果を同時に計測できれば薬剤開発の効率化が可能になると考え、その標識化法を検討している。本発表では、Boc-Phe(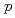 -SnBu
-SnBu )-OMeを前駆体としたBr-77標識アミノ酸の合成に関する基礎的検討について報告する。酸化剤にChloramine T、N-Chlorosuccinimideを用いて室温30分間標識化したところ、その標識率は60
)-OMeを前駆体としたBr-77標識アミノ酸の合成に関する基礎的検討について報告する。酸化剤にChloramine T、N-Chlorosuccinimideを用いて室温30分間標識化したところ、その標識率は60 85%であった。現在、Phe(
85%であった。現在、Phe(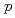 -SnBu
-SnBu )含有ペプチドへの適用も検討しており、併せて報告する予定である。
)含有ペプチドへの適用も検討しており、併せて報告する予定である。
渡邉 茂樹; 花岡 宏史*; 津久井 匠隆; 渡辺 智; 飯田 靖彦*; 遠藤 啓吾*; 石岡 典子
no journal, ,
腫瘍に発現する抗原を標的とする抗体は腫瘍特異的な集積を示すことから、PET核種を標識した抗体は腫瘍だけを選択的に描出するPET薬剤として利用が期待される。これまでわれわれは抗体の体内動態に適した半減期を有するBr-76(半減期=16.1h)に着目し、抗体のアミノ酸残基に直接Br-76を標識する方法でBr-76標識抗体の開発を行ってきた。しかし、直接標識は過剰量の酸化剤を使用することによる抗体の変性も懸念されるうえに、標識率が低いことから、抗体の性質を保持したままより効率よくBr-76を標識する方法が必要である。そこで、本発表では、安息香酸を標識中間体として用いる間接標識法によるBr-76標識抗体合成の基礎検討を行った。その結果、標識前駆体を全収率31%で合成し、目的物であることをNMR及び質量分析により確認した。Br-77を用いて標識を行った結果、標識率25%で反応が進行することを確認した。現在、安息香酸への標識条件について詳細な検討を行うとともに、抗体への導入について検討を行っている。また、標識位置による標識率と安定性の違いについても議論する予定である。
 I標識環状ペプチドSansalvamide A誘導体の合成と評価
I標識環状ペプチドSansalvamide A誘導体の合成と評価渡邉 茂樹; 山田 圭一*; 花岡 宏史*; 大島 康宏; 津久井 匠隆*; 高野 智香子*; 山口 藍子*; 奥 浩之*; 飯田 靖彦*; 遠藤 啓吾*; et al.
no journal, ,
Sansalvamide A(SA)は、抗腫瘍活性を持つ海洋真菌類由来の天然環状ペプチドである。われわれはSAのPhe側鎖芳香環にハロゲンを導入した誘導体SA-X(cyclo(Phe(p-X)-Leu-MeLeu-Val-Leu), X=Cl, Br, I)を合成し、これらが乳がん細胞MDA-MB-231に対してin vitroで細胞毒性を持つことを見いだした。本研究ではin vivo評価を目的として I標識Sansalvamide A誘導体[
I標識Sansalvamide A誘導体[ I]SA-Iの合成について検討した。その結果、Boc固相合成法により直鎖ペプチドBoc-Phe(p-SnBu
I]SA-Iの合成について検討した。その結果、Boc固相合成法により直鎖ペプチドBoc-Phe(p-SnBu )-Leu-MeLeu-Val-Leu-OMeを得た後、スズ-ヨウ素交換反応による
)-Leu-MeLeu-Val-Leu-OMeを得た後、スズ-ヨウ素交換反応による I標識,脱保護、及び、液相での環化を行うことで[
I標識,脱保護、及び、液相での環化を行うことで[ I]SA-Iを合成できることを見いだした。
I]SA-Iを合成できることを見いだした。
 I-Sansalvamide Aの合成と評価
I-Sansalvamide Aの合成と評価渡邉 茂樹; 津久井 匠隆; 花岡 宏史*; 山田 圭一*; 大島 康宏; 飯田 靖彦*; 遠藤 啓吾*; 石岡 典子
no journal, ,
抗がん作用や抗菌作用を示す生理活性物質は、創薬におけるリード化合物となる。Sansalvamide A(SA)は、構造中にエステル結合を有する海洋真菌類由来の環状デプシペプチドで、大腸がん細胞に対して高い細胞毒性を示すことから、抗がん剤開発のリード化合物として注目されている。これまでわれわれは、フェニルアラニン側鎖にヨウ素を導入したSA誘導体を開発し、この化合物が悪性度の高い乳がん細胞MD-MBA-231に対して高い細胞障害活性を示すことを明らかにしてきた。そこで、本研究ではI-SAの生体内における動態を解明するために、 Iを導入した
Iを導入した I-SAを合成し、ノーマルマウスにおける体内分布を明らかにすることとした。
I-SAを合成し、ノーマルマウスにおける体内分布を明らかにすることとした。