Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
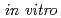 evaluation of F(
evaluation of F( -
- I)KCCYSL for targeting HER2
I)KCCYSL for targeting HER2佐々木 一郎; 渡辺 茂樹; 大島 康宏; 須郷 由美; 山田 圭一*; 花岡 宏史*; 石岡 典子
Peptide Science 2015, p.243 - 246, 2016/03
Radioisotope labeled peptides with high affinity to receptors overexpressing on the surface of tumor cells are promising for applications in nuclear medicine such as diagnostic radiography and radiotherapy. Radiohalogens such as  I and
I and 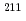 At are useful for clinical imaging and therapeutic applications, and it can be introduced at the
At are useful for clinical imaging and therapeutic applications, and it can be introduced at the 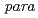 position of phenylalanine residue via electrophilic destannylation. KCCYSL (Lys
position of phenylalanine residue via electrophilic destannylation. KCCYSL (Lys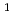 -Cys
-Cys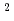 -Cys
-Cys -Tyr
-Tyr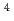 -Ser
-Ser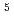 -Leu
-Leu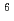 ) is a hexapeptide containing disulfide bond. Previous study revealed that KCCYSL has potential as tumor imaging and therapeutic agent targeting tumor cells overexpressing the human epidermal growth factor receptor type 2 (HER2). In this study, we report synthesis and
) is a hexapeptide containing disulfide bond. Previous study revealed that KCCYSL has potential as tumor imaging and therapeutic agent targeting tumor cells overexpressing the human epidermal growth factor receptor type 2 (HER2). In this study, we report synthesis and 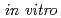 evaluation of radiohalogenated KCCYSL derivatives. Precursor peptides, Boc-F(
evaluation of radiohalogenated KCCYSL derivatives. Precursor peptides, Boc-F( -SnBu
-SnBu )K(Boc)C(Trt)C(Trt)Y(
)K(Boc)C(Trt)C(Trt)Y(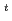 Bu)S(
Bu)S(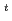 Bu)L-OH and Boc-F(
Bu)L-OH and Boc-F( -SnBu
-SnBu )GS(
)GS(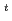 Bu)GK(Boc)C(Trt)C(Trt)Y(
Bu)GK(Boc)C(Trt)C(Trt)Y(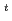 Bu)S(
Bu)S(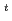 Bu)L-OH, were synthesized by the Fmoc solid phase peptide synthesis. Then, precursor peptides were radioiodinated via electrophilic destannylation, and they were deprotected to obtain F(
Bu)L-OH, were synthesized by the Fmoc solid phase peptide synthesis. Then, precursor peptides were radioiodinated via electrophilic destannylation, and they were deprotected to obtain F( -
- I)KCCYSL and F(
I)KCCYSL and F( -
- I)GSGKCCYSL in radiochemical yield 15% and 17%, respectively.
I)GSGKCCYSL in radiochemical yield 15% and 17%, respectively. 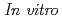 assays of the radioiodinated peptides for HER2 and stability in serum are being undertaken.
assays of the radioiodinated peptides for HER2 and stability in serum are being undertaken.
佐々木 一郎; 花岡 宏史*; 山田 圭一*; 渡辺 茂樹; 須郷 由美; 大島 康宏; 鈴木 博元; 石岡 典子
Peptide Science 2014, p.257 - 260, 2015/03
We have sought to establish drug discovery system using radioisotope (RI) labeled peptides which have high affinity to target proteins overexpressed in cancers. Of the target proteins, we chose the human epidermal growth factor receptor type 2 (HER2), a membrane protein overexpressed in various cancers to evaluate the drug discovery system. Three series of random hexapeptide libraries introduced a radioiodinated D-tyrosine (y(3- I)) to
I)) to 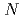 -terminal were designed and binding assay with HER2-expressed cell lines were conducted in this study. First, we synthesized a series of random hexapeptide libraries with fixed amino acid sequence at 1 and 2 positions, y(3-
-terminal were designed and binding assay with HER2-expressed cell lines were conducted in this study. First, we synthesized a series of random hexapeptide libraries with fixed amino acid sequence at 1 and 2 positions, y(3- I)X
I)X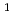 X
X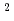 X
X X
X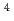 X
X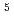 X
X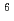 . Non-radioactive random peptide libraries, yXXXXXX, were prepared by Fmoc-SPPS with an automatic peptide synthesizer. Radioiodinated y(3-
. Non-radioactive random peptide libraries, yXXXXXX, were prepared by Fmoc-SPPS with an automatic peptide synthesizer. Radioiodinated y(3- I)XXXXXX were subsequently synthesized in 30-50% radiochemical yield. Binding assay using HER2-overexpressed cell line showed that high affinity (38-50% dose, n=6) was obtained with yIIXXXX, while other random peptide libraries were yielded low affinity (approximately 1% dose), which indicated that the system using RI labeled random peptide libraries have potential to discover peptide drug for cancer therapy. Preparation of other random hexapeptide libraries are being undertaken.
I)XXXXXX were subsequently synthesized in 30-50% radiochemical yield. Binding assay using HER2-overexpressed cell line showed that high affinity (38-50% dose, n=6) was obtained with yIIXXXX, while other random peptide libraries were yielded low affinity (approximately 1% dose), which indicated that the system using RI labeled random peptide libraries have potential to discover peptide drug for cancer therapy. Preparation of other random hexapeptide libraries are being undertaken.
佐々木 一郎; 山田 圭一*; 渡辺 茂樹; 花岡 宏史*; 須郷 由美; 奥 浩之*; 石岡 典子
JAEA-Review 2013-059, JAEA Takasaki Annual Report 2012, P. 96, 2014/03
Radioisotope (RI)-labeled peptide with high affinity to receptors overexpressing on the surface of tumor cells are promising for applications in nuclear medicine such as diagnostic radiography and radiotherapy. MARSGL (H-Met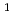 -Ala
-Ala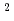 -Arg
-Arg -Ser
-Ser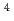 -Gly
-Gly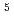 -Leu
-Leu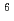 -OH), a linear peptide consisting of six amino acids, has high affinity to HER2/neu receptor overexpressing in various cancer cells. Radiohalogens (radionuclides) such as radioiodine and radiobromine are versatile for clinical imaging and therapeutic applications. Thus, radiohalogenated MARSGL may have potential for clinical applications to HER2 overexpressing tumors. In this study, in order to achieve the labeling of radiohalogen for MARSGL, we design a radioiodinated peptide, F(
-OH), a linear peptide consisting of six amino acids, has high affinity to HER2/neu receptor overexpressing in various cancer cells. Radiohalogens (radionuclides) such as radioiodine and radiobromine are versatile for clinical imaging and therapeutic applications. Thus, radiohalogenated MARSGL may have potential for clinical applications to HER2 overexpressing tumors. In this study, in order to achieve the labeling of radiohalogen for MARSGL, we design a radioiodinated peptide, F( -
- I)MARSGL, in which phenylalanine labeled with
I)MARSGL, in which phenylalanine labeled with  I (t
I (t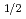 = 8.0 d) at the
= 8.0 d) at the 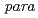 position of the aromatic ring is introduced into the N-terminal of MARSGL and report a new technique to prepare radiohalogen of peptide via electrophilic destanylation.
position of the aromatic ring is introduced into the N-terminal of MARSGL and report a new technique to prepare radiohalogen of peptide via electrophilic destanylation.
佐々木 一郎; 山田 圭一*; 渡邉 茂樹; 花岡 宏史*; 須郷 由美; 奥 浩之*; 石岡 典子
Peptide Science 2013, p.157 - 160, 2013/03
Radioisotope (RI)-labeled peptides which have the high affinity to receptors on surface of the tumor cell are promising for diagnostic radiography (PET and SPECT) and radiotherapy. MARSGL (H-Met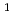 -Ala
-Ala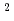 -Arg
-Arg -Ser
-Ser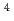 -Gly
-Gly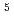 -Leu
-Leu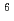 -OH), a linear hexapeptide consisting of six amino acids, has the high affinity to HER2/neu receptor overexpressing in various cancer cells. Thus, radiolabeled MARSGL has potential for the above mentioned purposes. Radiohalogens have various useful radionuclides, which could be introduced to aromatic compounds via tin-halogen exchange reaction. In this study, stannylated peptide Boc-F(
-OH), a linear hexapeptide consisting of six amino acids, has the high affinity to HER2/neu receptor overexpressing in various cancer cells. Thus, radiolabeled MARSGL has potential for the above mentioned purposes. Radiohalogens have various useful radionuclides, which could be introduced to aromatic compounds via tin-halogen exchange reaction. In this study, stannylated peptide Boc-F( -SnBu
-SnBu )MAR(Pbf)S(
)MAR(Pbf)S(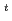 Bu)GL-OH was synthesized to prepare radiohalogen (
Bu)GL-OH was synthesized to prepare radiohalogen ( Br or
Br or  I)-labeled FMARSGL derivatives. First, Boc-Phe(
I)-labeled FMARSGL derivatives. First, Boc-Phe( -SnBu
-SnBu )-OH was prepared from Boc-Phe(
)-OH was prepared from Boc-Phe( -I)-OMe via Pd(0)-catalyzed coupling reaction with (Bu
-I)-OMe via Pd(0)-catalyzed coupling reaction with (Bu Sn)
Sn) and was successfully introduced into
and was successfully introduced into 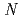 -terminal of H-MARSGL-Trt(2-Cl) resin synthesized from H-Leu-Trt(2-Cl) resin by Fmoc-SPPS. After cleavage reaction of Boc-F(
-terminal of H-MARSGL-Trt(2-Cl) resin synthesized from H-Leu-Trt(2-Cl) resin by Fmoc-SPPS. After cleavage reaction of Boc-F( -SnBu
-SnBu )MAR(Pbf)S(
)MAR(Pbf)S(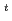 Bu)GL-Trt(2-Cl) resin with 25% 1,1,1,3,3,3-hexafluoro-2-propanol in CH
Bu)GL-Trt(2-Cl) resin with 25% 1,1,1,3,3,3-hexafluoro-2-propanol in CH Cl
Cl , Boc-F(
, Boc-F( -SnBu
-SnBu )MAR(Pbf)S(
)MAR(Pbf)S(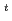 Bu)GL-OH was obtained and identified by using ESI-MS and NMR. Synthesis of
Bu)GL-OH was obtained and identified by using ESI-MS and NMR. Synthesis of  I-labeled FMARSGL is due to report in this presentation.
I-labeled FMARSGL is due to report in this presentation.
 Br-labeled amino acid derivative for PET imaging of tumor
Br-labeled amino acid derivative for PET imaging of tumor花岡 宏史*; 渡邉 茂樹; 富永 英之*; 大島 康宏; 渡辺 智; 山田 圭一*; 飯田 靖彦*; 石岡 典子; 遠藤 啓吾*
JAEA-Review 2012-046, JAEA Takasaki Annual Report 2011, P. 89, 2013/01
近年、がんに対する特異性が高いPET薬剤として、 Cや
Cや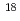 Fで標識したアミノ酸誘導体が開発され、臨床応用されるようになってきた。しかしながら
Fで標識したアミノ酸誘導体が開発され、臨床応用されるようになってきた。しかしながら Cや
Cや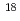 Fは半減期が非常に短いため、それぞれの病院で製造・合成する必要があり、限られた施設でしか使えないのが現状である。一方、
Fは半減期が非常に短いため、それぞれの病院で製造・合成する必要があり、限られた施設でしか使えないのが現状である。一方、 Brは、半減期が16.1時間とポジトロン放出核種としては比較的長く、またハロゲン核種であるため母体化合物との結合にキレート剤等が必要ないことから、アミノ酸のような低分子化合物に対しても応用可能である。そこで本研究では、広く臨床使用することが可能な、新規がん診断用PETイメージング薬剤として
Brは、半減期が16.1時間とポジトロン放出核種としては比較的長く、またハロゲン核種であるため母体化合物との結合にキレート剤等が必要ないことから、アミノ酸のような低分子化合物に対しても応用可能である。そこで本研究では、広く臨床使用することが可能な、新規がん診断用PETイメージング薬剤として Br標識アミノ酸誘導体の開発を計画した。基礎検討には半減期が長い放射性臭素である
Br標識アミノ酸誘導体の開発を計画した。基礎検討には半減期が長い放射性臭素である Br(半減期57時間)を用いて行うこととした。Br標識アミノ酸としては、
Br(半減期57時間)を用いて行うこととした。Br標識アミノ酸としては、 メチルフェニルアラニン(
メチルフェニルアラニン( -Me-Phe)のパラ位にBrを導入したBr-
-Me-Phe)のパラ位にBrを導入したBr- -Me-Pheを設計した。
-Me-Pheを設計した。 Br-
Br- -Me-Pheは標識率25-40%で合成することができた。
-Me-Pheは標識率25-40%で合成することができた。 Br-
Br- -Me-Pheを担癌マウスに投与したところ、腫瘍への高い集積性を示し、投与3時間後の腫瘍対血液比は3.94、腫瘍対筋肉比は3.95であった。
-Me-Pheを担癌マウスに投与したところ、腫瘍への高い集積性を示し、投与3時間後の腫瘍対血液比は3.94、腫瘍対筋肉比は3.95であった。 Br-
Br- -Me-Pheを担癌マウスに投与してPET撮像を行ったところ、腫瘍を明瞭に描出することができた。以上の結果から、
-Me-Pheを担癌マウスに投与してPET撮像を行ったところ、腫瘍を明瞭に描出することができた。以上の結果から、 Br-
Br- -Me-Pheの新規がんイメージング薬剤としての有用性が示唆された。
-Me-Pheの新規がんイメージング薬剤としての有用性が示唆された。
 I]-sansalvamide A derivative
I]-sansalvamide A derivative渡邉 茂樹; 山田 圭一*; 津久井 匠隆*; 花岡 宏史*; 大島 康宏; 山口 藍子*; 奥 浩之*; 石岡 典子
JAEA-Review 2012-046, JAEA Takasaki Annual Report 2011, P. 88, 2013/01
Sansalvamide A (SA), a penta cyclic peptide isolated marine fungus, is a lead compound of anti-cancer reagent because the peptide has cytotoxicity against various cancer cell lines. Halogenated SA derivatives (SA-X, X = Cl, Br, I) was prepared and remarkable cytotocity against malignant human breast cancer. In this study, a radiohalogenated SA derivative [ I]SA-I was prepared to conduct in vivo evaluation of SA derivatives. Synthetic scheme of [
I]SA-I was prepared to conduct in vivo evaluation of SA derivatives. Synthetic scheme of [ I]SA-I are as follows: an iodinated linear peptide, Boc-F(p-I)LLVL-OMe, was prepared by the conventional solid phase peptide synthesis. After preparation of stannylated peptide, Boc-F(p-SnBu
I]SA-I are as follows: an iodinated linear peptide, Boc-F(p-I)LLVL-OMe, was prepared by the conventional solid phase peptide synthesis. After preparation of stannylated peptide, Boc-F(p-SnBu )LLVL-OMe,
)LLVL-OMe,  I was labeled with electrophilic destannylation in the presence of oxidizing reagent. After deprotection of N- and C-termius, [
I was labeled with electrophilic destannylation in the presence of oxidizing reagent. After deprotection of N- and C-termius, [ I]SA-I was obtained successfully by macrocyclization in liquid phase. Overall labeled yield was 7%. To our best knowledge, this report is the first on the synthesis of radiolabeled SA derivative. In vivo evaluation of the SA derivative using [
I]SA-I was obtained successfully by macrocyclization in liquid phase. Overall labeled yield was 7%. To our best knowledge, this report is the first on the synthesis of radiolabeled SA derivative. In vivo evaluation of the SA derivative using [ I]SA-I is being undertaken.
I]SA-I is being undertaken.
 Cu-labeled DOTA-
Cu-labeled DOTA-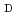 -Phe
-Phe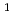 -Tyr
-Tyr -octreotide (
-octreotide ( Cu-DOTA-TOC) for imaging somatostatin receptor-expressing tumors
Cu-DOTA-TOC) for imaging somatostatin receptor-expressing tumors花岡 宏史*; 富永 英之*; 山田 圭一*; Paudyal, P.*; 飯田 靖彦*; 渡邉 茂樹; Paudyal, B.*; 樋口 徹也*; 織内 昇*; 遠藤 啓吾*
Annals of Nuclear Medicine, 23(6), p.559 - 567, 2009/08
被引用回数:19 パーセンタイル:50.64(Radiology, Nuclear Medicine & Medical Imaging)In-111 (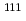 In)-labeled octreotide has been clinically used for imaging somatostatin receptor-positive tumors, and radiolabeled octreotide analogs for positron emission tomography (PET) have been developed. The aim of this study is to produce and fundamentally examine a
In)-labeled octreotide has been clinically used for imaging somatostatin receptor-positive tumors, and radiolabeled octreotide analogs for positron emission tomography (PET) have been developed. The aim of this study is to produce and fundamentally examine a  Cu-labeled octreotide analog,
Cu-labeled octreotide analog,  Cu-1,4,7,10-tetraazacyclododecane-1,4,7,10-tetraacetic acid-
Cu-1,4,7,10-tetraazacyclododecane-1,4,7,10-tetraacetic acid-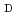 -Phe
-Phe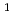 -Tyr
-Tyr -octreotide (
-octreotide ( Cu-DOTA-TOC).
Cu-DOTA-TOC).  Cu-DOTA-TOC can be produced in amounts efficient for clinical study with high radiochemical yield.
Cu-DOTA-TOC can be produced in amounts efficient for clinical study with high radiochemical yield.  Cu-DOTA-TOC was stable in vitro, but time-dependent transchelation to protein was observed after injection into mice. In biodistribution studies, the radioactivity of
Cu-DOTA-TOC was stable in vitro, but time-dependent transchelation to protein was observed after injection into mice. In biodistribution studies, the radioactivity of  Cu was higher than that of
Cu was higher than that of 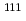 In in all organs except kidney. In tumor-bearing mice,
In in all organs except kidney. In tumor-bearing mice,  Cu-DOTA-TOC showed a high accumulation in the tumors, and the tumor-to-blood ratio reached as high as 8.81
Cu-DOTA-TOC showed a high accumulation in the tumors, and the tumor-to-blood ratio reached as high as 8.81  1.17 at 6 h after administration.
1.17 at 6 h after administration.  Cu-DOTA-TOC showed significantly higher accumulation in the tumor than
Cu-DOTA-TOC showed significantly higher accumulation in the tumor than  Cu-TETA-OC and
Cu-TETA-OC and  Cu-DOTA-OC. PET showed a very clear image of the tumor, which was comparable to that of
Cu-DOTA-OC. PET showed a very clear image of the tumor, which was comparable to that of 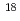 F-FDG PET and very similar to that of
F-FDG PET and very similar to that of  Cu-TETA-OC.
Cu-TETA-OC.  Cu-DOTA-TOC clearly imaged a somatostatin receptor-positive tumor and seemed to be a potential PET tracer in the clinical phase.
Cu-DOTA-TOC clearly imaged a somatostatin receptor-positive tumor and seemed to be a potential PET tracer in the clinical phase.
 enolase
enolase奥 浩之*; 山田 圭一*; 小林 京子*; 片貝 良一*; Ashfaq, M.*; 花岡 宏史*; 飯田 靖彦*; 遠藤 啓吾*; 長谷川 伸; 前川 康成; et al.
Peptide Science 2008, p.439 - 442, 2009/03
マラリアは、熱帯及び亜熱帯地域における主な死因の一つである。これまでの研究において、エノラーゼ基質結合部位の部分配列に由来する人工ペプチド抗原としてマラリアワクチン抗原の有用性を検証してきた。人工抗原ペプチドは、抗原性ペプチドに5(6)-カルボキシフルオロセインを用いて蛍光ラベルして合成した。合成したペプチドは、乳酸とグリコール酸の共重合体(PLGA)を用いて乳化重合後、ホモジナイズし、ナノ粒子化した。この粒子へ再度0.5%ポリビニルアルコールを加えた後、乳化,ホモジナイズして粒子径0.3から1.5mmのナノ粒子を調製した。蛍光強度からみた生体外での徐放試験において、ペプチド抗原のみから作製したナノ球体を用いた場合、薬剤は、保留日数に対してほぼ0次で急激に放出されるのに比べ、PLGAナノ粒子に調製した試料は、1 g/7日間で徐放されることがわかった。1.0mg(蛍光入り薬剤4.0
g/7日間で徐放されることがわかった。1.0mg(蛍光入り薬剤4.0 g)のナノ粒子を用いたハダカネズミによる生体内試験において、蛍光強度は、12日間かけ次第に減少し、今回調製されたナノ微粒子は持続的に抗原を徐放することがわかった。
g)のナノ粒子を用いたハダカネズミによる生体内試験において、蛍光強度は、12日間かけ次第に減少し、今回調製されたナノ微粒子は持続的に抗原を徐放することがわかった。
藤原 治; 大井 圭一*; 山田 和芳*; 加藤 めぐみ*; 小野 有五*; 伊勢 明広*
月刊地球, p.463 - 468, 1997/00
気候・海水準は、地層処分で対象とする長期的将来には現在と大きく変わると考えられる。この為気候・海水順の変化幅や周期性を明らかにし、地下水の涵養量や水質の変化と地質環境の長期安定性に影響を与える情報を整理しておくことが重要である。本研究では、湖沼や内湾等の堆積物を利用して、日本列島周辺の降水量変動などを支配するアジアモンスーンの変動を、過去3.5万年間について調べた。この結果は、国際的にも注目されているアジア地域の気候変動研究に寄与するとともに、過去の気候変動を検出する為の手法の確立にも寄与する。 なお本稿は、月刊地球からの要請で投稿・講演するものである。
山澤 弘実; 永井 晴康; 茅野 政道; 林 隆; 守屋 省三*; 高橋 圭一*; 小島 啓美*; 山田 智久*
JAERI-Data/Code 95-012, 65 Pages, 1995/09
本報告書は、平成5年12月に原研東海研構内の松林を対象に実施した小規模な森林内拡散実験および気象・乱流観測の結果をまとめたものである。拡散実験では、森林内外に設置した線状放出源からの鉛直拡散に着目し、4地点に高さ方向に設置した捕集装置により濃度分布を取得した。得られた拡散データは、図表の形で本報告書に収録した。気象・乱流観測では、超音波風向風速計を森林内外に5ヶ所設置して10Hzのサンプリングで行った。得られたデータは量が膨大で、今後種々の解析で使用されることを考え、統一した形式で光磁気ディスクに収録した。本報告書には、10分平均値及びデータファイルの収録形式のみを記載した。
佐々木 一郎; 花岡 宏史*; 山田 圭一*; 渡辺 茂樹; 須郷 由美; 大島 康宏; 石岡 典子
no journal, ,
生理活性ペプチドは、標的分子への特異性が高いことから分子標的治療薬として期待されているが、標的分子への特異的親和性および生体内での安定性を兼ね備えたペプチドの有効な選抜方法がないことから、薬剤開発が思うように進んでいない。そこで、標的分子に親和性を有するペプチドを感度よく選抜するため、生体内での安定性が期待できるD体アミノ酸由来ペプチドに放射性同位元素(RI)を標識したライブラリーを開発し、新規な医薬品候補化合物の選抜法の考案を計画した。本発表では、選抜法を評価するために、様々ながんに過剰発現するHER2 (ヒト上皮成長因子受容体)を標的分子に選び、ペプチドライブラリーの作製・RI標識・バインディングアッセイを実施した。ペプチド配列中のアミノ酸2残基を固定化し、4残基をランダム化したペプチドライブラリーを18種類のアミノ酸を用いて合成し、N末端に I標識が可能なD体チロシン(y)を導入したペプチドライブラリー(y(3-
I標識が可能なD体チロシン(y)を導入したペプチドライブラリー(y(3- I)-A
I)-A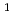 -A
-A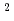 -X
-X -X
-X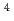 -X
-X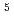 -X
-X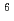 , A:固定, X:ランダム)を作製した。バインディングアッセイの結果、yIIXXXX(固定位置にイソロイシンが二つ配列したライブラリー)がHER2過剰発現細胞株に高い親和性(38-47%dose)を示した。一方、他のライブラリーは低い親和性(約1%dose)を示した。以上より、
, A:固定, X:ランダム)を作製した。バインディングアッセイの結果、yIIXXXX(固定位置にイソロイシンが二つ配列したライブラリー)がHER2過剰発現細胞株に高い親和性(38-47%dose)を示した。一方、他のライブラリーは低い親和性(約1%dose)を示した。以上より、 I標識ペプチドライブラリーを用いることで、がん細胞に特異的親和性を持つペプチド医薬品候補化合物が選抜できる可能性が示唆された。
I標識ペプチドライブラリーを用いることで、がん細胞に特異的親和性を持つペプチド医薬品候補化合物が選抜できる可能性が示唆された。
 Br)の製造と生理活性物質への標識法の検討
Br)の製造と生理活性物質への標識法の検討渡辺 茂樹; 渡辺 智; 花岡 宏史*; 大島 康宏; 山田 圭一*; 須郷 由美; 佐々木 一郎; 鈴木 博元; 石岡 典子
no journal, ,
放射性ハロゲンには、今後核医学検査や治療での利用が期待されているRIも数多くあり、その中でBr-76は核医学検査の可能性をさらに広げるRIとして利用が切望されている。発表ではBr-77を用いたセレン化銅ターゲットからの分離条件の最適化、およびRI特有の条件を考慮したBr-76の標識法として酸化剤を用いた求電子置換反応およびスズ-臭素交換反応による標識の検討結果について発表する。
佐々木 一郎; 花岡 宏史*; 山田 圭一*; 渡辺 茂樹; 須郷 由美; 大島 康宏; 石岡 典子
no journal, ,
生理活性ペプチドは、標的分子への親和性や特異性が高いことから分子標的治療薬として期待されているが、標的分子への特異的親和性及び生体内での安定性を兼ね備えたペプチドの有効な選抜方法がないことから、薬剤開発が思う様に進んでいない。そこで、標的分子に親和性を有するペプチドを感度よく選抜するため、生体内での安定性が期待できるD体アミノ酸由来ペプチドに放射性同位元素(RI)を標識したライブラリーを開発し、新規な医薬品候補化合物の選抜法の開発を計画した。本発表では、選抜法を評価するために、様々ながんに過剰発現するHER2(ヒト上皮成長因子受容体)を標的分子に選び、RI標識ペプチドライブラリーの作製及び細胞結合実験を実施した。配列中の2残基のアミノ酸を固定化し、4残基をランダム化したペプチドライブラリーを18種類のアミノ酸を用いて合成し、N末端に I標識が可能なD体チロシン(y)を導入したペプチドライブラリー(y(3-
I標識が可能なD体チロシン(y)を導入したペプチドライブラリー(y(3- I)-A
I)-A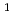 -A
-A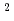 -X
-X -X
-X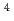 -X
-X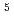 -X
-X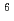 , A:固定, X:ランダム)を作製した。細胞結合実験の結果、yIIXXXX (固定位置にイソロイシンが二つ配列したライブラリー)がHER2過剰発現細胞株に高い親和性(約42%dose)を示した。一方、他のライブラリーは低い親和性(約1%dose)を示した。以上より、
, A:固定, X:ランダム)を作製した。細胞結合実験の結果、yIIXXXX (固定位置にイソロイシンが二つ配列したライブラリー)がHER2過剰発現細胞株に高い親和性(約42%dose)を示した。一方、他のライブラリーは低い親和性(約1%dose)を示した。以上より、 I標識ペプチドライブラリーを用いて、がん細胞に対して親和性を持つペプチドの選抜が可能であることが示唆された。
I標識ペプチドライブラリーを用いて、がん細胞に対して親和性を持つペプチドの選抜が可能であることが示唆された。
渡邉 早貴*; 渡辺 茂樹; 山田 圭一*; 奥 浩之*; 森口 朋尚*; 石岡 典子; 篠塚 和夫*
no journal, ,
放射性標識化アミノ酸・ペプチドは、PETなどの核医学診断において有用な化合物群である。本研究では、ケイ素-ハロゲン交換反応を利用したアミノ酸・ペプチドの新しい標識合成法を開発した。まず、ケイ素置換新規フェニルアラニン誘導体を合成し、次亜塩素酸tert-ブチル(TBHC)を酸化剤としてエタノール中で放射性臭素化を行い、良好な収率で標識化合物[ Br]4-ブロモフェニルアラニン誘導体を得た。
Br]4-ブロモフェニルアラニン誘導体を得た。
津久井 匠隆; 山田 圭一*; 渡邉 茂樹; 花岡 宏史*; 奥 浩之*; 遠藤 啓吾*; 石岡 典子; 松尾 一郎*
no journal, ,
p-(tri-n-butyl-stannyl)-phenylalanine (Phe(p-Bu Sn)) is an useful building blocks for synthesizing radiolabeled pharmaceutics. To best of our knowledge, there are few studies of the synthesis of Phe(p-Bu
Sn)) is an useful building blocks for synthesizing radiolabeled pharmaceutics. To best of our knowledge, there are few studies of the synthesis of Phe(p-Bu Sn)-containing peptides. In this study, we report solid-phase synthesis of cyclic peptides containing Phe(p-Bu
Sn)-containing peptides. In this study, we report solid-phase synthesis of cyclic peptides containing Phe(p-Bu Sn) residue, cyclo(Phe(p-Bu
Sn) residue, cyclo(Phe(p-Bu Sn)-Leu-MeLeu-Val-Leu) (I). Boc-Phe(p-Bu
Sn)-Leu-MeLeu-Val-Leu) (I). Boc-Phe(p-Bu Sn)-OH was synthesized from Boc-Phe(p-I)-OMe by treatment with bis(tri-n-butyl)tin and Pd(0) catalyst followed by saponification. The linear peptide containing Phe(p-Bu
Sn)-OH was synthesized from Boc-Phe(p-I)-OMe by treatment with bis(tri-n-butyl)tin and Pd(0) catalyst followed by saponification. The linear peptide containing Phe(p-Bu Sn) residue was assembled on Kaiser-oxime resin. On-resin macrocyclization of the linear peptide, however, did not afford the cyclic peptide I. Cross coupling of cyclic peptide containing Phe(p-I) residue, cyclo(Phe(p-I)-Leu-MeLeu-Val-Leu) with bis(tri-n-butyl)tin and Pd(0) catalyst gave the desired peptide, which was confirmed by ESI-MS. In this presentation, we will report the Fmoc-SPPS of the peptide I.
Sn) residue was assembled on Kaiser-oxime resin. On-resin macrocyclization of the linear peptide, however, did not afford the cyclic peptide I. Cross coupling of cyclic peptide containing Phe(p-I) residue, cyclo(Phe(p-I)-Leu-MeLeu-Val-Leu) with bis(tri-n-butyl)tin and Pd(0) catalyst gave the desired peptide, which was confirmed by ESI-MS. In this presentation, we will report the Fmoc-SPPS of the peptide I.
 I-Sansalvamide Aの合成と評価
I-Sansalvamide Aの合成と評価渡邉 茂樹; 津久井 匠隆; 花岡 宏史*; 山田 圭一*; 大島 康宏; 飯田 靖彦*; 遠藤 啓吾*; 石岡 典子
no journal, ,
抗がん作用や抗菌作用を示す生理活性物質は、創薬におけるリード化合物となる。Sansalvamide A(SA)は、構造中にエステル結合を有する海洋真菌類由来の環状デプシペプチドで、大腸がん細胞に対して高い細胞毒性を示すことから、抗がん剤開発のリード化合物として注目されている。これまでわれわれは、フェニルアラニン側鎖にヨウ素を導入したSA誘導体を開発し、この化合物が悪性度の高い乳がん細胞MD-MBA-231に対して高い細胞障害活性を示すことを明らかにしてきた。そこで、本研究ではI-SAの生体内における動態を解明するために、 Iを導入した
Iを導入した I-SAを合成し、ノーマルマウスにおける体内分布を明らかにすることとした。
I-SAを合成し、ノーマルマウスにおける体内分布を明らかにすることとした。
山田 圭一*; 渡邉 茂樹; 大島 康宏; 花岡 宏史*; 津久井 匠隆*; 高野 智香子*; 山口 藍子*; 奥 浩之*; 石岡 典子
no journal, ,
Sansalvamide A (SA) is a marin-derived cyclic depsipeptide that exhibits cytotoxicity against colon cancer cell line. Recently, a series of cyclic pentapeptide analogs of SA in which Hmp ((2S)-2-hydroxy-4-methylpentanoic acid) residue was replaced by amino acids or N-methyl-amino acids were synthesized. We previously reported that the haogenated analog of [MeLeu ]SA, namely SA-Br, SA-I, SA-Cl, exhibited potent cytotoxicity against MDA-MB-231. In the present study, we considered to evaluate in vivo biodistribution, stability and antitumor activity of these halogenated SA peptides in tumor-bearing mice. For this purpose, radiohalogen atoms are most suitable for labeling without changing their primary structure and biological activity. Here, we report the synthesis and in vivo biodistribution of
]SA, namely SA-Br, SA-I, SA-Cl, exhibited potent cytotoxicity against MDA-MB-231. In the present study, we considered to evaluate in vivo biodistribution, stability and antitumor activity of these halogenated SA peptides in tumor-bearing mice. For this purpose, radiohalogen atoms are most suitable for labeling without changing their primary structure and biological activity. Here, we report the synthesis and in vivo biodistribution of  I-labeled SA analog (SA-[
I-labeled SA analog (SA-[ I]).
I]).
 Br標識アミノ酸の開発
Br標識アミノ酸の開発花岡 宏史*; 渡邉 茂樹; 富永 英之*; 大島 康宏; 渡辺 智; 山田 圭一*; 荒野 泰*; 石岡 典子; 遠藤 啓吾*
no journal, ,
近年、がんに対する特異性が高いPET薬剤として、 Cや
Cや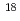 Fで標識したアミノ酸誘導体が開発され、臨床応用されるようになってきた。しかしながら
Fで標識したアミノ酸誘導体が開発され、臨床応用されるようになってきた。しかしながら Cや
Cや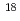 Fは半減期が非常に短いため、それぞれの病院で製造・合成する必要があり、限られた施設でしか使えないのが現状である。一方、
Fは半減期が非常に短いため、それぞれの病院で製造・合成する必要があり、限られた施設でしか使えないのが現状である。一方、 Brは、半減期が16.1時間とポジトロン放出核種としては比較的長く、またハロゲン核種であるため母体化合物との結合にキレート剤等が必要ないことから、アミノ酸のような低分子化合物に対しても応用可能である。そこで本研究では、広く臨床使用することが可能な、新規がん診断用PETイメージング薬剤として
Brは、半減期が16.1時間とポジトロン放出核種としては比較的長く、またハロゲン核種であるため母体化合物との結合にキレート剤等が必要ないことから、アミノ酸のような低分子化合物に対しても応用可能である。そこで本研究では、広く臨床使用することが可能な、新規がん診断用PETイメージング薬剤として Br標識アミノ酸誘導体の開発を計画した。基礎検討には半減期が長い放射性臭素である
Br標識アミノ酸誘導体の開発を計画した。基礎検討には半減期が長い放射性臭素である Br(半減期57時間)を用いて行うこととした。Br標識アミノ酸としては、
Br(半減期57時間)を用いて行うこととした。Br標識アミノ酸としては、 メチルフェニルアラニン(
メチルフェニルアラニン( -Me-Phe)のパラ位にBrを導入したBr-
-Me-Phe)のパラ位にBrを導入したBr- -Me-Pheを設計した。
-Me-Pheを設計した。 Br-
Br- -Me-Pheは標識率25-40%で合成することができた。
-Me-Pheは標識率25-40%で合成することができた。 Br-
Br- -Me-Pheを担癌マウスに投与したところ、腫瘍への高い集積性を示し、投与3時間後の腫瘍対血液比は3.94、腫瘍対筋肉比は3.95であった。
-Me-Pheを担癌マウスに投与したところ、腫瘍への高い集積性を示し、投与3時間後の腫瘍対血液比は3.94、腫瘍対筋肉比は3.95であった。 Br-
Br- -Me-Pheを担癌マウスに投与し、6時間後にPET撮像を行ったところ、腫瘍を明瞭に描出することができた。以上の結果から、
-Me-Pheを担癌マウスに投与し、6時間後にPET撮像を行ったところ、腫瘍を明瞭に描出することができた。以上の結果から、 Br-
Br- -Me-Pheの新規がんイメージング薬剤としての有用性が示唆された。
-Me-Pheの新規がんイメージング薬剤としての有用性が示唆された。
津久井 匠隆; 渡邉 茂樹; 花岡 宏史*; 山田 圭一*; 奥 浩之*; 石岡 典子; 遠藤 啓吾*; 松尾 一郎*
no journal, ,
生理活性ペプチドには顕著な抗腫瘍活性を示すものがあり、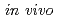 での治療効果に興味が持たれている。これらの生理活性ペプチドにおける構造活性相関等の創薬研究は、さまざまな所で行われている。創薬研究では、薬剤の体内分布や腫瘍への集積能が重要な因子となり得る。演者らは、放射性核種を標識した生理活性ペプチドを用いて体内での薬剤挙動と治療効果を同時に計測できれば薬剤開発の効率化が可能になると考え、その標識化法を検討している。本発表では、Boc-Phe(
での治療効果に興味が持たれている。これらの生理活性ペプチドにおける構造活性相関等の創薬研究は、さまざまな所で行われている。創薬研究では、薬剤の体内分布や腫瘍への集積能が重要な因子となり得る。演者らは、放射性核種を標識した生理活性ペプチドを用いて体内での薬剤挙動と治療効果を同時に計測できれば薬剤開発の効率化が可能になると考え、その標識化法を検討している。本発表では、Boc-Phe(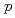 -SnBu
-SnBu )-OMeを前駆体としたBr-77標識アミノ酸の合成に関する基礎的検討について報告する。酸化剤にChloramine T、N-Chlorosuccinimideを用いて室温30分間標識化したところ、その標識率は60
)-OMeを前駆体としたBr-77標識アミノ酸の合成に関する基礎的検討について報告する。酸化剤にChloramine T、N-Chlorosuccinimideを用いて室温30分間標識化したところ、その標識率は60 85%であった。現在、Phe(
85%であった。現在、Phe(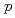 -SnBu
-SnBu )含有ペプチドへの適用も検討しており、併せて報告する予定である。
)含有ペプチドへの適用も検討しており、併せて報告する予定である。
渡辺 茂樹; 山田 圭一*; 渡邉 早貴*; 奥 浩之*; 森口 朋尚*; 篠塚 和夫*; 石岡 典子
no journal, ,
Br-76 (half-life: 16.1 h) is of interest for in vivo imaging using PET. Therefore, Br-76 labeled peptides which have high affinity to tumor cells are promising PET tracers for tumor imaging. Tin-halogen exchange reaction have been used for radiobromination. However, it is likely that synthesis of stannylated peptides is difficult because stannyl group is readily eliminated under acidic condition. Silicon-carbon bond is resistant to acid, leading us to employ silicon-bromine exchange reaction for the radiobromination. In this study, we are aiming to synthesize a radiobrominated phenylalanine derivative via the silicon-bromine exchange reaction as a feasible study.